Формула количества теплоты при нагревании газа. Расчёт количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении
ТЕПЛООБМЕН.
1.Теплообмен.
Теплообмен или теплопередача – это процесс передачи внутренней энергии одного тела другому без совершения работы.
Существуют три вида теплообмена.
1) Теплопроводность – это теплообмен между телами при их непосредственном контакте.
2) Конвекция – это теплообмен, при котором перенос тепла осуществляется потоками газа или жидкости.
3) Излучение – это теплообмен посредством электромагнитного излучения.
2.Количество теплоты.
Количество теплоты – это мера изменения внутренней энергии тела при теплообмене. Обозначается буквой Q .
Единица измерения количества теплоты = 1 Дж.
Количество теплоты, полученное телом от другого тела в результате теплообмена, может тратиться на увеличение температуры (увеличение кинетической энергии молекул) или на изменение агрегатного состояния (увеличение потенциальной энергии).
3.Удельная теплоёмкость вещества.
Опыт показывает, что количество теплоты, необходимое для нагревания тела массой m от температуры Т 1 до температуры Т 2 пропорционально массе тела m и разности температур (Т 2 – Т 1), т.е.
Q = cm (Т 2 – Т 1 ) = с m Δ Т,
с называется удельной теплоёмкостью вещества нагреваемого тела.
![]()
Удельная теплоёмкость вещества равна количеству теплоту, которое необходимо сообщить 1 кг вещества, чтобы нагреть его на 1 К.
Единица измерения удельной теплоёмкости =.
Значения теплоёмкости различных веществ можно найти в физических таблицах.
Точно такое же количество теплоты Q будет выделяться при охлаждении тела на ΔТ.
4.Удельная теплота парообразования.
Опыт показывает, что количество теплоты, необходимое для превращения жидкости в пар, пропорционально массе жидкости, т.е.
Q = Lm ,
где коэффициент пропорциональности L называется удельной теплотой парообразования.
Удельная теплота парообразования равна количеству теплоты, которое необходимо для превращения в пар 1 кг жидкости, находящейся при температуре кипения.
Единица измерения удельной теплоты парообразования .
При обратном процессе, конденсации пара, теплота выделяется в том же количестве, которое затрачено на парообразование.
5.Удельная теплота плавления.
Опыт показывает, что количество теплоты, необходимое для превращения твёрдого тела в жидкость, пропорционально массе тела, т.е.
Q = λ m ,
где коэффициент пропорциональности λ называется удельной теплотой плавления.
Удельная теплота плавления равна количеству теплоты, которое необходимо для превращения в жидкость твёрдого тела массой 1 кг при температуре плавления.
Единица измерения удельной теплоты плавления .
При обратном процессе, кристаллизации жидкости, теплота выделяется в том же количестве, которое затрачено на плавление.
6.Удельная теплота сгорания.
Опыт показывает, что количество теплоты, выделяемое при полном сгорании топлива, пропорционально массе топлива, т.е.
Q = q m ,
Где коэффициент пропорциональности q называется удельной теплотой сгорания.
Удельная теплота сгорания равна количеству теплоты, которое выделяется при полном сгорании 1 кг топлива.
Единица измерения удельной теплоты сгорания.
7.Уравнение теплового баланса.
В теплообмене участвуют два или более тела. Одни тела отдают теплоту, а другие принимают. Теплообмен происходит до тех пор, пока температуры тел не станут равными. По закону сохранения энергии, количество теплоты, которое отдаётся, равно количеству, которое принимается. На этом основании записывается уравнение теплового баланса.
Рассмотрим пример.
Тело массой m 1 ,
теплоёмкость которого с 1 ,
имеет температуру Т 1 ,
а тело массой m 2 ,
теплоёмкость которого с 2 ,
имеет температуру Т 2 .
Причём Т 1
больше Т 2 .
Эти тела приведены в соприкосновение.
Опыт показывает, что холодное тело (m 2)
начинает нагреваться, а горячее тело
(m 1)
– охлаждаться. Это говорит о том, что
часть внутренней энергии горячего тела
передаётся холодному, и температуры
выравниваются. Обозначим конечную общую
температуру θ.
Количество теплоты, переданной горячим телом холодному
Q передан. = c 1 m 1 (Т 1 – θ )
Количество теплоты, полученной холодным телом от горячего
Q получен. = c 2 m 2 (θ – Т 2 )
По закону сохранения энергии Q передан. = Q получен. , т.е.
c 1 m 1 (Т 1 – θ )= c 2 m 2 (θ – Т 2 )
Раскроем скобки и выразим значение общей установившейся температуры θ.
![]()
Значение температуры θ в данном случае получим в кельвинах.
Однако, так как в выражениях для Q передан. и Q получен. стоит разность двух температур, а она и в кельвинах, и в градусах Цельсия одинакова, то расчёт можно вести и в градусах Цельсия. Тогда
![]()
В этом случае значение температуры θ получим в градусах Цельсия.
Выравнивание температур в результате теплопроводности можно объяснить на основании молекулярно-кинетической теории как обмен кинетической энергией между молекулами при сталкивании в процессе теплового хаотического движения.
Этот пример можно
проиллюстрировать графиком.
1. Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количеством теплоты .
Количеством теплоты называется изменение внутренней энергии тела в процессе теплопередачи без совершения работы.
Количество теплоты обозначают буквой \(Q \) . Так как количество теплоты является мерой изменения внутренней энергии, то его единицей является джоуль (1 Дж).
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
2. Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество теплоты требуется ему для нагревания. То же самое и с охлаждением: тело большей массы при охлаждении отдаёт большее количество теплоты. Эти тела сделаны из одного и того же вещества и нагреваются они или охлаждаются на одно и то же число градусов.
3. Если теперь нагревать 100 г воды от 30 до 60 °С, т.е. на 30 °С, а затем до 100 °С, т.е. на 70 °С, то в первом случае на нагревание уйдёт меньше времени, чем во втором, и, соответственно, на нагревание воды на 30 °С, будет затрачено меньшее количество теплоты, чем на нагревание воды на 70 °С. Таким образом, количество теплоты прямо пропорционально разности конечной \((t_2\,^\circ C) \) и начальной \((t_1\,^\circ C) \) температур: \(Q\sim(t_2-t_1) \) .
4. Если теперь в один сосуд налить 100 г воды, а в другой такой же сосуд налить немного воды и положить в неё такое металлическое тело, чтобы его масса и масса воды составляли 100 г, и нагревать сосуды на одинаковых плитках, то можно заметить, что в сосуде, в котором находится только вода, температура будет ниже, чем в том, в котором находятся вода и металлическое тело. Следовательно, чтобы температура содержимого в обоих сосудах была одинаковой нужно воде передать большее количество теплоты, чем воде и металлическому телу. Таким образом, количество теплоты, необходимое для нагревания тела зависит от рода вещества, из которого это тело сделано.
5. Зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества .
Физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К), называется удельной теплоёмкостью вещества.
Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой \(c \) . Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Удельная теплоёмкость свинца 140 Дж/кг °С. Это значит, что для нагревания 1 кг свинца на 1 °С необходимо затратить количество теплоты 140 Дж. Такое же количество теплоты выделится при остывании 1 кг воды на 1 °С.
Поскольку количество теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты \(Q \) , необходимое для нагревания тела массой \(m \) от температуры \((t_1\,^\circ C) \) до температуры \((t_2\,^\circ C) \) , равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
\[ Q=cm(t_2{}^\circ-t_1{}^\circ) \]
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
6. Пример решения задачи . В стакан, содержащий 200 г воды при температуре 80 °С, налили 100 г воды при температуре 20 °С. После чего в сосуде установилась температура 60 °С. Какое количество теплоты получила холодная вода и отдала горячая вода?
При решении задачи необходимо выполнять следующую последовательность действий:
- записать кратко условие задачи;
- перевести значения величин в СИ;
- проанализировать задачу, установить, какие тела участвуют в теплообмене, какие тела отдают энергию, а какие получают;
- решить задачу в общем виде;
- выполнить вычисления;
- проанализировать полученный ответ.
1. Условие задачи .
Дано:
\(m_1 \)
= 200 г
\(m_2 \)
= 100 г
\(t_1 \)
= 80 °С
\(t_2 \)
= 20 °С
\(t \)
= 60 °С
______________
\(Q_1 \)
— ? \(Q_2 \)
— ?
\(c_1 \)
= 4200 Дж/кг · °С
2. СИ: \(m_1 \) = 0,2 кг; \(m_2 \) = 0,1 кг.
3. Анализ задачи . В задаче описан процесс теплообмена между горячей и холодной водой. Горячая вода отдаёт количество теплоты \(Q_1 \) и охлаждается от температуры \(t_1 \) до температуры \(t \) . Холодная вода получает количество теплоты \(Q_2 \) и нагревается от температуры \(t_2 \) до температуры \(t \) .
4. Решение задачи в общем виде . Количество теплоты, отданное горячей водой, вычисляется по формуле: \(Q_1=c_1m_1(t_1-t) \) .
Количество теплоты, полученное холодной водой, вычисляется по формуле: \(Q_2=c_2m_2(t-t_2) \) .
5.
Вычисления
.
\(Q_1 \)
= 4200 Дж/кг · °С · 0,2 кг · 20 °С = 16800 Дж
\(Q_2 \)
= 4200 Дж/кг · °С · 0,1 кг · 40 °С = 16800 Дж
6. В ответе получено, что количество теплоты, отданное горячей водой, равно количеству теплоты, полученному холодной водой. При этом рассматривалась идеализированная ситуация и не учитывалось, что некоторое количество теплоты пошло на нагревание стакана, в котором находилась вода, и окружающего воздуха. В действительности же количество теплоты, отданное горячей водой, больше, чем количество теплоты, полученное холодной водой.
Часть 1
1. Удельная теплоёмкость серебра 250 Дж/(кг · °С). Что это означает?
1) при остывании 1 кг серебра на 250 °С выделяется количество теплоты 1 Дж
2) при остывании 250 кг серебра на 1 °С выделяется количество теплоты 1 Дж
3) при остывании 250 кг серебра на 1 °С поглощается количество теплоты 1 Дж
4) при остывании 1 кг серебра на 1 °С выделяется количество теплоты 250 Дж
2. Удельная теплоёмкость цинка 400 Дж/(кг · °С). Это означает, что
1) при нагревании 1 кг цинка на 400 °С его внутренняя энергия увеличивается на 1 Дж
2) при нагревании 400 кг цинка на 1 °С его внутренняя энергия увеличивается на 1 Дж
3) для нагревания 400 кг цинка на 1 °С его необходимо затратить 1 Дж энергии
4) при нагревании 1 кг цинка на 1 °С его внутренняя энергия увеличивается на 400 Дж
3. При передаче твёрдому телу массой \(m \) количества теплоты \(Q \) температура тела повысилась на \(\Delta t^\circ \) . Какое из приведённых ниже выражений определяет удельную теплоёмкость вещества этого тела?
1) \(\frac{m\Delta t^\circ}{Q} \)
2) \(\frac{Q}{m\Delta t^\circ} \)
3) \(\frac{Q}{\Delta t^\circ} \)
4) \(Qm\Delta t^\circ \)
4. На рисунке приведён график зависимости количества теплоты, необходимого для нагревания двух тел (1 и 2) одинаковой массы, от температуры. Сравните значения удельной теплоёмкости (\(c_1 \) и \(c_2 \) ) веществ, из которых сделаны эти тела.

1) \(c_1=c_2 \)
2) \(c_1>c_2 \)
3) \(c_1
5. На диаграмме представлены значения количества теплоты, переданного двум телам равной массы при изменении их температуры на одно и то же число градусов. Какое соотношение для удельных теплоёмкостей веществ, из которых изготовлены тела, является верным?

1) \(c_1=c_2 \)
2) \(c_1=3c_2 \)
3) \(c_2=3c_1 \)
4) \(c_2=2c_1 \)
6. На рисунке представлен график зависимости температуры твёрдого тела от отданного им количества теплоты. Масса тела 4 кг. Чему равна удельная теплоёмкость вещества этого тела?

1) 500 Дж/(кг · °С)
2) 250 Дж/(кг · °С)
3) 125 Дж/(кг · °С)
4) 100 Дж/(кг · °С)
7. При нагревании кристаллического вещества массой 100 г измеряли температуру вещества и количество теплоты, сообщённое веществу. Данные измерений представили в виде таблицы. Считая, что потерями энергии можно пренебречь, определите удельную теплоёмкость вещества в твёрдом состоянии.
1) 192 Дж/(кг · °С)
2) 240 Дж/(кг · °С)
3) 576 Дж/(кг · °С)
4) 480 Дж/(кг · °С)
8. Чтобы нагреть 192 г молибдена на 1 К, нужно передать ему количество теплоты 48 Дж. Чему равна удельная теплоёмкость этого вещества?
1) 250 Дж/(кг · К)
2) 24 Дж/(кг · К)
3) 4·10 -3 Дж/(кг · К)
4) 0,92 Дж/(кг · К)
9. Какое количество теплоты необходимо для нагревания 100 г свинца от 27 до 47 °С?
1) 390 Дж
2) 26 кДж
3) 260 Дж
4) 390 кДж
10. На нагревание кирпича от 20 до 85 °С затрачено такое же количество теплоты, как для нагревания воды такой же массы на 13 °С. Удельная теплоёмкость кирпича равна
1) 840 Дж/(кг · К)
2) 21000 Дж/(кг · К)
3) 2100 Дж/(кг · К)
4) 1680 Дж/(кг · К)
11. Из перечня приведённых ниже высказываний выберите два правильных и запишите их номера в таблицу.
1) Количество теплоты, которое тело получает при повышении его температуры на некоторое число градусов, равно количеству теплоты, которое это тело отдаёт при понижении его температуры на такое же число градусов.
2) При охлаждении вещества его внутренняя энергия увеличивается.
3) Количество теплоты, которое вещество получает при нагревании, идёт главным образом на увеличение кинетической энергии его молекул.
4) Количество теплоты, которое вещество получает при нагревании, идёт главным образом на увеличение потенциальной энергии взаимодействия его молекул
5) Внутреннюю энергию тела можно изменить, только сообщив ему некоторое количество теплоты
12. В таблице представлены результаты измерений массы \(m \) , изменения температуры \(\Delta t \) и количества теплоты \(Q \) , выделяющегося при охлаждении цилиндров, изготовленных из меди или алюминия.

Какие утверждения соответствуют результатам проведённого эксперимента? Из предложенного перечня выберите два правильных. Укажите их номера. На основании проведенных измерений можно утверждать, что количество теплоты, выделяющееся при охлаждении,
1) зависит от вещества, из которого изготовлен цилиндр.
2) не зависит от вещества, из которого изготовлен цилиндр.
3) увеличивается при увеличении массы цилиндра.
4) увеличивается при увеличении разности температур.
5) удельная теплоёмкость алюминия в 4 раза больше, чем удельная теплоёмкость олова.
Часть 2
C1. Твёрдое тело массой 2 кг помещают в печь мощностью 2 кВт и начинают нагревать. На рисунке изображена зависимость температуры \(t \) этого тела от времени нагревания \(\tau \) . Чему равна удельная теплоёмкость вещества?

1) 400 Дж/(кг · °С)
2) 200 Дж/(кг · °С)
3) 40 Дж/(кг · °С)
4) 20 Дж/(кг · °С)
Ответы


Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количествоv теплоты.
– это изменение внутренней энергии тела в процессе теплопередачи без совершения работы. Количество теплоты обозначают буквой Q .
Работа, внутренняя энергия и количество теплоты измеряются в одних и тех же единицах - джоулях (Дж ), как и всякий вид энергии.
В тепловых измерениях в качестве единицы количества теплоты раньше использовалась особая единица энергии - калория (кал ), равная количеству теплоты, необходимому для нагревания 1 грамма воды на 1 градус Цельсия (точнее, от 19,5 до 20,5 °С). Данную единицу, в частности, используют в настоящее время при расчетах потребления тепла (тепловой энергии) в многоквартирных домах. Опытным путем установлен механический эквивалент теплоты - соотношение между калорией и джоулем: 1 кал = 4,2 Дж .
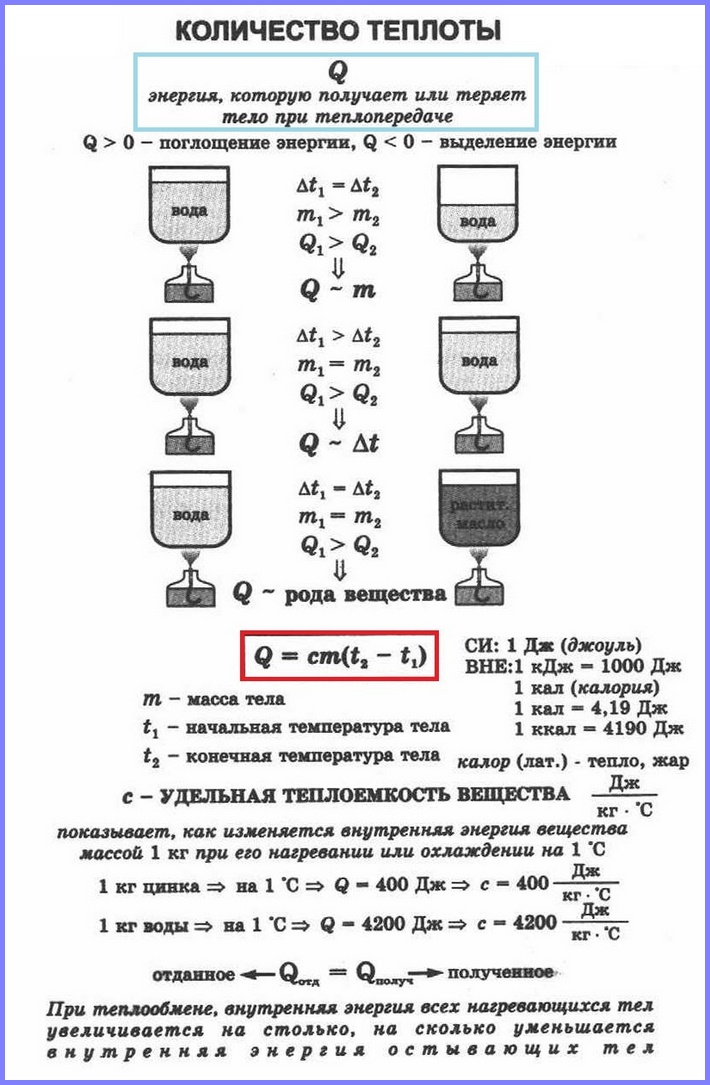
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество тепла требуется ему для нагревания. То же самое и с охлаждением.

Количество теплоты, необходимое для нагревания тела зависит еще и от рода вещества, из которого это тело сделано. Эта зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
– это физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К). Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой с . Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг °К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Поскольку кол-во теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С . В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Q , необходимое для нагревания тела массой m от температуры t 1 °С до температуры t 2 °С , равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.Q = c ∙ m (t 2 — t 1)
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.

Это конспект по теме «Количество теплоты. Удельная теплоёмкость» . Выберите дальнейшие действия:
- Перейти к следующему конспекту:
Изменить внутреннюю энергию газа в цилиндре можно не только совершая работу, но и нагревая газ (рис. 43). Если закрепить поршень, то объем газа не будет изменяться, но температура, а следовательно, и внутренняя энергия будут возрастать.
Процесс передачи энергии от одного тела к другому без совершения работы называют теплообменом или теплопередачей.
Энергию, переданную телу в результате теплообмена, называют количеством теплоты. Количеством теплоты называют также энергию, которую тело отдает в процессе теплообмена.
Молекулярная картина теплообмена. При теплообмене на границе между телами происходит взаимодействие медленно движущихся молекул холодного тела с более быстро движущимися молекулами горячего тела. В результате кинетические энергии
молекул выравниваются и скорости молекул холодного тела увеличиваются, а горячего уменьшаются.
При теплообмене не происходит превращения энергии из одной формы в другую: часть внутренней энергии горячего тела передается холодному телу.
Количество теплоты и теплоемкость. Из курса физики VII класса известно, что для нагревания тела массой от температуры до температуры необходимо сообщить ему количество теплоты
![]()
При остывании тела, его конечная температура меньше начальной и количество теплоты, отдаваемое телом, отрицательно.
Коэффициент с в формуле (4.5) называют удельной теплоемкостью. Удельная теплоемкость - это количество теплоты, которое получает или отдает 1 кг вещества при изменении его температуры на 1 К-
Удельную теплоемкость выражают в джоулях, деленных на килограмм, умноженный на кельвин. Различным телам требуется неодинаковое количество энергии для увеличения температуры на I К. Так, удельная теплоемкость воды а меди
Удельная теплоемкость зависит не только от свойств вещества, но и от того, при каком процессе осуществляется теплопередача Если нагревать газ при постоянном давлении, то он будет расширяться и совершать работу. Для нагревания газа на 1 °С при постоянном давлении ему нужно будет передать большее количество теплоты, чем для нагревания его при постоянном объеме.
Жидкие и твердые тела расширяются при нагревании незначительно, и их удельные теплоемкости при постоянном объеме и постоянном давлении мало различаются.
Удельная теплота парообразования. Для превращения жидкости в пар необходима передача ей определенного количества теплоты. Температура жидкости при этом превращении не меняется. Превращение жидкости в пар при постоянной температуре не ведет к увеличению кинетической энергии молекул, но сопровождается увеличением их потенциальной энергии. Ведь среднее расстояние между молекулами газа во много раз больше, чем между молекулами жидкости. Кроме того, увеличение объема при переходе вещества из жидкого состояния в газообразное требует совершения работы против сил внешнего да вления.
Количество теплоты, необходимое для превращения при постоянной температуре 1 кг жидкости в пар, называют
удельной теплотой парообразования. Обозначают эту величину буквой и выражают в джоулях на килограмм
Очень велика удельная теплота парообразования воды: при температуре 100°С. У других жидкостей (спирт, эфир, ртуть, керосин и др.) удельная теплота парообразования меньше в 3-10 раз.
Для превращения в пар жидкости массой требуется количество теплоты, равное:
При конденсации пара происходит выделение такого же количества теплоты:
Удельная теплота плавления. При плавлении кристаллического тела вся подводимая к нему теплота идет на увеличение потенциальной энергии молекул. Кинетическая энергия молекул не меняется, так как плавление происходит при постоянной температуре.
Количество теплоты А, необходимое для превращения 1 кг кристаллического вещества при температуре плавления в жидкость той же температуры, называют удельной теплотой плавления.
При кристаллизации I кг вещества выделяется точно такое же количество теплоты. Удельная теплота плавления льда довольно велика:
Для того чтобы расплавить кристаллическое тело массой необходимо количество теплоты, равное:
Количество теплоты, выделяемое при кристаллизации тела, равно:
1. Что называют количеством теплоты? 2. От чего зависит удельная теплоемкость веществ? 3. Что называют удельной теплотой парообразования? 4. Что называют удельной теплотой плавления? 5. В каких случаях количество переданной теплоты отрицательно?
Как известно, при различных механических процессах происходит изменение механической энергии W meh . Мерой изменения механической энергии является работа сил, приложенных к системе:
\(~\Delta W_{meh} = A.\)
При теплообмене происходит изменение внутренней энергии тела. Мерой изменения внутренней энергии при теплообмене является количество теплоты.
Количество теплоты - это мера изменения внутренней энергии, которую тело получает (или отдает) в процессе теплообмена.
Таким образом, и работа, и количество теплоты характеризуют изменение энергии, но не тождественны энергии. Они не характеризуют само состояние системы, а определяют процесс перехода энергии из одного вида в другой (от одного тела к другому) при изменении состояния и существенно зависят от характера процесса.
Основное различие между работой и количеством теплоты состоит в том, что работа характеризует процесс изменения внутренней энергии системы, сопровождающийся превращением энергии из одного вида в другой (из механической во внутреннюю). Количество теплоты характеризует процесс передачи внутренней энергии от одних тел к другим (от более нагретых к менее нагретым), не сопровождающийся превращениями энергии.
Опыт показывает, что количество теплоты, необходимое для нагревания тела массой m от температуры T 1 до температуры T 2 , рассчитывается по формуле
\(~Q = cm (T_2 - T_1) = cm \Delta T, \qquad (1)\)
где c - удельная теплоемкость вещества;
\(~c = \frac{Q}{m (T_2 - T_1)}.\)
Единицей удельной теплоемкости в СИ является джоуль на килограмм-Кельвин (Дж/(кг·К)).
Удельная теплоемкость c численно равна количеству теплоты, которое необходимо сообщить телу массой 1 кг, чтобы нагреть его на 1 К.
Теплоемкость тела C T численно равна количеству теплоты, необходимому для изменения температуры тела на 1 К:
\(~C_T = \frac{Q}{T_2 - T_1} = cm.\)
Единицей теплоемкости тела в СИ является джоуль на Кельвин (Дж/К).
Для превращения жидкости в пар при неизменной температуре необходимо затратить количество теплоты
\(~Q = Lm, \qquad (2)\)
где L - удельная теплота парообразования. При конденсации пара выделяется такое же количество теплоты.
Для того чтобы расплавить кристаллическое тело массой m при температуре плавления, необходимо телу сообщить количество теплоты
\(~Q = \lambda m, \qquad (3)\)
где λ - удельная теплота плавления. При кристаллизации тела такое же количество теплоты выделяется.
Количество теплоты, которое выделяется при полном сгорании топлива массой m ,
\(~Q = qm, \qquad (4)\)
где q - удельная теплота сгорания.
Единица удельных теплот парообразования, плавления и сгорания в СИ - джоуль на килограмм (Дж/кг).
Литература
Аксенович Л. А. Физика в средней школе: Теория. Задания. Тесты: Учеб. пособие для учреждений, обеспечивающих получение общ. сред, образования / Л. А. Аксенович, Н.Н.Ракина, К. С. Фарино; Под ред. К. С. Фарино. - Мн.: Адукацыя i выхаванне, 2004. - C. 154-155.




