Яичниковая и надпочечниковая гиперандрогения – как женскому организму справиться с мужскими гормонами? Идиопатическая гиперандрогения. Лечение и симптомы гиперандрогении у женщин Гиперандрогения у женщин симптомы имеет трех типов
Патологическое состояние гормонального баланса в женском организме, при котором происходит избыточное производство мужских половых гормонов – андрогенов имеет название гиперандрогенией. Заболевание связано с нарушениями в работе эндокринной системы. Синдром гиперандрогении отмечают примерно у 5-7 % женщин, около 20 % из них не могут забеременеть или выносить ребенка.
В норме андрогены вырабатываются половыми органами в количестве, которое обеспечивает рост волосяного покрова на лобке и в области подмышек, формирование клитора, своевременное половое созревание и сексуальное влечение. Андрогены несут ответственность за нормальную работу печени и почек.
Активная выработка андрогенов происходит в подростковом возрасте, во время формирования вторичных половых признаков. В зрелом возрасте андрогены необходимы для укрепления костной ткани. Однако, чрезмерная выработка данных гормонов приводит к патологическим изменениям, которые значительно ухудшают качество жизни женщины. К наиболее плачевным результатам относятся и . В этих случаях необходимо лечение, которое будет способствовать нормализации гормонального фона.
Разновидности и причины синдрома
Процесс созревания андрогенов происходит в яичниках и надпочечниках. Нормальное количество вырабатываемого гормона и его правильное соотношение с эстрогенами обеспечивает необходимый для полноценного функционирования организма гормональный баланс.
В зависимости от происхождения патологии выделяют несколько ее форм:
- Гиперандрогения яичникового генеза – возникает при синдроме поликистозных яичников. Причина – нарушение работы системы гипоталамус-гипофиз. Нарушение носит наследственный характер.
- Гиперандрогения надпочечникового генеза вызвана нарушением работы коры надпочечников. Заболевание носит врожденный характер, а также может быть вызвано опухолями (болезнь Иценко-Кушинга). В этом случае первые месячные начинаются поздно, со скудными выделениями, а со временем могут и вовсе прекратиться. Другие характерные признаки – обилие угрей в области спины и груди, недоразвитие молочных желез, формирование фигуры по мужскому типу, увеличение клитора.
У ряда пациенток диагностируются гиперандрогения смешанного генеза. В этом случае в организме одновременно нарушено функционирование яичников и надпочечников. Данная патология вызвана гипоталамическими и нейроэндокринными нарушениями. Сбои в гормональном балансе усугубляются вегетативно-невротическими расстройствами. В ряде случаев диагностируется слабовыраженная гиперандрогения, при которой показатели андрогенов отвечают норме, а не обнаруживает наличие опухолей во внутренних органах.
Смешанная форма препятствует наступлению беременности и делает невозможным успешное вынашивание ребенка.
Учитывая степень превышения допустимого уровня андрогенов, выделяют абсолютную и относительную форму адреногенитального синдрома. В первом случае концентрация мужских гормонов превышает допустимые нормы. Относительная гиперандрогения диагностируется при допустимых показателях мужских гормонов. При этом отмечают повышенную чувствительность органов и желез женщины к их воздействию.
Подводя итог, можно выделить следующие главные причины данного синдрома:
- неправильная выработка особого фермента, синтезирующего андрогены, в результате чего происходит их чрезмерное накопление в организме;
- наличие опухолей надпочечников;
- заболевания и сбои в работе яичников, провоцирующие излишнюю выработку андрогенов;
- патологии щитовидной железы (гипотериоз), опухоли гипофиза;
- длительный прием стероидов во время профессиональных занятий силовыми видами спорта;
- ожирение в детском возрасте;
- генетическая предрасположенность.
При нарушениях работы яичников, увеличении коры надпочечников, гиперчувствительности клеток кожи к воздействию тестостерона, опухолях половых и щитовидных желез возможно развитие патологии и в детском возрасте.
Врожденная гиперандрогения иногда не позволяет с точностью установить пол родившегося ребенка. У девочки могут отмечаться большие половые губы, увеличенный до размеров пениса клитор. Внешний вид внутренних половых органов соответствует норме.
Одной из разновидностей адреногенитального синдрома является сольтеряющая форма. Заболевание носит наследственный характер и обычно выявляется в первые месяцы жизни ребенка. В результате неудовлетворительной работы надпочечников у девочек появляется рвота, диарея, судороги.
В старшем возрасте гиперандрогения вызывает избыточный рост волос по всему телу, задержку формирования молочных желез и появление первых месячных.
Клинические проявления
Симптомы могут варьировать от незначительных (избыточный рост волос на теле) до тяжелых (развитие вторичных мужских половых признаков).

Клинические проявления гиперандрогении у женщин в виде акне и оволосения по мужскому типу
Главными проявлениями патологических нарушений являются:
- акне – возникает при повышенной жирности кожи, которая приводит к закупорке и воспалениям сальных желез;
- себорея волосистой кожи головы;
- гирсутизм – появление сильного оволосения в местах нетипичных для женщин (лице, груди, животе, ягодицах);
- истончение и выпадение волос на голове, появление залысин;
- усиленный рост мышц, формирование мускулатуры по мужскому типу;
- огрубление тембра голоса;
- , скудость выделений, иногда полное прекращение менструаций;
- повышенное половое влечение.
Происходящие сбои в гормональном балансе становятся причиной развития сахарного диабета, появления лишнего веса, нарушений липидного обмена. Женщины становятся очень восприимчивы к различным инфекционным заболеваниям. У них нередко развиваются депрессии, хроническая усталость, повышенная раздражительность и общая слабость.
Одним из наиболее тяжелых последствий гиперандрогении является вирилизация или вирильный синдром. Так называют патологию развития женского организма, при которой он приобретает ярко выраженные мужские признаки. Вирилизация относится к редким отклонениям, ее диагностируют только у одной пациентки из 100, у которых отмечают чрезмерный рост волос на теле.
У женщины формируется мужская фигура с усиленным ростом мышц, полностью прекращаются месячные, значительно увеличивается размеры клитора. Очень часто подобные признаки развиваются у женщин, которые бесконтрольно принимают стероиды для повышения выносливости и физической силы при занятиях спортом.
Постановка диагноза
Диагностика патологического состояния включает внешний и гинекологический осмотр пациентки, анализ ее жалоб на общее самочувствие. Обращают внимание на длительность менструального цикла, локализацию избыточного оволосения, индекс массы тела, внешний вид половых органов.
Какие анализы нужно сдать для определения уровня андрогенов?
Врачи (гинеколог, эндокринолог, генетик) назначают следующие исследования:
- определение уровня тестостерона, фолликулярного гормона, пролактина, эстрадиола в крови и кортизола в моче;
- пробы с дексеметазоном для определения причины развития синдрома;
- УЗИ яичников и надпочечников;
- КТ гипофиза;
- исследования уровня глюкозы, инсулина, холестерина.
УЗИ органов малого таза позволит определить возможное наличие . Проведение анализов необходимо для установки разновидности заболевания.
Материалы для исследований берут в утренние часы, до приема пищи. Поскольку гормональный фон отличается нестабильностью, для точного диагностирования берут три пробы с перерывами не менее получаса. Желательно сдавать анализы во второй половине менструального цикла, ближе к предполагаемому началу месячных.
Принципы терапии
Лечение гиперандрогении должно быть комплексным и, в первую очередь, направлено на устранение проблем и заболеваний, которые выступают провоцирующими факторами. В перечень таких болезней входят патологии щитовидной железы, синдром поликистозных яичников, адреногенитальный синдром.
Выбор методов лечения зависит от формы патологии и цели, которую преследует терапия (борьба с гирсутизмом, восстановление репродуктивной функции, сохранение беременности при угрозе выкидыша).
Главные лечебные меры включают:
- медикаментозную терапию;
- хирургическое вмешательство;
- использование средств народной медицины;
- нормализацию питания и физические нагрузки.
Консервативная терапия
Применяется для снижения количества вырабатываемых мужских гормонов и для блокировки процессов, которые способствуют их чрезмерной активности. Наличие опухолей в половых органах, вызывающее яичниковую гиперандрогению, устраняется при помощи хирургического вмешательства.
Если в ближайшее время женщина не планирует беременность, но страдает от угревой сыпи и чрезмерного количества волос на теле, для избавления от данных симптомов назначают с антиандрогенным действием (например, Диане 35).
Подобные препараты не только устраняют неприятные внешние признаки, но и способствуют нормализации менструального цикла. Для косметического эффекта назначают противовоспалительные мази, которые уменьшают выработку кожного сала.
При наличии противопоказаний к применению контрацептивов для лечения применяют Спиронолактон. Его назначают при тяжелом протекании предменструального синдрома и при поликистозных яичниках. Препарат успешно лечит угревую сыпь и избыточный рост волос.
Аналоговым препаратом является Верошпирон. Его главным действующим веществом также является спиронолактон. Прием Верошпирона крайне нежелателен без согласования с врачом длительности использования и необходимой дозировки.
Если гипреандрогения вызвана отсутствием фермента, превращающего андрогены в глюкокортикоиды, показаны средства, которые нормализуют данный процесс. Большой эффективностью обладает препарат Метипред. Формы его выпуска – таблетки и порошки для инъекций. Средство противопоказано при наличии инфекционных и вирусных заболеваний, туберкулеза, сердечной недостаточности. Длительность курса лечения и дозировку определяет врач.

Препараты применяемые для лечения гиперандрогении
Одним из успешных методов консервативного лечения является низкокалорийная диета. Она необходима для избавления от лишнего веса, который нередко осложняет течение заболевания и приносит женщине дополнительный психологический дискомфорт.
Общее количество калорий, употребляемых ежедневно, не должен превышать 2000. В этом случае, при достаточной физической активности, количество потребляемых калорий будет ниже расходуемых, что и приведет к постепенному снижению веса.
Диета, показанная при гиперандрогении, предусматривает исключение из рациона жирной, соленой и острой пищи, а также алкоголя, соусов и жирных подлив.
Соблюдение принципов правильного питания подкрепляется регулярными занятиями спортом. Полезны бег, аэробика, плавание, активные игры на свежем воздухе.
Борьбу с гирсутизмом проводят, используя различные косметические процедуры: удаление при помощи воска, депиляция, устранение нежелательных волос лазером.
Применение народной медицины
Лечение народными средствами вполне применимо в комплексе медикаментозной терапии, но не является полноценной заменой традиционным способам.
Популярные рецепты:
- Травы донника, шалфея, лабазника и спорыша в равных долях смешивают, заливают 200 мл воды, держат на водяной бане в течение 20 минут и процеживают. К полученному отвару добавляют 1,5 мл настойки родиолы розовой. Принимают отвар по трети стакана несколько раз в день до приема пищи.
- 2 столовые ложки измельченной череды, 1 ложку тысячелистника и пустырника заливают кипятком, настаивают примерно час, процеживают. Принимают по половине стакана натощак утром и перед сном.
- Несколько столовых ложек сухих листьев крапивы заливают стаканом воды, настаивают в закрытой посудине, процеживают. Принимают несколько раз в день по столовой ложке.
- Плоды шиповника, черной смородины заливают кипятком, настаивают около часа. Затем добавляют немного меда. Полученный коктейль пьют несколько раз в сутки после еды.
Среди наиболее распространенных народных средств в борьбе с заболеваниями гинекологической сферы – боровая матка. Ее используют совместно с другими лечебными средствами в виде отвара или настойки.
- 100 г боровой матки залить 500 мл водки и настаивать в течение 2 недель. Настойку принимать по 0,5 чайной ложки три раза в день.
- 2 столовые ложки боровой матки залить стаканом кипятка, настаивать около часа. Пить небольшими порциями в течение дня.
- 100 г зеленых очищенных орехов и боровой матки смешать с 800 г сахара, добавить такое же количество водки. Бутылку со смесью поставить в темное место на 14 дней. После процеживания принимать по чайной ложке за полчаса до принятия пищи.
Для уменьшения количества производимых андрогенов используют мяту. На ее основе готовят настойки и чаи. Для большей эффективности к мяте можно добавить расторопшу. Нормализует женский гормональный баланс регулярный прием зеленого чая.
Как лечить проблему при помощи лечебных трав и сочетать этот метод с другими видами лечения, всегда подскажет лечащий врач. Заниматься самолечением недопустимо!
Гиперандрогения и бесплодие
Избыток производимых андрогенов нередко становится препятствием для желанной беременности.
Как забеременеть при помощи медикаментозной терапии и насколько это реально?
Лечение бесплодия в этом случае направлено на использование препаратов, стимулирующих выход яйцеклетки из яичников. Примером такого лекарственного средства может быть Кломифен.

Одним из наиболее эффективных препаратов, используемых для стимуляции овуляции и нормализации менструального цикла, является Дюфастон. После наступления беременности прием препарата продолжают, чтобы предотвратить выкидыш и нормализовать развитие беременности.
Если стимуляция оказывается неэффективной, врачи советуют прибегнуть к хирургическому лечению. Современная медицина широко применяет метод . Во время проведения этой процедуры производят иссечение яичников, чтобы помочь «выходу» зрелой яйцеклетки. Вероятность забеременеть после лапароскопии тем выше, чем меньше времени проходит со дня операции. Максимальная способность к зачатию отмечается в первые три месяца.
Но и после успешного зачатия наличие гиперандрогении может воспрепятствовать успешному вынашиванию ребенка. Избыток мужских гормонов часто приводит к тому, что плодное яйцо не может удержаться в матке. Вероятность выкидыша сохраняется высокой.
Опасные недели беременности при гиперандрогении – это период до 12-й недели и после 19-й. В первом случае гормоны вырабатываются плацентой, а после 19-й недели они могут продуцироваться самим плодом.
Для сохранения беременности пациентке назначают Дексаметазон (метипред). Он способствует снижению уровня андрогена. Дозировку препарата подбирает исключительно врач!
Многие будущие мамы очень боятся побочных эффектов препарата и опасаются, что он может нанести вред еще не родившемуся малышу. Многолетний опыт применения данного препарата доказывает его безопасность, как для развития будущего ребенка, так и для протекания самих родов.
В большинстве случаев, чтобы избежать риска выкидыша врачи советуют сначала пройти полный курс лечения, а уже затем планировать беременность. Если женщине не удается зачать ребенка, возможно проведение .
Профилактика
Каких-либо специфических мер профилактики гиперандрогении не существует, поскольку данный синдром развивается на гормональном уровне.
К общим профилактическим мерам относят:
- рациональное питание, включающее в меню продукты, богатые клетчаткой, контроль веса;
- отказ от курения и злоупотребления алкоголем;
- регулярное посещение гинеколога;
- прием лекарственных препаратов и противозачаточных средств только после рекомендации врача;
- своевременное лечение патологий щитовидной железы, заболеваний печени и надпочечников.
Гиперандрогения – это не только проблемы с кожей, волосами и менструальным циклом. Это общее заболевание организма, которое не позволяет женщине вести качественный образ жизни и зачастую лишает ее радостей материнства. Современные методы диагностики и лечения позволяют вовремя выявить патологию и успешно устранять ее проявления.
Когда речь идет о таком заболевании, как гиперандрогения у женщин, причины симптомы, лечение и профилактические меры всегда связаны с такой проблемой, как воздействие адрогенов на организм. Этот процесс приводит к появлению в женской внешности мужских черт и другим не очень приятным изменениям. Если говорить более подробно, то речь идет о таких проявлениях, как появление растительности на лице и теле, низкий голос, а также изменения некоторых элементов фигуры.
Стоит отметить тот факт, что данная патология женской эндокринной системы встречается часто, и способна не только привести к неприятным внешним изменениям, но и стать причиной бесплодия. Поэтому при появлении первых симптомов гиперандрогении, нужно сразу же планировать визит к врачу.
Почему развивается патология
Тема «гиперандрогения у женщин: причины симптомы, лечение» очень важна для представительниц слабого пола, поскольку проявляется данная проблема приблизительно у 20% пациенток. Поэтому есть смысл обратить внимание на те факторы и процессы, которые приводят к развитию этого заболевания.
В качестве основной причины можно определить АГС — адреногенитальный синдром. Суть в том, что надпочечники способны вырабатывать много других гормонов, помимо адрогенов, например, глюкокортикоиды. Последние появляются под воздействием определенного фермента. Основой для их возникновения являются накопившиеся андрогены. Иногда у женщин уже при рождении присутствует дефект фермента, в результате чего мужские гормоны не преобразуются, а накапливаются на постоянной основе, становясь причиной неприятных изменений в женском организме.
Есть еще один процесс, по причине которого развивается гиперандрогения надпочечникового генеза. Речь идет об опухолях надпочечников. Формируются они также на фоне увеличения концентрации андрогенов.
Риск развития упомянутой выше патологии появляется и в том случае, когда происходит выработка мужских гормонов в яичниках женщины. Более того, клетки, которые вырабатывают адрогены, могут стать причиной образования опухоли в области яичников.
Синдром гиперандрогении иногда является следствием воздействия патологий других эндокринных органов, например, гипофиза.
Признаки избытка андрогенов
Если говорить о клинических симптомах повышенной концентрации мужского гормона, то их можно описать следующим образом:
- угревая сыпь;
- выпадение волос и залысины в области лба (адрогенная алопеция);

- сальные железы начинают вырабатывать чрезмерное количество секрета, вследствие чего жирность кожи повышается;
- барифония, что означает понижение тембра голоса;
- на животе и груди появляются волосы.
Стоит отметить тот факт, что гирсутизм — избыточный рост терминальных волос на женском теле, диагностируется у 80% пациенток, с такой проблемой, как синдром гиперандрогении.
При подобном заболевании у некоторых представительниц слабого пола возможно нарушение менструального цикла, полное отсутствие месячных, а также гипертрофия миокарда, ожирение, бесплодие и гипертония.
Концентрация мужских гормонов может стать причиной усиления восприимчивости женского организма к инфекциям различного типа. Возможна также быстрая утомляемость и склонность к депрессии.
Угри и сальные железы
Чтобы ясно понимать, что делать с такой проблемой, как гиперандрогения у женщин, причины, симптомы, лечение и диагностику стоит рассмотреть основательно. Поскольку факторы, обуславливающие развитие заболевания, были рассмотрены выше, есть смысл изучить особенности симптоматики.
Если касаться такой проблемы как угри, то стоит отметить, что они являются следствием ороговения стенок фолликула и повышенной выработки кожного сала, которую стимулирует концентрация андрогенов, в том числе и в плазме. При таких симптомах, как правило, назначают КОК или антиандрогены, что позволяет ощутимо улучшить состояние пациентки.

Также под воздействием мужских гормонов в андрогенозависимых зонах появляются пигментированные, толстые, грубые волосы вместо пушковых. Обычно это происходит в пубертатном периоде. При этом воздействие андрогена на область бровей, ресниц, височных и затылочных частей остается минимальным.
Надпочечниковая гиперандрогения
Стоит напомнить о том, что надпочечники — это две эндокринные железы, которые находятся непосредственно над самими почками.
Именно они являются источником 95% вырабатываемого андрогена (ДЭА-сульфат). Сложность гиперандрогении, связанной с этими железами, сводится к тому факту, что патология имеет врожденный характер и дает о себе знать на фоне андрогенитального синдрома. Он приводит к критическому снижению в женском организме уровня ферментов, необходимых для выработки таких гормонов, как глюкокортикоиды.
Гиперандрогения надпочечникового генеза оубсловлена именно этим дефицитом, который приводит к увеличению концентрации других гормонов — прегненолона, прогестерона и др. Такие изменения завершаются увеличенной выработкой андрогена в женском организме.

Иногда диагностируется патология, которая была вызвана опухолями надпочечников, выделяющих мужской гормон. По статистике такая форма болезни как надпочечниковая гиперандрогения фиксируется у 30-50% женщин, имеющих проблемы с андрогеном.
Воздействие на яичники
Высокая концентрация мужских гормонов может повлиять и на функционирование яичников. В большинстве случаев данная проблема дает о себе знать посредством двух форм: гипертекоз и поликистоз. Важно обратить внимание на тот факт, что риск развития данной патологии у женщин возрастает при регулярных занятиях силовыми видами спорта.
Яичниковая гиперандрогения является следствием замедления роста фолликулов под воздействием андрогенов. Поскольку из них и состоят яичники, итогом подобных процессов становится заращение последних. Медицинское название этой проблемы — фолликулярная атрезия.
Но это не все сложности, которыми сопровождается гиперандрогения яичников генеза. Суть в том, что мужской гормон играет роль фактора, на фоне которого развивается патологическое образование волокнистой соединительной ткани, что приводит к поликистозу. В данной ситуации хорошей новостью является тот факт, что с подобной проблемой сталкивается всего лишь 5% женщин.

Также стоит отметить, что данная форма гиперандрогении у представительниц слабого пола является причиной сбоя центральной регуляции уровня андрогенов. Происходит данный процесс на уровне гипоталамуса и гипофиза. В итоге гормональный фон ощутимо изменяется.
Признаки, на которые стоит обратить внимание
Есть ряд симптомов, свидетельствующих о появлении описанной выше проблемы. О том, что имеет место быть такая патология как гиперандрогения яичников генеза, можно узнать по следующим проявлениям:
- остеопороз;
- себорея;
- на лице, помимо угрей, появляется шелушение и воспаления, которые трудно нейтрализовать привычными косметологическими методами;
- атрофия мышц;
- лишний вес;
- изменение пропорций женского тела — маскулинизация;
- огрубение голоса (барифония);
- рост волос по всему телу, даже на лице;
- образование залысин на голове.
Помимо этого, есть еще много вторичных симптомов, таких как повышение уровня глюкозы в крови, артериальная гипертония, понижение иммунитета и др.
Лишний вес
Ожирение у женщин может вызвать описанная выше яичниковая гиперандрогения. При данной форме патологии нередко фиксируется повышение уровня эстрадиола.
Медиками было проведено исследование, согласно которому подтвердилась следующая информация: как высокий уровень мужского гормона, так и образующие под его влиянием эстрогены, оказывают самое непосредственное влияние на развитие ожирения, соответствующего мужскому типу.

Такие процессы являются причиной усиления инсулинозависимости и последующего роста концентрации мужского гормона в организме женщин, страдающих описанной выше патологией. В некоторых случаях андрогены оказывают влияние не вес женщины через центральную нервную систему.
Смешанная форма
Врачам с определенной периодичностью приходится сталкиваться с проявлением нескольких форм гиперандрогении. Объясняется такая ситуация тем фактом, что в одно и то же время происходит нарушение функций надпочечников и яичников.
Возможность подобного осложнения важно учитывать при изучении того, чем опасна гиперандрогения у женщин. По сути, происходит вот что: надпочечниковые андрогены, концентрируясь в надпочечниках, тем самым повышают уровень мужского гормона в яичниках. Этот процесс происходит и в крови, что влечет усиленное продуцирование лютеинизирующего гормона. Последний, в свою очередь, провоцирует появление гиперандрогенного синдрома.
Возникновение смешанной формы патологии может быть обусловлено сильными травмами, интоксикацией мозга или опухолью гипофиза.
Диагностика
Изначально врач должен отделить гиперандрогению от других заболеваний, на фоне которых она развивается (акромегалия, синдром Кушинга, болезни печени и др.). Следующим этапом является определение гормонального уровня. Эта процедура должна проводиться на голодный желудок в утреннее время. Подобный анализ необходимо выполнить три раза, поскольку гормональный фон при высокой концентрации андрогена постоянно изменяется.

Внимание обращается на уровень дегидроэпиандростерона, высокое содержание которого будет свидетельствовать о надпочечниковой гиперандрогении. Важен также и уровень кетостероидов в моче. Если его содержание выходит за пределы нормы, то есть смысл подозревать развитие патологии.
Методы лечения
Гиперандрогения — это слишком серьезная проблема, чтобы игнорировать помощь квалифицированных медиков. И если проанализировать весь курс лечения, то можно сделать вывод, что он направлен на достижение 4 ключевых целей:
- устранений проявлений на коже;
- нормализация менструального цикла;
- лечение бесплодия, которое было вызвано ановуляцией;
- ликвидация и профилактика метаболических нарушений, сопутствующих основному заболеванию.
Диета при гиперандрогении у женщин назначается в случае значительного повышения веса. В этом случае важно в точности придерживаться всех рекомендаций врача, только при соблюдении этого условия можно получить нужный результат.
Тем пациенткам, которые намерены иметь ребенка, в большинстве случаев назначается гормональная терапия, способная обеспечить полноценную овуляцию.

Женщины, не планирующие беременность, проходят лечение, включающее оральные контрацептивы, а в некоторых случаях клиновидное иссечение яичников.
Препараты для лечения гиперандрогении у женщин также активно применяются, если организм не способен нейтрализовать высокий уровень андрогена самостоятельно. Речь идет о таких средствах, как «Метипред», «Дексаметазон» и др. Оперативное вмешательство может быть назначено в том случае, если патология спровоцирована опухолью.
Итоги
Высокая концентрация мужского гормона в женском организме — это более чем серьезная проблема, которая часто развивается на фоне не менее опасных заболеваний. Поэтому при появлении первых симптомов диагностику и лечение нужно проводить в обязательном порядке.
Разновидности и причины синдрома
Процесс созревания андрогенов происходит в яичниках и надпочечниках. Нормальное количество вырабатываемого гормона и его правильное соотношение с эстрогенами обеспечивает необходимый для полноценного функционирования организма гормональный баланс.
В зависимости от происхождения патологии выделяют несколько ее форм:
- Гиперандрогения яичникового генеза – возникает при синдроме поликистозных яичников. Причина – нарушение работы системы гипоталамус-гипофиз. Нарушение носит наследственный характер.
- Гиперандрогения надпочечникового генеза вызвана нарушением работы коры надпочечников. Заболевание носит врожденный характер, а также может быть вызвано опухолями (болезнь Иценко-Кушинга). В этом случае первые месячные начинаются поздно, со скудными выделениями, а со временем могут и вовсе прекратиться. Другие характерные признаки – обилие угрей в области спины и груди, недоразвитие молочных желез, формирование фигуры по мужскому типу, увеличение клитора.
У ряда пациенток диагностируются гиперандрогения смешанного генеза. В этом случае в организме одновременно нарушено функционирование яичников и надпочечников. Данная патология вызвана гипоталамическими и нейроэндокринными нарушениями. Сбои в гормональном балансе усугубляются вегетативно-невротическими расстройствами. В ряде случаев диагностируется слабовыраженная гиперандрогения, при которой показатели андрогенов отвечают норме, а УЗИ не обнаруживает наличие опухолей во внутренних органах.
Смешанная форма препятствует наступлению беременности и делает невозможным успешное вынашивание ребенка.
Учитывая степень превышения допустимого уровня андрогенов, выделяют абсолютную и относительную форму адреногенитального синдрома. В первом случае концентрация мужских гормонов превышает допустимые нормы. Относительная гиперандрогения диагностируется при допустимых показателях мужских гормонов. При этом отмечают повышенную чувствительность органов и желез женщины к их воздействию.
Подводя итог, можно выделить следующие главные причины данного синдрома:
- неправильная выработка особого фермента, синтезирующего андрогены, в результате чего происходит их чрезмерное накопление в организме;
- наличие опухолей надпочечников;
- заболевания и сбои в работе яичников, провоцирующие излишнюю выработку андрогенов;
- патологии щитовидной железы (гипотериоз), опухоли гипофиза;
- длительный прием стероидов во время профессиональных занятий силовыми видами спорта;
- ожирение в детском возрасте;
- генетическая предрасположенность.
При нарушениях работы яичников, увеличении коры надпочечников, гиперчувствительности клеток кожи к воздействию тестостерона, опухолях половых и щитовидных желез возможно развитие патологии и в детском возрасте.
Врожденная гиперандрогения иногда не позволяет с точностью установить пол родившегося ребенка. У девочки могут отмечаться большие половые губы, увеличенный до размеров пениса клитор. Внешний вид внутренних половых органов соответствует норме.
Одной из разновидностей адреногенитального синдрома является сольтеряющая форма. Заболевание носит наследственный характер и обычно выявляется в первые месяцы жизни ребенка. В результате неудовлетворительной работы надпочечников у девочек появляется рвота, диарея, судороги.
В старшем возрасте гиперандрогения вызывает избыточный рост волос по всему телу, задержку формирования молочных желез и появление первых месячных.
Клинические проявления
Симптомы могут варьировать от незначительных (избыточный рост волос на теле) до тяжелых (развитие вторичных мужских половых признаков).
Главными проявлениями патологических нарушений являются:
- акне – возникает при повышенной жирности кожи, которая приводит к закупорке и воспалениям сальных желез;
- себорея волосистой кожи головы;
- гирсутизм – появление сильного оволосения в местах нетипичных для женщин (лице, груди, животе, ягодицах);
- истончение и выпадение волос на голове, появление залысин;
- усиленный рост мышц, формирование мускулатуры по мужскому типу;
- огрубление тембра голоса;
- нарушение менструального цикла, скудость выделений, иногда полное прекращение менструаций;
- повышенное половое влечение.
Происходящие сбои в гормональном балансе становятся причиной развития сахарного диабета, появления лишнего веса, нарушений липидного обмена. Женщины становятся очень восприимчивы к различным инфекционным заболеваниям. У них нередко развиваются депрессии, хроническая усталость, повышенная раздражительность и общая слабость.
Одним из наиболее тяжелых последствий гиперандрогении является вирилизация или вирильный синдром. Так называют патологию развития женского организма, при которой он приобретает ярко выраженные мужские признаки. Вирилизация относится к редким отклонениям, ее диагностируют только у одной пациентки из 100, у которых отмечают чрезмерный рост волос на теле.
У женщины формируется мужская фигура с усиленным ростом мышц, полностью прекращаются месячные, значительно увеличивается размеры клитора. Очень часто подобные признаки развиваются у женщин, которые бесконтрольно принимают стероиды для повышения выносливости и физической силы при занятиях спортом.
Постановка диагноза
Диагностика патологического состояния включает внешний и гинекологический осмотр пациентки, анализ ее жалоб на общее самочувствие. Обращают внимание на длительность менструального цикла, локализацию избыточного оволосения, индекс массы тела, внешний вид половых органов.
Какие анализы нужно сдать для определения уровня андрогенов?
Врачи (гинеколог, эндокринолог, генетик) назначают следующие исследования:
- определение уровня тестостерона, фолликулярного гормона, пролактина, эстрадиола в крови и кортизола в моче;
- пробы с дексеметазоном для определения причины развития синдрома;
- УЗИ яичников и надпочечников;
- КТ гипофиза;
- исследования уровня глюкозы, инсулина, холестерина.
УЗИ органов малого таза позволит определить возможное наличие поликистоза яичников. Проведение анализов необходимо для установки разновидности заболевания.
Материалы для исследований берут в утренние часы, до приема пищи. Поскольку гормональный фон отличается нестабильностью, для точного диагностирования берут три пробы с перерывами не менее получаса. Желательно сдавать анализы во второй половине менструального цикла, ближе к предполагаемому началу месячных.
Принципы терапии
Лечение гиперандрогении должно быть комплексным и, в первую очередь, направлено на устранение проблем и заболеваний, которые выступают провоцирующими факторами. В перечень таких болезней входят патологии щитовидной железы, синдром поликистозных яичников, адреногенитальный синдром.
Выбор методов лечения зависит от формы патологии и цели, которую преследует терапия (борьба с гирсутизмом, восстановление репродуктивной функции, сохранение беременности при угрозе выкидыша).
Главные лечебные меры включают:
- медикаментозную терапию;
- хирургическое вмешательство;
- использование средств народной медицины;
- нормализацию питания и физические нагрузки.
Консервативная терапия
Применяется для снижения количества вырабатываемых мужских гормонов и для блокировки процессов, которые способствуют их чрезмерной активности. Наличие опухолей в половых органах, вызывающее яичниковую гиперандрогению, устраняется при помощи хирургического вмешательства.
Если в ближайшее время женщина не планирует беременность, но страдает от угревой сыпи и чрезмерного количества волос на теле, для избавления от данных симптомов назначают оральные контрацептивы с антиандрогенным действием (например, Диане 35).
Подобные препараты не только устраняют неприятные внешние признаки, но и способствуют нормализации менструального цикла. Для косметического эффекта назначают противовоспалительные мази, которые уменьшают выработку кожного сала.
При наличии противопоказаний к применению контрацептивов для лечения применяют Спиронолактон. Его назначают при тяжелом протекании предменструального синдрома и при поликистозных яичниках. Препарат успешно лечит угревую сыпь и избыточный рост волос.
Аналоговым препаратом является Верошпирон. Его главным действующим веществом также является спиронолактон. Прием Верошпирона крайне нежелателен без согласования с врачом длительности использования и необходимой дозировки.
Если гипреандрогения вызвана отсутствием фермента, превращающего андрогены в глюкокортикоиды, показаны средства, которые нормализуют данный процесс. Большой эффективностью обладает препарат Метипред. Формы его выпуска – таблетки и порошки для инъекций. Средство противопоказано при наличии инфекционных и вирусных заболеваний, туберкулеза, сердечной недостаточности. Длительность курса лечения и дозировку определяет врач.
Одним из успешных методов консервативного лечения является низкокалорийная диета. Она необходима для избавления от лишнего веса, который нередко осложняет течение заболевания и приносит женщине дополнительный психологический дискомфорт.
Общее количество калорий, употребляемых ежедневно, не должен превышать 2000. В этом случае, при достаточной физической активности, количество потребляемых калорий будет ниже расходуемых, что и приведет к постепенному снижению веса.
Диета, показанная при гиперандрогении, предусматривает исключение из рациона жирной, соленой и острой пищи, а также алкоголя, соусов и жирных подлив.
Соблюдение принципов правильного питания подкрепляется регулярными занятиями спортом. Полезны бег, аэробика, плавание, активные игры на свежем воздухе.
Борьбу с гирсутизмом проводят, используя различные косметические процедуры: удаление при помощи воска, депиляция, устранение нежелательных волос лазером.
Применение народной медицины
Лечение народными средствами вполне применимо в комплексе медикаментозной терапии, но не является полноценной заменой традиционным способам.
Популярные рецепты:
- Травы донника, шалфея, лабазника и спорыша в равных долях смешивают, заливают 200 мл воды, держат на водяной бане в течение 20 минут и процеживают. К полученному отвару добавляют 1,5 мл настойки родиолы розовой. Принимают отвар по трети стакана несколько раз в день до приема пищи.
- 2 столовые ложки измельченной череды, 1 ложку тысячелистника и пустырника заливают кипятком, настаивают примерно час, процеживают. Принимают по половине стакана натощак утром и перед сном.
- Несколько столовых ложек сухих листьев крапивы заливают стаканом воды, настаивают в закрытой посудине, процеживают. Принимают несколько раз в день по столовой ложке.
- Плоды шиповника, черной смородины заливают кипятком, настаивают около часа. Затем добавляют немного меда. Полученный коктейль пьют несколько раз в сутки после еды.
Среди наиболее распространенных народных средств в борьбе с заболеваниями гинекологической сферы – боровая матка. Ее используют совместно с другими лечебными средствами в виде отвара или настойки.
- 100 г боровой матки залить 500 мл водки и настаивать в течение 2 недель. Настойку принимать по 0,5 чайной ложки три раза в день.
- 2 столовые ложки боровой матки залить стаканом кипятка, настаивать около часа. Пить небольшими порциями в течение дня.
- 100 г зеленых очищенных орехов и боровой матки смешать с 800 г сахара, добавить такое же количество водки. Бутылку со смесью поставить в темное место на 14 дней. После процеживания принимать по чайной ложке за полчаса до принятия пищи.
Для уменьшения количества производимых андрогенов используют мяту. На ее основе готовят настойки и чаи. Для большей эффективности к мяте можно добавить расторопшу. Нормализует женский гормональный баланс регулярный прием зеленого чая.
Как лечить проблему при помощи лечебных трав и сочетать этот метод с другими видами лечения, всегда подскажет лечащий врач. Заниматься самолечением недопустимо!
Гиперандрогения и бесплодие
Избыток производимых андрогенов нередко становится препятствием для желанной беременности.
Как забеременеть при помощи медикаментозной терапии и насколько это реально?
Лечение бесплодия в этом случае направлено на использование препаратов, стимулирующих выход яйцеклетки из яичников. Примером такого лекарственного средства может быть Кломифен.

Одним из наиболее эффективных препаратов, используемых для стимуляции овуляции и нормализации менструального цикла, является Дюфастон. После наступления беременности прием препарата продолжают, чтобы предотвратить выкидыш и нормализовать развитие беременности.
Если стимуляция оказывается неэффективной, врачи советуют прибегнуть к хирургическому лечению. Современная медицина широко применяет метод лапароскопии. Во время проведения этой процедуры производят иссечение яичников, чтобы помочь «выходу» зрелой яйцеклетки. Вероятность забеременеть после лапароскопии тем выше, чем меньше времени проходит со дня операции. Максимальная способность к зачатию отмечается в первые три месяца.
Но и после успешного зачатия наличие гиперандрогении может воспрепятствовать успешному вынашиванию ребенка. Избыток мужских гормонов часто приводит к тому, что плодное яйцо не может удержаться в матке. Вероятность выкидыша сохраняется высокой.
Опасные недели беременности при гиперандрогении – это период до 12-й недели и после 19-й. В первом случае гормоны вырабатываются плацентой, а после 19-й недели они могут продуцироваться самим плодом.
Для сохранения беременности пациентке назначают Дексаметазон (метипред). Он способствует снижению уровня андрогена. Дозировку препарата подбирает исключительно врач!
Многие будущие мамы очень боятся побочных эффектов препарата и опасаются, что он может нанести вред еще не родившемуся малышу. Многолетний опыт применения данного препарата доказывает его безопасность, как для развития будущего ребенка, так и для протекания самих родов.
В большинстве случаев, чтобы избежать риска выкидыша врачи советуют сначала пройти полный курс лечения, а уже затем планировать беременность. Если женщине не удается зачать ребенка, возможно проведение ЭКО.
Причины
Гиперандрогения – проявление широкого спектра синдромов. Специалисты называют три наиболее вероятные причины гиперандрогении:
- повышение уровня андрогенов в сыворотке крови;
- превращение андрогенов в метаболически активные формы;
- активная утилизация андрогенов в тканях-мишенях вследствие аномальной чувствительности андрогенных рецепторов.
Чрезмерный синтез мужских половых гормонов, как правило, связан с нарушением функции яичников. Чаще всего встречается синдром поликистозных яичников (СПКЯ) – образование множественных мелких кист на фоне комплекса эндокринных расстройств, включая патологии щитовидной и поджелудочной железы, гипофиза, гипоталамуса и надпочечников. Заболеваемость СПКЯ среди женщин фертильного возраста достигает 5–10%.
Гиперсекреция андрогенов также наблюдается при следующих эндокринопатиях:
- адреногенитальный синдром;
- врожденная гиперплазия надпочечников;
- синдром галактореи-аменореи;
- стромальный текоматоз и гипертекоз;
- вирилизирующие опухоли яичников и надпочечников, продуцирующие мужские гормоны.
Гиперандрогения на почве трансформации половых стероидов в метаболически активные формы часто вызывается разнообразными нарушениями липидно-углеводного обмена, сопровождающихся инсулинорезистентностью и ожирением. Чаще всего наблюдается трансформация продуцируемого яичниками тестостерона в дигидротестостерон (ДГТ) – стероидный гормон, стимулирующий выработку кожного сала и рост стержневых волос на теле, а в редких случаях – потерю волос на голове.
Компенсаторная гиперпродукция инсулина стимулирует выработку клеток яичников, продуцирующих андрогены. Транспортная гиперандрогения наблюдается при нехватке глобулина, связывающего свободную фракцию тестостерона, что характерно для синдрома Иценко – Кушинга, дислипопротеидемии и гипотиреоза. При высокой плотности андрогенных рецепторов клеток тканей яичников, кожи, волосяных фолликулов, сальных и потовых желез симптомы гиперандрогении могут наблюдаться при нормальном уровне половых стероидов в крови.
Степень выраженности симптомов зависит от причины и формы эндокринопатии, сопутствующих заболеваний и индивидуальных особенностей.
Вероятность манифестации патологических состояний, ассоциированных с симптомокомплексом гиперандрогении, зависит от ряда факторов:
- наследственная и конституциональная предрасположенность;
- хронические воспалительные заболевания яичников и придатков;
- выкидыши и аборты, особенно в ранней молодости;
- нарушения обмена веществ;
- избыточная масса тела;
- вредные привычки – курение, злоупотребление алкоголем и наркотиками;
- дистресс;
- длительный прием лекарств, содержащих стероидные гормоны.
Идиопатическая гиперандрогения является врожденной или возникает в детстве либо в пубертатном периоде без видимых причин.
Виды
В гинекологической практике выделяют несколько типов гиперандрогенных состояний, которые отличаются друг от друга по этиологии, течению и симптоматике. Эндокринная патология может быть как врожденной, так и приобретенной. Первичная гиперандрогения, не связанная с другими заболеваниями и функциональными расстройствами, обусловлена нарушениями гипофизарной регуляции; вторичная выступает следствием сопутствующих патологий.
Исходя из специфики манифестации, различают абсолютную и относительную разновидности гиперандрогении. Абсолютная форма характеризуется повышением уровня мужских гормонов в сыворотке крови женщины и, в зависимости от источника гиперсекреции андрогенов, подразделяются на три категории:
- овариальная, или яичниковая;
- адреналовая, или надпочечниковая;
- смешанная – одновременно присутствуют признаки яичниковой и надпочечниковой форм.
Относительная гиперандрогения протекает на фоне нормального содержания мужских гормонов при избыточной чувствительности тканей-мишеней к половым стероидам или усиленной трансформации последних в метаболически активные формы. В отдельную категорию выделяют ятрогенные гиперандрогенные состояния, развившиеся в результате продолжительного приема гормональных препаратов.
Быстрое развитие признаков вирилизации у взрослой женщины дает основание заподозрить андроген-продуцирующую опухоль яичника или надпочечника.
Симптомы гиперандрогении
Клиническая картина гиперандрогенных состояний характеризуется большим многообразием проявлений, которые укладываются в стандартный комплекс симптомов:
- расстройства менструальной функции;
- нарушения обмена веществ;
- андрогенная дермопатия;
- бесплодие и невынашивание беременности.
Степень выраженности симптомов зависит от причины и формы эндокринопатии, сопутствующих заболеваний и индивидуальных особенностей. К примеру, дисменорея проявляется особенно ярко при гиперандрогении овариального генеза, которая сопровождается аномалиями развития фолликулов, гиперплазией и неравномерным отслоением эндометрия, кистозными изменениями в яичниках. Пациентки жалуются на скудные и болезненные менструации, нерегулярные или ановуляторные циклы, маточные кровотечения и предменструальный синдром. При синдроме галактореи-аменореи отмечается дефицит прогестерона.
Выраженные метаболические расстройства – дислипопротеидемия, инсулинорезистентность и гипотиреоз характерны для первичной гипофизарной и надпочечниковой форм гиперандрогении. Примерно в 40% случаях у пациенток обнаруживают абдоминальное ожирение по мужскому типу или с равномерным распределением жировой ткани. При адреногенитальном синдроме наблюдается промежуточное строение гениталий, а в самых тяжелых случаях – псевдогермафродитизм. Вторичные половые признаки выражены слабо: у взрослых женщин отмечается недоразвитие груди, понижение тембра голоса, увеличение мышечной массы и оволосение тела; для девочек характерно позднее менархе. Быстрое развитие признаков вирилизации у взрослой женщины дает основание заподозрить андроген-продуцирующую опухоль яичника или надпочечника.
Андрогенная дермопатия обычно связана с повышенной активностью дигидротестостерона. Воздействие гормона, стимулирующего секреторную активность кожных желез, изменяет физико-химические свойства кожного сала, провоцируя закупорку выводных протоков и воспаление сальных желез. В результате у 70–85% пациенток с гиперандрогенией присутствуют признаки акне – угревая сыпь, расширение кожных пор и комедоны.
Гиперандрогенные состояния – одна из самых распространенных причин женского бесплодия и невынашивания беременности.
Реже встречаются другие проявления андрогенной дерматопатии – себорея и гирсутизм. В отличие от гипертрихоза, при котором наблюдается избыточный рост волос по всему телу, гирсутизм характеризуется превращением пушковых волос в жесткие терминальные волосы в андрогеночувствительных зонах – над верхней губой, на шее и подбородке, на спине и груди вокруг соска, на предплечьях, голенях и внутренней стороне бедра. У женщин в период постменопаузы изредка отмечается битемпоральная и париетальная алопеция – выпадение волос на висках и в области темени соответственно.
Особенности протекания гиперандрогении у детей
В допубертатном периоде у девочек могут проявиться врожденные формы гиперандрогении, обусловленные генетическими аномалиями или воздействием андрогенов на плод во время беременности. Гипофизарную гиперандрогению и врожденную гиперплазию надпочечников распознают по выраженной вирилизации девочки и аномалиями строения гениталий. При адреногенитальном синдроме могут присутствовать признаки ложного гермафродитизма: гипертрофия клитора, сращение больших половых губ и вагинального отверстия, смещение уретры к клитору и уретрогенитальный синус. Одновременно отмечаются:
- раннее зарастание родничков и эпифизарных щелей в младенчестве;
- преждевременное оволосение тела;
- быстрый соматический рост;
- замедленное половое созревание;
- позднее менархе или отсутствие менструаций.
Врожденная гиперплазия надпочечников сопровождается нарушениями водно-солевого баланса, гиперпигментацией кожи, гипотонией и вегетативными расстройствами. Начиная со второй недели жизни, при врожденной гиперплазии надпочечников и тяжелом течении адреногенитальном синдрома возможно развитие адреналового криза – острой надпочечниковой недостаточности, сопряженной с угрозой для жизни. Родителей должны насторожить резкое падение артериального давления до критической отметки, рвота, диарея и тахикардия у ребенка. В подростковом возрасте адреналовый криз могут спровоцировать нервные потрясения.
Умеренную гиперандрогению в подростковом возрасте, ассоциированную с резким ростовым скачком, следует дифференцировать с врожденным поликистозом яичников. Дебют СПКЯ зачастую происходит на этапе становления менструальной функции.
Врожденная гиперандрогения надпочечникового генеза у детей и девочек-подростков может внезапно осложниться адреналовым кризом.
Диагностика
Заподозрить гиперандрогению у женщины можно по характерным изменениям внешности и на основании данных анамнеза. Для подтверждения диагноза, определения формы и выявления причины гиперандрогенного состояния проводится анализ крови на андрогены – общий, свободный и биологически доступный тестостерон, дигидротестостерон, дегидроэпиандростерон-сульфат (ДЭА-сульфат), а также глобулин, связывающий половые гормоны (ГСПГ).
В норме содержание свободного тестостерона в сыворотке крови половозрелых женщин до 50 лет колеблется от 0,001 до 0,0034 нмоль/литр, биологически доступного тестостерона – от 0,033 до 0,774 нмоль/литр. Для женщин старшего возраста показатели составляют 0,001–0,022 и 0,002–0,46 нмоль/литр соответственно. Повышенное содержание тестостерона свидетельствует о яичниковом происхождении гиперандрогении; увеличение концентрации ДЭА-сульфата – о гиперандрогении надпочечникового генеза. Экстремально высокий уровень тестостерона и ДЭА-сульфата может свидетельствовать о вирилизующей опухоли.
В целях выявления патологии яичников, вызвавшей овариальную гиперандрогению, назначают УЗИ органов малого таза и дополнительные лабораторные исследования гормонального фона с определением уровня эстрадиола, пролактина, лютеинизирующего и фолликулостимулирующего гормонов.
При гиперандрогенных состояниях адреналовой, гипофизарной и транспортной этиологии женщину направляют на МРТ или КТ гипофиза и надпочечников. По показаниям выполняют анализы крови на 17-оксипрогестерон и мочи на кортизол и 17-кетостероиды. Для диагностики обменных патологий применяются лабораторные исследования:
- пробы с дексаметазоном и хорионическим гонадотропином человека;
- определение уровня холестерина и липопротеидов;
- анализы крови на сахар и гликированный гликоген, тест на толерантность к глюкозе;
- пробы с адренокортикотропным гормоном.
Для улучшения визуализации железистой ткани при подозрении на новообразование показана МРТ или КТ с применением контрастных веществ.
Лечение гиперандрогении
Коррекция гиперандрогении дает стойкий результат только в рамках терапии основных заболеваний, таких как СПКЯ или синдром Иценко – Кушинга, и сопутствующих патологий – гипотиреоза, инсулинорезистентности, гиперпролактинемии и др.
Гиперандрогенные состояния яичникового генеза корректируют при помощи эстроген-гестагенных оральных контрацептивов, подавляющих секрецию овариальных гормонов и блокирующих андрогеновые рецепторы. При сильной андрогенной дермопатии выполняют периферическую блокаду рецепторов кожи, сальных желез и волосяных фолликулов.
В случае надпочечниковой гиперандрогении применяют кортикостероиды; при развитии метаболического синдрома дополнительно назначают инсулиновые синтетайзеры в сочетании с низкокалорийной диетой и дозированными физическими нагрузками. Андроген-секретирующие новообразования, как правило, имеют доброкачественную природу и не рецидивируют после удаления хирургическим путем.
Для женщин, планирующих беременность, лечение гиперандрогении служит обязательным условием восстановления репродуктивной функции.
Профилактика
Для предотвращения гиперандрогенных состояний женщинам и девушкам-подросткам рекомендуются профилактические осмотры гинеколога и скрининговые тесты для контроля андрогенного статуса. Раннее выявление и лечение гинекологических заболеваний, своевременная коррекция гормонального фона и грамотный подбор контрацептивов успешно профилактируют гиперандрогению и способствуют поддержанию репродуктивной функции.
При склонности к гиперандрогении и врожденных адренопатиях важно придерживаться здорового образа жизни и щадящего режима труда и отдыха, отказаться от вредных привычек, ограничить влияние стресса, вести упорядоченную половую жизнь, избегать абортов и средств экстренной контрацепции; категорически запрещен бесконтрольный прием гормональных препаратов и анаболических препаратов. Немаловажное значение имеет контроль массы тела; предпочтительна умеренная двигательная активность без тяжелых физических нагрузок.
Чаще всего гиперандрогения у женщин впервые диагностируется в репродуктивном возрасте – от 25 до 45 лет; реже – у девочек в подростковом периоде.
Последствия и осложнения
Гиперандрогенные состояния – одна из самых распространенных причин женского бесплодия и невынашивания беременности. Длительное течение гиперандрогении повышает риск развития метаболического синдрома и сахарного диабета II типа, атеросклероза, артериальной гипертензии и ишемической болезни сердца. По некоторым данным, высокая активность андрогенов коррелирует с заболеваемостью некоторыми формами рака груди и раком шейки матки у женщин, инфицированных онкогенными папилломавирусами. Кроме того, эстетический дискомфорт при андрогенной дермопатии оказывает на пациенток сильное психотравмирующее воздействие.
Врожденная гиперандрогения надпочечникового генеза у детей и девочек-подростков может внезапно осложниться адреналовым кризом. В силу возможности летального исхода при первых признаках острой надпочечниковой недостаточности следует немедленно доставить ребенка в больницу.
Гиперандрогения у женщин - состояние, при котором в крови определяется повышенный уровень андрогенов, а также фиксируются клинические данные избытка мужских половых гормонов.
Встречается у разных возрастных групп. Основными причинами гиперандрогении являются адреногенитальный синдром (АГС) и поликистоз яичников (СПКЯ). Лечение гиперандрогении направлено на коррекцию гормонального фона и профилактику последствий избытка андрогенов. В норме гормональный статус женщины допускает определенный уровень андрогенов в крови. Из них под действием ароматазы образуется часть эстрогенов.
Избыточное же количество приводит к нарушению репродуктивной функции, повышается риск онкологических заболеваний. В МКБ-10 нет классификации данного синдрома, так как он не является болезнью.
Что это такое?
Гиперандрогения у женщин – понятие, объединяющее патогенетически разнородные синдромы, обусловленные повышенной продукцией андрогенов эндокринной системой или чрезмерной восприимчивостью к ним тканей–мишеней. Значимость гиперандрогении в структуре гинекологической патологии объясняется ее широким распространением среди женщин детородного возраста (4–7,5% у девочек-подростков, 10-20% у пациенток старше 25 лет).
Причины возникновения
Гиперандрогения – проявление широкого спектра синдромов. Специалисты называют три наиболее вероятные причины гиперандрогении:
- повышение уровня андрогенов в сыворотке крови;
- превращение андрогенов в метаболически активные формы;
- активная утилизация андрогенов в тканях-мишенях вследствие аномальной чувствительности андрогенных рецепторов.
Чрезмерный синтез мужских половых гормонов, как правило, связан с нарушением функции яичников. Чаще всего встречается синдром поликистозных яичников (СПКЯ) – образование множественных мелких кист на фоне комплекса эндокринных расстройств, включая патологии щитовидной и поджелудочной железы, гипофиза, гипоталамуса и надпочечников. Заболеваемость СПКЯ среди женщин фертильного возраста достигает 5–10%.
Гиперсекреция андрогенов также наблюдается при следующих эндокринопатиях:
- адреногенитальный синдром;
- врожденная гиперплазия надпочечников;
- синдром галактореи-аменореи;
- стромальный текоматоз и гипертекоз;
- вирилизирующие опухоли яичников и надпочечников, продуцирующие мужские гормоны.
Гиперандрогения на почве трансформации половых стероидов в метаболически активные формы часто вызывается разнообразными нарушениями липидно-углеводного обмена, сопровождающихся инсулинорезистентностью и ожирением. Чаще всего наблюдается трансформация продуцируемого яичниками тестостерона в дигидротестостерон (ДГТ) – стероидный гормон, стимулирующий выработку кожного сала и рост стержневых волос на теле, а в редких случаях – потерю волос на голове.
Компенсаторная гиперпродукция инсулина стимулирует выработку клеток яичников, продуцирующих андрогены. Транспортная гиперандрогения наблюдается при нехватке глобулина, связывающего свободную фракцию тестостерона, что характерно для синдрома Иценко – Кушинга, дислипопротеидемии и гипотиреоза. При высокой плотности андрогенных рецепторов клеток тканей яичников, кожи, волосяных фолликулов, сальных и потовых желез симптомы гиперандрогении могут наблюдаться при нормальном уровне половых стероидов в крови.
Степень выраженности симптомов зависит от причины и формы эндокринопатии, сопутствующих заболеваний и индивидуальных особенностей.
Вероятность манифестации патологических состояний, ассоциированных с симптомокомплексом гиперандрогении, зависит от ряда факторов:
- наследственная и конституциональная предрасположенность;
- хронические воспалительные заболевания яичников и придатков;
- выкидыши и аборты, особенно в ранней молодости;
- нарушения обмена веществ;
- избыточная масса тела;
- вредные привычки – курение, злоупотребление алкоголем и наркотиками;
- дистресс;
- длительный прием лекарств, содержащих стероидные гормоны.
Идиопатическая гиперандрогения является врожденной или возникает в детстве либо в пубертатном периоде без видимых причин.
Классификация
В зависимости от причины, уровня и механизма развития патологии выделяют следующие виды гиперандрогении.
- Яичниковая. Характеризуется нарушениями генетического или приобретенного происхождения. Для овариальной гиперандрогении свойственно стремительное развитие и внезапное появление симптомов. В яичниках происходит превращение андрогенов в эстрогены под действием фермента ароматазы. При нарушении его работы возникает дефицит женских половых гормонов и избыток мужских. Помимо этого, гиперандрогению яичникового генеза могут провоцировать гормонально-активные опухоли данной локализации.
- Надпочечниковая. Такую гиперандрогению вызывают опухоли надпочечников (чаще всего андростеромы) и адреногенитальный синдром. Последняя патология обусловлена генетическими аномалиями гена, который отвечает за образование фермента С21-гидроксилаза. Недостаток этого вещества на протяжении длительного времени может восполняться работой других гормонопродуцирующих органов, поэтому состояние имеет скрытое течение. При психоэмоциональном перенапряжении, беременности и других стрессовых факторах дефицит фермента не покрывается, поэтому клиника АГС становится более явной. Надпочечниковая гиперандрогения характеризуется дисфункцией яичников и нарушением менструального цикла, отсутствием овуляции, аменореей, недостаточностью желтого тела при созревании яйцеклетки.
- Смешанная . Тяжелая форма гиперандрогении, сочетает в себе дисфункцию яичников и надпочечников. Пусковым механизмом развития смешанной гиперандрогении являются нейроэндокринные расстройства, патологические процессы в области гипоталамуса. Проявляется нарушениями жирового обмена, часто бесплодием или невынашиванием.
- Центральная и периферическая . Связана с дисфункцией гипофиза и гипоталамуса, нарушением работы нервной системы. Возникает дефицит фолликулостимулирующего гормона, что нарушает созревание фолликулов. Как итог - повышается уровень андрогенов.
- Транспортная. Эта форма гиперандрогении основана на дефиците глобулина, отвечающего за связывание половых стероидов в крови, а также блокирующего чрезмерную активность тестостерона.
По очагу зарождения патологии выделяют следующие виды гиперандрогении:
- первичная - берет начало в яичниках и надпочечниках;
- вторичная - очаг зарождения в гипофизе.
По способу развития патологии выделяются:
- наследственная;
- приобретенная.
По степени концентрации мужских гормонов гиперандрогения бывает:
- относительная - уровень андрогенов в норме, но сенситивность к ним органов-мишеней увеличена, и мужские половые гормоны имеют склонность к превращению в активные формы;
- абсолютная - допустимая норма содержания андрогенов превышена.

Симптомы
Симптомы гиперандрогении у женщин могут варьировать от незначительных (избыточный рост волос на теле) до тяжелых (развитие вторичных мужских половых признаков).
Главными проявлениями патологических нарушений являются:
- акне – возникает при повышенной жирности кожи, которая приводит к закупорке и воспалениям сальных желез;
- себорея волосистой кожи головы;
- гирсутизм – появление сильного оволосения в местах нетипичных для женщин (лице, груди, животе, ягодицах);
- истончение и выпадение волос на голове, появление залысин;
- усиленный рост мышц, формирование мускулатуры по мужскому типу;
- огрубление тембра голоса;
- нарушение менструального цикла, скудость выделений, иногда полное прекращение менструаций;
- повышенное половое влечение.
Происходящие сбои в гормональном балансе становятся причиной развития сахарного диабета, появления лишнего веса, нарушений липидного обмена. Женщины становятся очень восприимчивы к различным инфекционным заболеваниям. У них нередко развиваются депрессии, хроническая усталость, повышенная раздражительность и общая слабость.
Одним из наиболее тяжелых последствий гиперандрогении является вирилизация или вирильный синдром. Так называют патологию развития женского организма, при которой он приобретает ярко выраженные мужские признаки. Вирилизация относится к редким отклонениям, ее диагностируют только у одной пациентки из 100, у которых отмечают чрезмерный рост волос на теле.
У женщины формируется мужская фигура с усиленным ростом мышц, полностью прекращаются месячные, значительно увеличивается размеры клитора. Очень часто подобные признаки развиваются у женщин, которые бесконтрольно принимают стероиды для повышения выносливости и физической силы при занятиях спортом.
Гиперандрогения при беременности
Среди всех возможных причин развития самопроизвольного аборта у беременной женщины в первом триместре, гиперандрогения занимает лидирующую позицию. К сожалению, во время обнаружения признаков гиперандрогении у женщины в период уже имеющейся беременности крайне затруднительно определить, врожденный или приобретенный характер имеет данная патология. В этом периоде определение генеза заболевания не имеет столь большого значения, так как первоочередно необходимо осуществлять все мероприятия по сохранению беременности.
Фенотипические признаки гиперандрогении у беременной женщины ничем не отличаются от проявлений данного патологического состояния у любой другой представительницы женского пола, с той лишь разницей, что в некоторых ситуациях гиперандрогения проявляется в виде прерывания беременности на раннем сроке, что не всегда расценивается женщиной как выкидыш. Развитие самопроизвольного выкидыша на раннем сроке обусловлено недостаточным прикреплением плодного яйца к стенке матки и отторжением его даже при малейшем травматическом влиянии. Ярким клиническим проявлением данного состояния является обнаружение влагалищного кровотечения, которое кстати, может быть не столь интенсивным, тянущей боли в надлобковой области и нивелирование признаков раннего токсикоза.
После 14 недели беременности создаются физиологические условия для предотвращения факта прерывания беременности, так как в этом периоде отмечается повышение активности женских половых гормонов, секретируемых плацентой в большом количестве.
Еще одним критическим периодом возникновения угрозы прерывания беременности у женщины, страдающей гиперандрогенией, является 20 неделя беременности, когда происходит активный выброс дегидроэпиандростерона надпочечниками плода, что неизбежно провоцирует усиление андрогенизации беременной женщины. Осложнением данных патологических изменений является развитие признаков истмико-цервикальной недостаточности, которая может провоцировать наступление преждевременного родоразрешения. В третьем триместре беременности гиперандрогения является провокатором раннего излития околоплодных вод, вследствие чего женщина может родить раньше положенного срока.
Для определения гиперандрогении у беременной женщины целесообразно применять лишь лабораторные методы диагностики, принципиально отличающиеся от обследования остальной категории пациенток. С целью определения концентрации мужских половых гормонов необходимо исследовать мочу беременной женщины с определением «суммы 17- кетостероидов».
Следует учитывать, что не все случаи выявления признаков гиперандрогении у беременной женщины должны подвергаться медикаментозной коррекции, даже при условии подтверждения диагноза лабораторными методиками. Медикаментозные методы терапии применяются только в случае имеющейся угрозы вынашиванию плода. Препаратом выбора для лечения гиперандрогении при беременности является Дексаметазон, начальная суточная доза которого составляет ¼ таблетки, действие которого направлено на ингибирование функции гипофиза, оказывающего опосредованное влияние на продукцию мужских половых гормонов. Применение данного препарата оправдано полным отсутствием негативного влияния на развитие плода с одновременным положительным эффектом в отношении нивелирования признаков гиперандрогении.
В послеродовом периоде, женщины, страдающие гиперандрогенией, обязательно должны находиться под наблюдением не только гинеколога, но и эндокринолога, так как данное патологическое состояние склонно прогрессировать и провоцировать серьезные осложнения.
Осложнения
Спектр возможно осложнений при всех описанных выше заболеваниях крайне велик. Можно отметить только некоторые, самые важные:
- При врожденной патологии возможны аномалии развития, самые распространенные из них — аномалии развития половых органов.
- Метастазирования злокачественных опухолей – осложнение, более характерное для опухолей надпочечников.
- Осложнения со стороны других систем органов, которые подвергаются негативному влиянию изменения гормонального фона при патологии надпочечников, гипофиза и яичников: хроническая почечная недостаточность, патология щитовидной железы и т.д.
Этим простым перечислением список далеко не окончен, что говорит в пользу своевременного обращения к врачу, дабы предвосхитить их наступление. Только своевременная диагностика и квалифицированное лечение способствуют достижению положительных результатов.
Диагностика
В диагностике гиперандрогении имеют значение как жалобы, анамнез и данные объективного статуса пациента, так и лабораторные и инструментальные методы исследования. То есть после оценивания симптомов и данных анамнеза необходимо не только выявить факт повышения уровня тестостерона и других мужских половых гормонов в крови, но и обнаружить их источник – новообразование, синдром поликистозных яичников или иную патологию.
Половые гормоны исследуют на 5-7 день менструального цикла. Определяют уровень в крови общего тестостерона, ГСПГ, ДГЭА, фолликулостимулирующего, лютеинизирующего гормонов, а также 17-гидроксипрогестерона.
Чтобы обнаружить источник проблемы, проводят УЗИ органов малого таза (при подозрении на патологию яичников – с использованием трансвагинального датчика) либо, если есть возможность, магнитно-резонансную томографию данной области.
С целью диагностики опухоли надпочечников больному назначают компьютерную, магнитно-резонансную томографию или сцинтиграфию с радиоактивным йодом. Стоит отметить, что опухоли малого размера (менее 1 см в диаметре) во многих случаях диагностировать не удается.
Если результаты вышеперечисленных исследований отрицательные, пациенту может быть назначена катетеризация вен, уносящих кровь от надпочечников и яичников, с целью определения уровня андрогенов в крови, оттекающей непосредственно от этих органов.
Лечение гиперандрогении у женщин
Основной метод лечения гиперандрогении у женщин – прием эстроген-гестагенных оральных контрацептивов с антиандрогенным эффектом, например, Диане 35. Препараты замедляют синтез гонадотропинов, подавляют секрецию овариальных гормонов и нормализуют менструальный цикл. Иногда обходятся и гестагенными средствами, такими как Утрожестан.
Другие принципы лечения:
- Если женщине противопоказаны оральные контрацептивы, то их заменяют Спиронолактоном или Верошпироном. Они используются при тяжелом предменструальном синдроме и поликистозе яичников для блокады внутриклеточного рецептора дигидротестостерона и подавления синтеза тестостерона.
- Андрогенизация у женщин при адреногенитальном синдроме лечится при помощи глюкокортикоидов, таких как Дексаметазон и Преднизолон.
- В случае гипотиреоза или высокого уровня пролактина корректируют непосредственно концентрацию этих веществ. Количество андрогенов в таком случае нормализуется само.
- При гиперинсулизме и ожирении принимают сахароснижающий препарат Метформин, соблюдают диету и занимаются спортом.
- Доброкачественные новообразования яичников или надпочечников – показание к хирургическому вмешательству.
- Чтобы нормализовать менструальный цикл, часто используют Дюфастон. Его принимают даже после наступления беременности, чтобы снизить риск выкидыша.
- Устранить артериальную гипертензию помогают блокаторы ренин-ангиотензина (Вальсартан) и ингибиторы АПФ (Рамиприл, Периндоприл).
На схему терапии влияет и форма гиперандрогении. Пациенту может требоваться помощь по борьбе с гирсутизмом, нарушением репродуктивной функции или полным бесплодием. Целью лечения у беременных женщин, если есть угроза выкидыша, является сохранение беременности.

Профилактика
Гиперандрогения не имеет специфических мер профилактики.
К основным можно отнести соблюдение режима правильного питания и образа жизни. Каждой женщине необходимо помнить, что чрезмерное похудание способствует гормональным нарушениям и может приводить как к описанному состоянию, так и ко многим другим. Кроме того, не следует увлекаться занятиями спортом, что тоже (особенно при приеме стероидных препаратов) может приводить к гиперандрогении.
Реабилитацию требуют пациенты с гиперандрогенией опухолевого генеза, подвергшиеся оперативному и химиотерапевтическому лечению. Кроме того, обязательно консультация с психологом, особенно для молодых девушек с выраженным гирсутизмом и гинекологическими проблемами.
Для цитирования:
Пищулин А.А., Карпова Е.А. Овариальная гиперандрогения и метаболический синдром // РМЖ. 2001. №2. С. 93
Эндокринологический научный центр РАМН, Москва
С индром овариальной гиперандрогении неопухолевого генеза или гиперандрогенная дисфункция яичников, называемый ранее синдромом Штейна - Левенталя, в настоящее время, согласно классификации ВОЗ, больше известен в мировой литературе, как синдром поликистозных яичников (СПЯ).
Клиническая картина СПЯ проявляется хроническим ановуляторным состоянием яичников или выраженной гипофункцией желтого тела, что приводит к двустороннему увеличению размеров яичников с утолщением и склерозом белочной оболочки. Эти изменения проявляются нарушением менструальной функции - опсоменореей, аменореей, однако не исключается и развитие метроррагии. Нарушения фолликулогенеза приводят к развитию ановуляторного первичного или вторичного бесплодия.
Одним из основных диагностических критериев СПЯ является гиперандрогенемия - повышение уровня андрогенных стероидов в крови (таких как тестостерон, андростендион), что приводит к развитию гирсутизма и других андрогензависимых дермопатий.
Ожирение или избыточная масса тела часто сопутствуют СПЯ. Определение индекса массы тела (ИМТ) позволяет выявить степень ожирения. Измерение показателей объема талии (ОТ) и бедер (ОБ) и их соотношение указывает на тип ожирения (прогностически неблагоприятным является абдоминальный тип ожирения, при котором ОТ/ОБ > 0,85).
Кроме основных симптомов заболевания, клиническая картина во многом определяется общими обменными нарушениями, такими как дислипидемия, нарушение углеводного обмена, повышенным риском развития гиперпластических и опухолевых процессов со стороны гениталий. Дислипидемия заключается в повышении уровня триглицеридов, холестерина, липопротеидов низкой плотности, липопротеидов очень низкой плотности и снижении липопротеидов высокой плотности. Эти нарушения ведут к риску раннего развития атеросклеротических изменений сосудов, гипертонической болезни и ишемической болезни сердца.
Нарушения углеводного обмена заключаются в развитии комплекса инсулинорезистентность-гиперинсулинемия, что в последнее время является основным направлением в изучении патогенетических звеньев развития СПЯ.
В 60-х годах патогенез СПЯ связывали с первичным ферментативным дефектом овариальной 19-гидроксилазы и/или 3b-дегидрогеназы, объединяя эти нарушения в понятие первичного поликистоза яичников. Однако в работах последующих лет было показано, что ароматазная активность клеток гранулезы является ФСГ зависимой функцией.
Выявленный при СПЯ повышенный уровень лютенизирующего гормона (ЛГ), отсутствие его овуляторного пика, нормальный или сниженный уровень фолликулостимулирующего гормона (ФСГ) при нарушенном соотношении ЛГ/ФСГ (2,5-3) предполагал первичное нарушение гонадотропной регуляции стероидогенеза в овариальной ткани с развитием вторичного поликистоза яичников.
До середины 80-х годов считалось (теория S.S.C. Yen) , что пусковым механизмом в патогенезе СПЯ является избыточный синтез андрогенов надпочечниками в период адренархе в результате измененной чувствительности надпочечников к АКТГ или чрезмерной стимуляции сетчатой зоны коры надпочечников не АКТГ-подобным фактором или под влиянием b-эндорфинов , нейротрансмиттеров, например, дофамина . При достижении критической массы тела (особенно при превышении ее нормы) увеличивается периферическая конверсия андрогенов в эстрогены, прежде всего в печени и жировой ткани . Повышение уровня эстрогенов, в первую очередь эстрона, приводит к гиперсенсибилизации гонадотрофов по отношению к люлиберину (ГнРГ). Одновременно под действием эстрона увеличивается продукция гипоталамусом ГнРГ, повышается амплитуда и частота импульсов его секреции, в результате чего увеличивается продукция аденогипофизом ЛГ, нарушается соотношение ЛГ/ФСГ, возникает относительная недостаточность ФСГ . Усиление влияния ЛГ на яичники способствует повышению продукции андрогенов текальными клетками и их гиперплазии. Относительно низкий уровень ФСГ приводит к снижению активности ФСГ-зависимой ароматазы, и клетки гранулезы теряют способность ароматазировать андрогены в эстрогены. Гиперандрогения препятствует нормальному росту фолликулов и способствует формированию их кистозной атрезии. Отсутствие роста и созревания фолликулов еще более ингибирует секрецию ФСГ. Возросший пул андрогенов в периферических тканях конвертируется в эстрон. Замыкается порочный круг.
Таким образом результатом нарушения центральных и периферических механизмов регуляции стероидогенеза является развитие у больных с СПЯ функциональной овариальной гиперандрогении.
Патогенез СПЯ по S.S.C. Yen представлен на схеме 1:
Схема 1.
В начале 80-х годов ряд авторов предложили новую теорию патогенеза синдрома поликистозных яичников, отличную от теории S.S.C. Yen . Было обнаружено, что СПЯ связан с гиперинсулинемией, и этому синдрому свойственны как нарушение репродуктивной функции, так и метаболических процессов.
На наличие взаимосвязи между гиперинсулинемией и гиперандрогенией указывали еще в 1921 году Achard and Thieris . Они описали гиперандрогению у женщины, страдавшей ожирением и сахарным диабетом 2-го типа и назвали это состояние “диабет бородатых женщин”.
В дальнейшем Д. Барген обнаружил, что у женщин с СПЯ и гиперандрогенией отмечалась базальная и глюкозостимулированная гиперинсулинемия по сравнению с контрольной группой женщин одинакового веса, что предполагало наличие инсулинорезистентности. Выявилась прямая зависимость между уровнями инсулина и андрогенов, и было высказано предположение, что причиной гиперандрогении может быть гиперинсулинемия.
В 1988 году G. Reaven впервые высказал предположение о том, что ИР и компенсаторная гиперинсулинемия (ГИ) играют основную роль в развитии синдрома метаболических нарушений. Он назвал его “синдромом Х” . В настоящее время наиболее часто употребляют термин “метаболический синдром” или “синдром инсулинорезистентности” .
Гипотезы патогенеза гиперинсулинемии и гиперандрогении
Механизм возникновения гиперандрогении и гиперинсулинемии окончательно не изучен. Теоретически возможны три варианта взаимодействия: гиперандрогения (ГА) вызывает ГИ; ГИ приводит к ГА: имеется какой-то третий фактор, ответственный за оба феномена .
1. Предположение о том, что ГА вызывает ГИ основано на следующих фактах. У женщин, которые принимают оральные контрацептивы, содержащие прогестины с “андрогенными свойствами”, выявляется нарушение толерантности к глюкозе. Длительное назначение тестостерона транссексуалам сопровождается возникновением ИР . Показано, что андрогены влияют на состав мышечной ткани, увеличивая количество мышечных волокон второго типа, менее чувствительных к инсулину по сравнению с волокнами первого типа .
2. Большинство факторов свидетельствуют в пользу того, что ГИ приводит к ГА. Было показано, что ИР сохраняется у пациенток, подвергшихся субтотальному или тотальному удалению яичников, а также у женщин, длительно применявших агонисты-ГнРГ, когда отмечалась выраженная супрессия уровня андрогенов . Назначение диазоксида - препарата, подавляющего выделение инсулина поджелудочной железой, вызвало снижение уровня тестостерона (Т) и повышение уровня сексстероидсвязывающего глобулина (СССГ) у пациенток с СПЯ, ожирением и гиперинсулинемией. Внутривенное введение инсулина женщинам с СПЯ приводило к повышению уровня циркулирующих андростендиона и Т. Мероприятия, направленные на повышение чувствительности к инсулину (снижение веса, голодание и низкокалорийная диета), сопровождались понижением уровня андрогенов . Есть данные, что инсулин напрямую может подавлять продукцию СССГ печенью, а в условиях гиперинсулинемии этот эффект усиливается. При этом полагают, что инсулин, а не половые гормоны, является основным регулятором синтеза СССГ. Понижение уровня СССГ приводит к возрастанию концентрации свободного и, следовательно, биологически активного Т (в норме 98% Т находится в связанном состоянии) .
Гипотеза, связывающая ГА с гиперинсулинемией, не дает ответа на вопрос, каким образом яичник сохраняет чувствительность к инсулину при инсулинорезистентном состоянии организма. Было предложено несколько возможных объяснений. Так как инсулин обладает множеством функций, можно предположить селективный дефект некоторых из них. Может наблюдаться органоспецифичность чувствительности к инсулину. Но более вероятно предположение о том, что инсулин действует на яичник не только через рецепторы инсулина, но также через рецепторы инсулиноподобных факторов роста (ИФР) .
Инсулиновые рецепторы и рецепторы ИФР-1 были идентифицированы в яичниках человека (в стромальной ткани яичников здоровых женщин, женщин с СПЯ, в фолликулярной ткани и клетках гранулезы) . Инсулин может связываться с рецепторами ИФР-1, хотя с меньшим сродством, чем с собственными рецепторами. Однако при ГИ, а также в ситуации, когда рецепторы инсулина блокированы или имеется их дефицит, можно ожидать, что инсулин будет связываться с рецепторами ИФР-1 в большей степени .
Возможно, механизмы стимуляции инсулином/ИФР-1 стероидогенеза в яичнике могут быть разделены на неспецифические и специфические. Неспецифические заключаются в классическом действии инсулина на метаболизм глюкозы, аминокислот и синтез ДНК. В результате повышается жизнеспособность клетки и, следовательно, усиливается синтез гормонов . Специфические механизмы включают прямое действие инсулина/ИФР-1 на стероидогенные ферменты, синергизм между инсулином и ЛГ/ФСГ и влияние на количество рецепторов к ЛГ .
Инсулин/ИФР-1, действуя синергично с ФСГ, стимулируют ароматазную активность в культуре клеток гранулезы и тем самым увеличивают синтез эстрадиола. Кроме того, они приводят к повышению концентрации рецепторов ЛГ, усиливая ЛГ-зависимый синтез андростендиона тека- и стромальными клетками.
Возрастающая концентрация андрогенов в яичнике под действием инсулина/ИФР-1 вызывает атрезию фолликулов, что приводит к постепенной элиминации эстроген- и прогестеронпродуцирующих клеток гранулезы, с последующей гиперплазией текальных клеток и лютеинизацией межуточной ткани яичника, которые являются местом продукции андрогенов. Этим объясняется тот факт, что стимуляция яичникового стероидогенеза инсулином проявляется преимущественно в виде гиперандрогении.
Было высказано предположение, что инсулин/ИФР-1 могут стимулировать как ЛГ-зависимую активность цитохрома Р450с17a в яичниках, так и АКТГ-зависимую активность Р450с17a в надпочечниках. Этим, по-видимому, объясняется частое сочетание яичниковой и надпочечниковой форм гиперандрогении у пациенток с СПЯ.
Возможна также взаимосвязь с теорией S.S.C. Yen об участии надпочечникового стероидогенеза в патогенезе СПЯ (схема 2).

Схема 2. Действие инсулина при синдроме поликистозных яичников
V. Insler (1993), проведя исследование уровней инсулина, ИФР-1, гормона роста и их корреляции с уровнями гонадотропинов и андрогенов у женщин с СПЯ, предложил две модели развития данного синдрома. У пациенток с ожирением ГИ вызывает избыточную продукцию андрогенов через рецепторы ИФР-1, которые, действуя в синергизме с ЛГ, вызывают повышение активности цитохрома Р450с17a, основного контролирующего фермента в синтезе андрогенов. У пациенток с нормальной массой тела относительное повышение концентрации гормона роста стимулирует избыточную продукцию ИФР-1. С этого момента синергизм с ЛГ приводит к гиперпродукции андрогенов по тому механизму, что и у пациенток с ожирением. Повышение уровня андрогенов вызывает изменение функции гипоталамических центров, приводя к нарушению секреции гонадотропинов и типичным для СПЯ изменениям (схема 3).
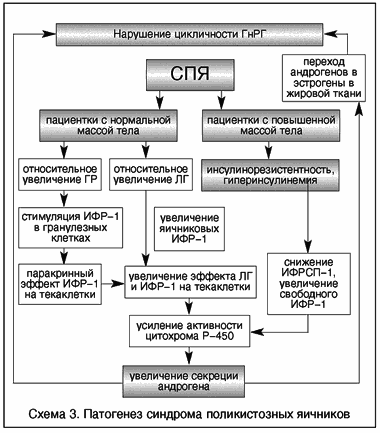
Схема 3. Патогенез синдрома поликистозных яичников
3. Однако имеется ряд хорошо известных состояний ИР, которые не связаны с ГА, например, простое ожирение и СД 2 типа . Для объяснения, почему не у всех пациенток с ожирением и ГИ развивается гиперандрогения и СПЯ, выдвинута гипотеза о существовании генетической предрасположенности к стимулирующему действию инсулина на синтез андрогенов в яичнике . Очевидно, существует ген или группа генов, которые делают яичники женщины с СПЯ более чувствительными к стимуляции инсулином продукции андрогенов .Молекулярные механизмы, приводящие к развитию инсулинорезистентности, до конца не изучены. Однако последние достижения в области молекулярной биологии позволили определить структуру гена, кодирующего рецептор к инсулину у женщин с овариальной гиперандрогенией.
Moller и Flier изучали последовательность аминокислот в структуре ДНК-цепей у больных с овариальной гиперандрогенией. Они обнаружили замещение триптофана на серозин в кодоне 1200. Исследователи предположили, что такое изменение нарушает процесс активации тирозин-киназной системы в рецепторе к инсулину. Низкая активность инсулиновых рецепторов приводит к развитию ИР и компенсаторной ГИ.
Yoshimasa et al. описали другой вариант точечной мутации у больной с гиперандрогенией, инсулинорезистентностью и черным акантозом. Они обнаружили замещение серина на аргинин в тетрамерной структуре инсулинового рецептора. Данная мутация в активном локусе приводила к невозможности соединения a- и b-субъединиц, в результате чего функционально активный рецептор не синтезировался. Приведенные исследования - лишь первые попытки выявления специфической генетической этиологии стромального текоматоза яичников.
Позднее Dunaif A. отмечает, что при синдроме поликистозных яичников ИР может быть обусловлена нарушением аутофосфорилирования b-субъединиц инсулинового рецептора (иР), цитоплазматическая часть которых обладает тирозинкиназной активностью. При этом повышается инсулиннезависимое фосфорилирование остатков серина (СПЯ-ser) с подавлением активности тирозинкиназы (вторичный передатчик сигнала, определяющий чувствительность инсулина к одноименным рецепторам). Данный дефект характерен только для СПЯ-зависимой ИР, при других инсулинорезистентных состояниях (ожирение, ИНСД) эти изменения не выявляются .
Нельзя исключить, что при СПЯ-ser существует некий серинфосфорилирующий фактор. Так, например, выделяют ингибитор серин/треонинфосфатазы, который, по-видимому, и нарушает фосфорилирование иР при СПЯ-ser. Данное соединение схоже с недавно выделенным мембранным гликопротеидом РС-1 (ингибитор тирозинкиназы инсулинового рецептора), но последний не увеличивает инсулиннезависимое фосфорилирование серина иР.
Подобными свойствами обладает и фактор некроза опухоли-a (ФНО-a): фосфорилирование остатков серина IRS-1 (один из вторичных передатчиков сигнала иР) под влиянием ФНО-a влечет за собой подавление тирозинкиназной активности иР.
Moller et al. обнаружили, что фосфорилирование серина Р450с17 человека, ключевого фермента, регулирующего биосинтез надпочечниковых и овариальных андрогенов, повышает 17,20-лиазную активность. Модулирование энзимной активности стероидогенеза за счет фосфорилирования серина было описано для 17b-гидроксистероиддегидрогеназы. Если предположить, что один и тот же фактор (энзим) фосфорилирует серин инсулинового рецептора, вызывая ИР, и серин Р450с17, вызывая гиперандрогению, то тогда можно объяснить взаимосвязь СПЯ и ИР. В экспериментах in vitro было показано, что протеинкиназа А (серин/треонинкиназа) катализирует фосфорилирование серина инсулиновых рецепторов (схема 4).

Схема 4. Ген инсулинорезистентности при СПЯ
Роль лептина при СПЯВ последнее время проводился ряд исследований, посвященных биологической роли лептина, результаты которых обнадеживают. Являясь протеиновым гормоном, лептин влияет на пищевое поведение и оказывает пермиссивное действие в отношении инициации полового созревания у животных. Роль данного гормона в регуляции метаболизма и репродуктивной функции у человека, к сожалению, окончательно не выяснена. По этой причине данные об уровне лептина при овариальной гиперандрогении в сочетании с инсулинорезистентностью и представления о его роли в развитии этих изменений весьма противоречивы.
В последнее время проводился ряд исследований, посвященных биологической роли лептина, результаты которых обнадеживают. Являясь протеиновым гормоном, лептин влияет на пищевое поведение и оказывает пермиссивное действие в отношении инициации полового созревания у животных. Роль данного гормона в регуляции метаболизма и репродуктивной функции у человека, к сожалению, окончательно не выяснена. По этой причине данные об уровне лептина при овариальной гиперандрогении в сочетании с инсулинорезистентностью и представления о его роли в развитии этих изменений весьма противоречивы.Так, согласно результатам исследования, проведенного Brzechffa et al. (1996), значительная часть женщин в популяции с СПЯ имеет уровень лептина выше, чем ожидалось с учетом их ИМТ, свободного тестостерона, чувствительности к инсулину. С другой стороны, последние работы в этой области не показали существенных различий уровней лептина в исследуемых группах при СПЯ и в группах контроля. Кроме того, было установлено, что на содержание лептина не оказывают влияние базальный уровень инсулина, содержание гонадотропинов и половых стероидов. Однако Zachow и Magffin (1997), принимая во внимание данные о наличии мРНК рецепторов лептина в овариальной ткани, продемонстрировали прямое действие указанного гормона на стероидогенез клеток гранулезы крыс in vitro. При этом было показано дозозависимое подавляющее действие лептина на ИФР-1, потенцированное увеличением ФСГ-стимулированного синтеза Е 2 клетками гранулезы. Эти данные подтверждают гипотезу о том, что повышение уровня лептина у лиц с ожирением может противодействовать созреванию доминантного фолликула и овуляции. Весьма интересными являются данные Spicer и Franciso (1997), свидетельствующие о том, что лептин в нарастающих концентрациях (10-300 нг/мл) ингибирует инсулинзависимую продукцию Е 2 и прогестерона в культуре клеток гранулезы. Этот эффект обусловлен наличием специфических сайтов связывания для лептина. По аналогии с этим можно предположить, что высокий уровень лептина может снижать чувствительность у других тканей-мишеней к действию эндогенного инсулина, приводя к развитию ИР при ожирении.
Диагноз
Диагностика синдрома овариальной гиперандрогении при типичной клинической картине не представляет трудностей. Прежде всего это нарушение менструальной функции по типу олиго-, опсо- или аменореи, ановуляция и обусловленное ею первичное или вторичное бесплодие, гирсутизм, угревая сыпь, у 40% больных имеется ожирение различной степени выраженности. При гинекологическом осмотре выявляется двухстороннее увеличение размеров яичников, нередко на фоне гипопластичной матки.
Важное место в диагностике СПЯ занимают гормональные методы исследования , направленные на выявление гиперандрогении, ее источника и определение уровня гонадотропных гормонов: ЛГ и ФСГ. У больных с СПЯ часто встречается преобладание уровня ЛГ над ФСГ, соотношение их нарушено и увеличено (больше 2,5-3). Уровень пролактина нормальный, хотя у 30% больных наблюдается его некоторое повышение.
Уровень экскреции с мочой суммарных 17-КС при СПЯ колеблется в широких пределах и мало информативен. Определение фракций 17-КС (ДГА, 11-окисленных кетостероидов, андростерона, этиохоланолона) также не обеспечивает выявление локализации источника гиперандрогении . Подтверждением овариального источника гиперандрогении является повышение уровня андростендиона (А) и тестостерона (Т) крови и повышение соотношения А/Т. Надпочечниковый генез гиперандрогении подтверждается при повышении уровня дегидроэпиандростерона (ДГА) и его сульфата (ДГА-С) и 17-оксипрогестерона (17-ОН-Р) в крови. Для уточнения локализации источника гиперандрогении предложены различные функциональные тесты, наибольшее распространение из которых получили проба с дексаметазоном, синактеном-депо.
С учетом открытия новых патогенетических звеньев в развитии СПЯ для оценки состояния углеводного обмена необходимо проводить стандартный глюкозо-толерантный тест (75 мл глюкозы per os) с определением уровня глюкозы и иммуно-реактивного инсулина (ИРИ). Свидетельством в пользу инсулинорезистентности являются также ИМТ более 25 и ОТ/ОБ больше 0,85, а также дислипидемия.
Лечение
В основе современного подхода к патогенетическому лечению СПЯ лежит принцип восстановления нарушенной функции яичников
, то есть устранение ановуляции, что в свою очередь приводит к снижению гиперандрогении и восстановлению фоликулогенеза. Однако изучение особенностей этиопатогенеза овариальной гиперандрогении приводит к заключению, что выбор методов адекватного лечения СПЯ оказывается непростой задачей.
Комбинированные оральные контрацептивы - наиболее часто используемая при СПЯ группа препаратов. Механизм действия заключается в подавлении повышенного ЛГ, нормализации соотношения ЛГ/ФСГ, повышении синтеза печенью СССГ. После отмены достигается “ребаунд-эффект”, заключающийся в нормализации гипоталамо-гипофизарной функции, снижении гиперпродукции андрогенов овариальной тканью, нормализации фолликулогенеза и восстановлении овуляции.
Лечение проводится по стандартной схеме: по 1 таблетке в день с 5 по 25 день цикла в течение 3-6 месяцев. При необходимости курсы повторяют. Однако известно, что длительный прием эстроген-гестагенных контрацептивов может привести к гиперинсулинемии, усугубляя тем самым основное патогенетическое звено СПЯ.
Некоторые контрацептивы имеют в своем составе гестагенные компоненты производные 19-норстероидов (норэтистерон, левоноргестрел), обладающих в разной степени андрогенными эффектами, в связи с чем назначение препаратов, содержащих эти компоненты, у больных с гирсутизмом ограничено. Более целесообразно при симптомах гиперандрогении использовать оральные контрацептивы с гестагеном без андрогенного действия.
Возможно применение гестагенных препаратов, лишенных андрогенных свойств в виде монотерапии, особенно при гиперплазии эндометрия. Дидрогестерон назначают по 1 таблетке (10 мг) 2 раза в день с 14-16 по 25 день цикла продолжительностью от 3 до 6 курсов.
Наиболее эффективным средством стимуляции овуляции при СПЯ является антиэстрогенный препарат кломифенцитрат . Основными эффектами антиэстрогенов являются снижение гиперсенсибилизации гипофиза к действию ГнРГ, снижение продукции ЛГ, индукция овуляторного выброса ЛГ, стимуляция овуляции. Препарат назначается по 50 мг, 100 мг в сутки с 5 по 9 день цикла до достижения овуляции по тестам функциональной диагностики, но не более 3-х курсов подряд. В последнее время появились публикации о влиянии кломифенцитрата на систему инсулин-инсулиноподобный фактор роста. В них указывалось, что к 5 дню проводимой стимуляции овуляции кломифеном (150 мг/сут) определялось прогрессивное снижение (максимально на 30%) уровня ИФР-1. Однако в ряде других аналогичных исследований достоверного снижения базального уровня инсулина в ответ на введение кломифена не было обнаружено.
Появление препаратов с антиандрогенными свойствами значительно расширило терапевтические возможности при СПЯ. Наиболее широко применяется препарат Диане-35, содержащий 35 мг этинилэстрадиола и 2 мг ципротерона ацетата. Кроме действия, характерного для оральных контрацептивов, препарат блокирует действие андрогенов на уровне клеток-мишеней, в частности, волосяных фолликулов. Последнее приводит к уменьшению гирсутизма. Препарат применяют по стандартной схеме, как оральный контрацептив курсами по 6 и более циклов. Однако нужно отметить наличие отрицательного эффекта этих препаратов на липидный и углеводный обмены, проявляющегося в повышении уровня холестерина, липопротеидов низкой плотности, а также в увеличении гиперинсулинемии, что требует постоянного динамического контроля за этими показателями у пациенток с СПЯ. Антиандрогенными свойствами обладают также спиронолактон, который широко применяется в лечении андрогензависимых дермопатий.
Одним из основных направлений в современной терапии овариальной гиперандрогении является поиск и применение препаратов и средств, направленных на устранение инсулинорезистентности и компенсаторной гиперинсулинемии.
Прежде всего это мероприятия, обеспечивающие снижение избыточной массы тела: низкокалорийная диета (в пределах 1500-2200 ккал/сут) с ограничением жиров и легко усваиваемых углеводов, ограничение потребления соли до 3-5 г в сутки, занятия умеренной физической нагрузкой, нормализация режима труда и отдыха. Возможно применение препаратов, способствующих снижению ИМТ, например, орлистата, селективно угнетающего желудочно-кишечные липазы (“блокатор жира”) или сибутрамина, блокирующего обратный захват норадреналина и серотонина в синапсах гипоталамического центра “насыщения”. Увеличенный расход энергии (термогенез) также обусловлен синергическим взаимодействием между усиленной функцией норадреналина и серотонина в центральной нервной системе. Это выражается в селективной активации центрального симпатического воздействия на бурую жировую ткань за счет непрямой активации b 3 -адренорецепторов.
Следующим этапом является применение препаратов, улучшающих нарушенную чувствительность тканей к действию инсулина. В литературе имеются данные о снижении гиперандрогении и восстановлении менструальной и овуляторной функции при назначении препаратов ряда бигуанидов (метформин /Сиофор®/, “Берлин-Хеми”). Они потенцируют действие инсулина на рецепторном и пострецепторном уровне и значительно улучшают чувствительность тканей к данному гормону. В некоторых исследованиях показано значительное снижение уровня инсулина натощак и через 2 часа после нагрузки 75 г глюкозы у женщин с СПЯ, применявших метформин. Это снижение коррелировало со снижением уровня андрогенов. Необходимо отметить также, что применение бигуанидов, нормализующих углеводные нарушения, нередко приводит к снижению ИМТ у пациенток с ожирением и положительно влияет на липидный обмен.
В мировой литературе сообщаются результаты применения препаратов, относящихся к классу тиазолидиндионов. Исследования показали, что на фоне лечения троглитазоном (200-400 мг/сут) улучшается чувствительность к инсулину у женщин с СПЯ, снижается уровень андрогенов. Однако выявленное цитотоксическое, гепатотоксическое действие этой группы препаратов ограничивает возможность их широкого применения. Ведется поиск новых препаратов, избирательно влияющих на чувствительность к инсулину.
Несмотря на значительный арсенал различных средств, применяемых для лечения овариальной гиперандрогении, терапия данной патологии должна быть комплексной и последовательной, учитывающей ведущее патогенетическое звено на данном этапе лечения.
Лечение женщин с СПЯ должно быть направлено не только на коррекцию выявленных симптомов этого заболевания, но и на профилактику возможных будущих осложнений. Очень важным является подавление избыточной секреции андрогенов и индуцирование стабильности ежемесячных менструальных кровотечений, что радежно достигается при применении препаратов с антиандрогенными свойствами (Диане-35).
В случае неэффективности консервативной терапии через год можно ставить вопрос об оперативном лечении - лапароскопии с клиновидной резекцией яичников или их лазерной вапоризацией . Эффективность хирургического лечения высокая (до 90-95% восстановления овуляции), а предварительная патогенетическая терапия повышает стабильность достигнутого результата.
Литература:1. Овсянникова Т.В., Демидова И.Ю., Глазкова О.И. Проблемы репродукции, 1998; 6: 5-8.
2. Гинзбург М.М., Козупица Г.С. Проблемы эндокринологии, 1997; 6: 40-2.
3. Старкова Н.Т. Клиническая эндокринология. Руководство для врачей, 1991; 399.
4. Givens J.R., Wiedeme E. B-endorphine and B-lipotropin levels in hirsute women: correlation with body weight. J Clin Endocr Metabol. 1980; 50: 975-81.
5. Aleem F.A., McIntosh T. Elevated plasma levels of f-endorph in a group of women with polycystic ovarian desease. Fertil and Steril. 1984; 42: 686-9.
6. Дедов И.И., Сунцов Ю.И., Кудрякова С.В. Проблемы эндокринологии. 1998; 6: 45-8.
7. Francis S., Greenspan, Forshman P.H. Basic and clinical endocrinology. 1987.
8. Акмаев И.К. Проблемы эндокринологии. 1990; 12-8.
9. Barbieri R.L., Hornstein M.D. Hyperinsulinemia and ovarian hyperandrogenism: cause and effect. Endocrinol Metab Clin North Am. 1988; 17: 685-97.
10. Barbieri R.L., Macris A., Ryan K.J. Insulin stimulates androgen accumulation in incubation of human ovarian stroma and theca. Obstet Gynecol. 1984; 64: 73-80.
11. Barbieri R.L., Ryan K.J. Hyperandrogenism, insulin resistence, acantosis nigricans: a common endocrinopathy with unique pathophysiologic features. Am J Obstet Gynecol. 1983; 147: 90-103.
12. Barbieri R.L., Smith S., Ryan K.J. The role of Hyperinsulinemia in the pathogenesis of ovarian Hyperandrogenism. Fertil and Steril. 1988; 50: 197-210.
13. Stuart C.A., Prince M.J., Peters E.J. Obstet Gynecol. 1987; 69: 921-3.
14. Yen S.S.C. Chronic anovuletion causet by peripheral endocrine disorders. In: Yen S.S.C., Jaffe R.B. Reproductive endocrinology: physiology, pathophysiology, and clinical managment. Philadelphia: Saunders W.B. 1986; 462-87.
15. Moller D.E., Flier J.S. Detection of an alteration in the insulin-reseptor gene in a patient with insulin resistance, acantosis nigricans and polycystic ovarian syndrome. N Engl J Med. 1988; 319: 1526-32.
16. Burgen G.A., Givens J.R. Insulin resistance and hyperandrogenism: clinical syndromes and possible mechanisms. Hemisphera Pablishing CO, Washington, DC. 1988; 293-317.
17. Speroff L., Glass R. H. Clinical gynecologic. Endocrinology and Infertiliti 5 th ed. 1994.
18. Yoshimasa Y., Seino S., et al. Insulin resistance diabetes due to a point mutacion that privents insulin proreceptor processing./ Science. 1988; 240: 784-9.
19. Dunaif A. Endocrin. Rev., 18(6): 1997; 12: 774-800.
Этинилэстрадиол + ципротерона ацетат
Диане-35 (торговое название)
(Shering AG)
РОСТОВСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
КАФЕДРА ВНУТРЕННИХ БОЛЕЗНЕЙ
Реферат на тему:
“ Гиперандрогения”
Преподаватель Коломацкая Ольга Евгеньевна
Выполнила студентка 5 группы ЛПФ IV курса
Новичкова Полина Дмитриевна
Ростов-на-Дону
Гиперандрогения – состояние, связанное с избыточной секрецией андрогенов и/или усиленным их воздействием на организм, которое у женщин чаще всего проявляется вирилизацией (появление мужских черт), у мужчин гинекомастией (увеличение молочных желез) и импотенцией.
Андрогены - название группы стероидных гормонов, производимых в основном яичками у мужчин и яичниками у женщин, а также корой надпочечников. К андрогенам относят, например: тестостерон, 17-ОН-прогестерон (оксипрогестерон), ДГЭА-сульфат и т.д.
Среди всех эндокринных заболеваний в гинекологической практике чаще всего встречаются патология щитовидной железы и гиперандрогения.
Весь процесс контролируется гормонами гипофиза – АКТГ (аденокортикотропным гормоном) и ЛГ (лютеинизирующим гормоном).
Синтез всех стероидных гормонов начинается с превращения холестерина в прегненолон. Этот этап происходит во всех стероидпродуцирующих тканях.
Остальные процессы также в той или иной степени происходит во всех органах, имеющих отношение к стероидогенезу, однако на выходе в разных органах продуцируются как одинаковые так и разные стероидные гормоны.
Продукция стероидных гормонов может происходить не только в этих органах, но также и на периферии. В частности для женщины важную роль в продукции стероидов играет подкожная жировая клетчатка.
Гиперандрогения- причины возникновения заболевания:
Факторы риска: эндокринная патология (адреногенитальный синдром, опухоли надпочечников или яичников, патология гипофиза) .
Причиной гиперандогении является длительное (месяцы – годы) повышение уровня мужских гормонов андрогенов в женском организме.
Источниками мужских гормонов в женском организме могут быть яичники или надпочечники, если рассматривать только неопухолевые варианты болезни. При нарушении процесса превращения андрогенов в эстрадиол они могут накапливаться в избытке и поступать в кровь. Наиболее частой основой для выработки избытка андрогенов в яичниках является их поликистозное перерождение, то есть образование в ткани яичников множества содержащих жидкость пузырьков. По разным источникам такой формой болезни страдают от 6 до 10 % женщин репродуктивного возраста. Сверх неприятных кожных проявлений у таких больных часто развивается ожирение, артериальная гипертензия, высока вероятность развития сахарного диабета. Даже при регулярном менструальном цикле половина таких женщин бесплодна.
Основной причиной развития поликистоза яичников в настоящее время признается инсулинорезистентность, то есть недостаточная чувствительность тканей к инсулину.
В надпочечниках в норме синтезируются андрогены. Их синтез находится под контролем адренокортикотропного гормона гипофиза (АКТГ). Поэтому любые состояния, сопровождающиеся хроническим повышением выброса АКТГ из гипофиза, могут вызвать повышение уровня мужских гормонов в организме женщины. Такими состояниями могут быть: хронический психологический стресс, физиологически стресс, имеющий место при спортивных перетренировках, частичная (парциальная) несостоятельность коры надпочечников, врожденная гиперплазия надпочечников.
Симптомы гиперандрогении
Среди всех симптомов гиперандрогении преобладают следующие:
Гирсутизм – избыточный рост волос у женщин, так называемое оволосение по мужскому типу, является самым частым признаком гиперандрогении. О нем можно говорить при появлении волос на животе по срединной линии, на лице, груди. Вместе с тем на голове возможны залысины.
Следует различать этот симптом от гипертрихоза – избыточный рост волос, не зависимый от андрогенов, который может быть как врожденным, так и приобретенным (при различных заболеваниях, например при порфириях). Надо также обращать внимание на расовую принадлежность пациентки – так у эскимосок и женщин выходцев из среднеазиатских стран оволосение более выражено, нежели у женщин в Европе или Северной Америке.
Акне, шелушение кожи – косметический дефект, который, как правило, является сопутствующим при других, более серьезных симптомах.
Опсоолигоменорея (укороченные и разделенные длительным промежутком месячные), аменорея (отсутствие месячных) и бесплодие – чаще всего данный симптом встречается при поликистозе яичников, сопровождающимся гиперандрогенией.
Ожирение – характерно как для яичниковой патологии, так и для патологии со стороны надпочечников.
Атрофия мышц конечностей, мышц живота, остеопароз, атрофия кожи – наиболее характерно для синдрома Кушинга (или Иценко-Кушинга в русскоязычной литературе).
Высокий риск инфекций – связано с пониженным иммунным ответом организма, в связи с неадекватной гормонпродукцией.
Нарушение толерантности к глюкозе – преимущественно при поражении надпочечников, часто так же и при патологии со стороны яичников.
Формирование наружных половых органов промежуточного типа (гипертрофия клитора, мочеполовой синус, частичное сращение больших половых губ) – выявляется сразу после рождения или в раннем детском периоде; чаще при врожденной гиперплазии коры надпочечников.
Артериальная гипертония, гипертрофия миокарда, ретинопатия (невосполительное повреждение сетчатки глаза).
Депрессия, сонливость, повышенная утомляемость – связано кроме всего с тем, что нарушается секреция глюкокортикоидов надпочечников.
Причины гиперандрогении
Состояния, сопровождающиеся гиперандрогенией:
Синдром поликистозных яичников (синдром Штейна-Левенталя) - сочетание аменореи и двусторонних множественных кист яичников. При этом чаще всего встречается: нарушение менструального цикла, бесплодие, гирсутизм и ожирение. Диагноз ставиться по наличию гиперандрогении и хронической ановуляции. Повышен риск инсулинорезистентности и гиперинсулинэмии, сахарный диабет наблюдается у 20% больных.
Синдром Кушинга – состояние характеризующиеся избытком продукции глюкокортикоидов надпочечниками. У большинства больных отмечается увеличение веса с отложением жира на лице (лунообразное лицо), шее, туловище. Характерно: гирсутизм; нарушение менструальной функции, бесплодие; атрофия мышц конечностей, остеопороз; снижение иммунорезистентности; нарушение толерантности к глюкозе; депрессия и психозы; у мужчин – возможно гинекомастия и импотенция. Существуют следующие варианты синдрома:
А. АКТГ (аденокортикотропный гормон продуцируемый гипофизом) зависимый синдром:
Гипофизарный – чаще всего опухолевое поражение гипофиза
Эктопический – секреция АКТГ (или кортиколиберина) опухолью, любой локализации
Б. АКТГ независимый синдром:
Надпочечниковый – рак, аденома или гиперплазия коры надпочечников
Экзогенный – самолечение препаратами глюкокортикоидов или лечение другой патологии, с вынужденным приемом данных препаратов
Врожденная гиперплазия коры надпочечников – наследственное генетическое заболевание. Важны следующие формы:
Недостаточность 21-гидроксилазы (90-95% случаев) – частой причиной является недостаточность альдостерона. Характеризуется: ацидоз (смещение кислотно-основного баланса в организме в сторону увеличения кислотности); патология развития наружных половых органов.
Недостаточность 11β-гидроксилазы – нарушение формирование кортизола. Характеризуется: классическая форма - вирилизация, артериальная гипертония, гипертрофия миокарда, ретинопатия, патология развития наружных половых органов; неклассическая форма - гирсутизм, угревая сыпь, нарушение менструального цикла.
Недостаточность 3 β-гидроксистероиддегидрогеназы – его можно заподозрить при повышении уровней дегидроэпиандростерона и дегидроэпиандростерона сульфата при нормальных или незначительно повышенных уровнях тестостерона и андростендиона.
Андрогенсекретирующие опухоли яичников и надпочечников – чаще всего данная патология характерна для людей с выраженной вирилизацией или же с ее резким появлением и быстрым прогрессированием. При этом повышение уровня тестостерона более характерно для опухолей яичников, а повышение уровня дегидроэпиандростерона сульфата – для опухолей надпочечников. Наиболее часто встречается при:
Гранулезоклеточной опухоли яичников,
Текоме яиника,
Андробластоме яичника,
Стероидоклеточных опухолях яичников (лютеома беерменности, лейдигома),
Адеоме надпочечников – 90% среди всех опухолей яичников, которые характеризуются продукцией только андрогенов.
Стромальная гиперплазия яичников и гипертекоз – наблюдается чаще всего после 60-80 лет. Повышено соотношение уровня эстрадиола и эстрона.
Характеризуется: гиперандрогенией, ожирением, артериальной гипертонией, нарушение толерантностик глюкозе и раком тела матки.
Представленные выше патологии чаще всего сопровождаются гиперандрогенией, однако список этот может существенно дополнен. В виду невозможности описать все в одной статье мы сочли разумным представить только основную патологию.
Диагностика гиперандрогении
Первым и главным методом в диагностике гиперандрогенных состояний является лабораторное исследование крови на содержание на уровень стероидных гормонов. Отступая не на долго в сторону, приведем показатели нормы для стероидных гормонов в крови:
Нормы для женщин:
Тестостерон – 0,2-1,0 нг/мл или 0,45 - 3,75 нмоль/л
Эстрадиол – 0,17±0,1нмоль/л - фолликулиновая фаза, 1,2±0,13нмоль/л-овуляция, 0.57±0,01 нмоль/л – лютеиновая фаза.
Прогестерон - 1.59±0,3 нмоль/л – фолликулиновая фаза, 4.77±0.8 нмоль/л– овуляция, 29.6±5.8 нмоль/л – лютеиновая фаза
Кортизол - 190-750 нмоль/л
Альдостерон - 4-15 нг/м
Кроме того, надо знать нормы гормонов, влияющих на продукцию стероидов:
ЛГ - фолликулиновая фаза – 1,1 – 11,6 мМЕ/л, овуляция 17 – 77 мМЕ/л, лютеиновая фаза 0 -14,7 мМЕ/л
АКТГ – 0 – 46 пг/мл
ФСГ - фолликулиновая фаза-2,8-11,3 мМЕ/л, овуляция - 5,8 – 21 мМЕ/л, лютеиновая фаза - 1,2 - 9,0 мМЕ/л
Разнообразие заболеваний, которые сопровождаются гиперандрогенными состояниями, предрасполагает рассмотрение методов диагонстики (а так же лечения) отдельно для каждого заболевания. Рассмотрим методы диагностики описанных выше патологий:
Синдром поликистозных яичников (СПКЯ):
Данные анамнеза и осмотра (см. выше)
Анализ крови на гормоны – обычно наблюдается выравнивание соотношения тестостерона и ЛГ; возможно измение уровня ФСГ; в 25% случаев гиперпролактинэмия; повышение уровня глюкозы
УЗИ – увеличение яичников и двусторонние множественные кисты
Лапароскопия – редко применяется, как правило при болевом синдроме неясного генеза, когда по какой-либо причине нет возможности выполнить УЗИ
Синдром Кушинга:
В общем анализе крови – лейкоцитоз; лимфопения и эозинопения.
Анализ крови на гормоны одновременный избыток половых гормонов, синтезируемых надпочечниками.
УЗИ исследование – возможно, для диагностики эктопической формы (выявление опухолей, локализованных вне надпочечников) и надпочечниковой формы (для диагностики крупных опухолей надпочечников).
МРТ (магнитнорезонансная томография) – при подозрении на онкологию, при неинформативности УЗИ.
Краниография – рентгеновское исследование черепа в 2х проекциях для диагностики патологий гипофиза (деформация турецкого седла – место расположения гипофиза в клиновидной кости черепа).
Повышение 17-гидроксипрогестерона в сыворотке при недостаточности 21-гидроксилазы (выше 800 нг%); возможно проведение пробы с АКТГ. Важно отметить, что подобное состояние можно выявить у плодов еще до рождения и начать лечение еще в утробе матери – диагностика при высоком риске данной патологии заключается в исследовании околоплодных вод на уровень прогестерона и андростендиона.
Пробы с АКТГ так же проводят и для диагностики недостаточности 11β-гидроксилазы и 3 β-гидроксистероиддегидрогеназы.
Андрогенсекретирующие опухоли:
Анализ крови на гормоны – повышение уровня андрогенов – тестостерона для опухолей яичников; дегидроэпиандростерона – для опухолей надпочечников
УЗИ малого таза – для опухолей яичников.
КТ (компьютерная томография) и МРТ – преимущественно для опухолей надпочечников.
Катетеризация надпочечниковой вены с определением уровня тестостерона – спорный метод, ввиду большого количества осложнений.
Сцинтиграфия брюшной полости и малого таза с I-холестерином.
Анализ крови на гормоны – уровни яичниковых андрогенов обычно равны мужской норме.
Уровень гонадотропных гормонов обычно нормальный – дифференциальная диагностика от СПКЯ
Лечение гиперандрогении
Медикаментозное лечение
А. Медроксипрогестерон – эффективен при гирсутизме. 20-40 мг/сут внуть или 150 мг внутримышечно 1 раз в 6-12 нед.
Б. Комбинированные перооральные контрацептивы – снижают секрецию стероидных гормонов, уменьшают оволосение у 70% больных с гирсутизмом, лечат акне, утсраняют дисфункциональные маточные кровотечения. Предпочтительны ПК со слабым андрогенным действием: дезогестрел, гестоден и норгестимат.
В. Глюкокортикоиды – дексаметозон – 0,25 мг/сут (не более 0,5 мг/сут).
Г. Кетоконазол – 200 мг/сут – подавляет стероидогенез.
Д. Спироналактон 200 мг/сут в течении 6 мес. – улучшение у 70-80% пациенток – при гирсутизме; возможно нарушение менструального цикла
Оперативное лечение – при неэффективности медикаментозного лечения:
А. Клиновидная резекция некогда популярный, ныне этот метод уже не так часто применяется в стационарах
Б. Лапароскопическая электрокоагуляция яичников – коагулируют (прижигают) яичник в 4-8 точках электродом
Синдром Кушинга:
АКТГ зависимый
А. Медикаментозное лечение - к сожалению, во многих случаях диагноз ставиться довольно поздно. Медикаментозное лечение чаще рассматривается как подготовка к операции, нежели как самостоятельный метод лечения. Применяют ингибиторы стероидогенеза, чаще всего кетоконазол – 600-800 мг/сут
Б. Хирургическое лечение – производят аденомэктомию, которая, при микроаденомах (менее 1 см размер опухоли) положительные результаты отмечаны у 80% больных; при макроаденомах – у 50%.
В. Лучевая терапия – обычно при патологии гипофиза. Положительные результаты у взрослых в 15-25% случаев.
АКТГ независимый – чаще всего единственный радиукальный метод лечения при опухолях надпочечников – операция с последующим назначением глюкокортикоидов в послеоперационном периоде и митотана, для предотвращения рецидивов.
Врожденная гиперплазия коры надпочечников:
Дексаметозон – для подавления секреции АКТГ, в дозе 0,25 – 0,5 мг/сут внутрь. Проводят лечение под контролем кортизола (если его уровень не менее 2 мкг%, то лечение проводится эффективное без последующих осложнений со стороны гипоталамо-гипофизарной системы).
Выше упоминалось о том, что выявление патологии и ее лечение возможно еще в утробе (для недостаточности 21-гидроксилазы). Применяется дексаметозон в дозе 20 мкг/кг/сут в 3 приема. При высоком риске формирования патологии у ребенка лечение начинают с момента выявления беременности. В случае, если плод оказывается мужского пола – лечение прекращают, если женского – продолжают. Если лечение начато до 9 недель беременности и до родов – риск патологии формирования половых органов значительно меньше. Данная схема лечения является предметом спора специалистов, указывающих на то, что возможно большое количество осложнений для матери при довольно невысокой эффективности самого лечения.
Андрогенсекретирующие опухоли яичников и надпочечников
Лечение только в онкологическом стационаре, чаще всего операция в сочетании с химиотерапией, лучевой или гормональной терапией. Прогноз лечение зависит от времени диагностики и характера самой опухоли.
Стромальная гиперплазия яичников и гипертекоз:
При легкой форме эффективна клиновидная резекция яичников. Возможно применение аналогов гонадолиберина. При тяжелой патологии – возможно двусторонняя ампутация яичников с целью нормализации артериального давления и коррекции нарушений толерантности к глюкозе.
С появлением симптомов гиперандрогении обязательно обращение к врачу. Чаще всего – врач-эндокринолог или гинеколог, нередко терапевт. Обязательно детально разобраться в причинах гирсутизма и других симптомов, и при необходимости, направить в специализированный стационар.
Любое самолечение полностью и категорически противопоказано! Допустимо только удаление волос косметическими средствами.
Профилактика гиперандрогении
Гиперандрогения не имеет специфических мер профилактики. К основным можно отнести соблюдение режима правильного питания и образа жизни. Каждой женщине необходимо помнить, что чрезмерное похудание способствует гормональным нарушениям и может приводить как к описанному состоянию, так и ко многим другим. Кроме того, не следует увлекаться занятиями спортом, что тоже (особенно при приеме стероидных препаратов) может приводить к гиперандрогении.
Реабилитацию требуют пациенты с гиперандрогенией опухолевого генеза, подвергшиеся оперативному и химиотерапевтическому лечению. Кроме того, обязательно консультация с психологом, особенно для молодых девушек с выраженным гирсутизмом и гинекологическими проблемами.
Осложнения гиперандрогении.
Спектр возможно осложнений при всех описанных выше заболеваниях крайне велик. Можно отметить только некоторые, самые важные:
При врожденной патологии возможны аномалии развития, самые распространенные из них - аномалии развития половых органов.
Метастазирования злокачественных опухолей – осложнение, более характерное для опухолей надпочечников.
Осложнения со стороны других систем органов, которые подвергаются негативному влиянию изменения гормонального фона при патологии надпочечников, гипофиза и яичников: хроническая почечная недостаточность, патология щитовидной железы и т.д.




