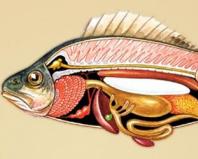
Помірна рестрикція. Рестриктивні порушення дихання. Симптоми дихальної недостатності
Процес дихання є дуже важливою складовою для будь-якого живого організму на нашій планеті. Порушення дихання може викликати різні хвороби, пов'язані насамперед із кисневим голодуванням. Дуже розвинена дихальна система, незважаючи на її зрілість і багато структурність, схильна до різних перебоїв і порушень. Через складну влаштованість організму людини причин тому може бути кілька, починаючи від і закінчуючи проблемами з повітроносними шляхами.
Фахівці розрізняють такі види порушення дихання:
- обструктивний;
- рестриктивний;
- змішаний.
Дані типи розрізняються в першу чергу з причин, що спричинили порушення біомеханіки дихання. При обструктивному вигляді значно зменшується прохідність повітроносних шляхів, які несуть кисень до органів людини.
Існує така недуга, як синдром обструктивного, що характеризується саме тим, що під час сну у людини можуть відбуватися численні зупинки дихання, при цьому сплячий не може це контролювати. Більшості його головними причинами лікарі називають зайву вагу (скупчення жирових) та анатомічні особливості будови носа та горла.
Рестриктивні порушення дихання – це порушення, пов'язані з обмеженими розправами легень. Через легеневі перебої більше енергії задіюється в інших органів, відповідальних за дихання, відповідно, у кілька разів збільшується навантаження на них. Утрудняється вентиляція легень та газообмін у них. Ці ознаки також призводять до кисневого голодування на етапах ускладнення.
Лікування
Лікування даних порушень дихання зазвичай спрямоване не так на полегшення симптомів, але в відновлення нормальної вентиляції легких. Для цих цілей проводиться оксигенотерапія – подача кисню в організм людини у певних кількостях та концентраціях. Також успіх у лікуванні матимуть масаж грудної клітки, заняття плаванням, аквааеробікою, лікувальна фізкультура, звичайні прогулянки свіжим повітрям.
Відео
Характер вентиляції легень може змінюватися внаслідок різних причин. Дихання посилюється при роботі, зміні метаболічних потреб організму та при патологічних станах. Можна довільно посилити дихання.
Зниження вентиляції також може бути довільним, або наступати в результаті дії регуляторних або патологічних факторів. Розроблено фізіологічно чітку класифікацію типів вентиляції, в основу якої покладено парціальний тиск газів в альвеолах. Відповідно до цієї класифікації виділяються такі типи вентиляції.
1. Нормовентиляція – нормальна вентиляція, при якій парціальний тиск СО2 в альвеолах підтримується на рівні близько 40 мм рт. ст.
2. Гіпервентиляція – посилена вентиляція, що перевищує метаболічні потреби організму (раСО2 3. Гіповентиляція – знижена вентиляція порівняно з метаболічними потребами організму (раС02 > 40 мм рт. ст.).
4. Підвищена вентиляція - будь-яке збільшення альвеолярної вентиляції порівняно з рівнем спокою незалежно від парціального тиску газів в альвеолах (наприклад, при м'язовій роботі).
5. Еупное - нормальна вентиляція у спокої, що супроводжується суб'єктивним почуттям комфорту.
6. Гіперпное - збільшення глибини дихання незалежно від того, чи підвищена при цьому частота дихальних рухів чи ні.
7. Тахіпное – збільшення частоти дихання.
8. Брадіпное – зниження частоти дихання.
9. Апное - зупинка дихання, зумовлена головним чином відсутністю фізіологічної стимуляції дихального центру (зменшення напруги С02 в артеріальній крові).
10. Диспное (задишка) – неприємне суб'єктивне відчуття недостатності дихання або утрудненого дихання.
11. Ортопное - виражена задишка, пов'язана із застоєм крові в легеневих капілярах внаслідок недостатності лівого серця. У горизонтальному положенні цей стан посилюється, і тому лежати таким хворим важко.
12. Асфіксія - зупинка чи пригнічення дихання, пов'язані переважно з паралічем дихальних центрів. Газообмін при цьому різко порушений (спостерігається гіпоксія та гіперкапнія).
Вентиляція легень часто порушується через патологічні зміни дихального апарату. З метою діагностики доцільно розрізняти два типи порушень вентиляції – рестриктивний та обструктивний.
До рестриктивного типу порушень вентиляції відносяться всі патологічні стани, при яких знижується дихальна екскурсія легенів.
Обструктивний тип порушень вентиляції обумовлений звуженням повітроносних шляхів, тобто. підвищенням їхнього аеродинамічного опору. Подібні стани зустрічаються, наприклад, при накопиченні в дихальних шляхах слизу, набуханні їх слизової оболонки або спазмі бронхіальних м'язів (бронхіальна астма, астмоїдний бронхіт тощо). У таких хворих опір видиху підвищено, і тому згодом легкість легких і ФОЕ у них збільшуються. Патологічне стан, що характеризується надмірним розтягуванням легень та його структурними змінами (зниженням числа еластичних волокон, зникненням альвеолярних перегородок, збіднінням капілярної мережі), називається емфіземою легень.
Для диференціальної діагностики між рестриктивними та обструктивними порушеннями вентиляції використовують методи, спрямовані на виявлення особливостей цих патофізіологічних станів. При рестриктивних порушеннях знижується здатність легень розправлятися, тобто. зменшується їхня розтяжність. Для обструктивних порушень характерно збільшення опору дихальних шляхів. В даний час розроблена досконала апаратура для визначення розтяжності легень або опору повітроносних шляхів, проте орієнтовно виявити той чи інший тип порушення вентиляції можна і за допомогою більш простих методів:
Зниження ЖЕЛ – ознака рестриктивного порушення вентиляції.
Проте, якщо розтяжність легень (Сл) відбиває здатність розправлятися лише легень, то ЖЕЛ залежить також рухливості грудної клітини. Отже, ЖЕЛ може зменшуватися як легеневих, так і позалегеневих рестриктивних змін.
Об'єм форсованого видиху (тест Тіффно). Об'єм повітря, що видаляється з легень при форсованому видиху (ОФВ) за одиницю часу (зазвичай за секунду), є хорошим показником обструктивних порушень вентиляції. Цей обсяг визначається наступним чином: випробуваний, повітроносні шляхи якого з'єднані зі спірометром закритого або відкритого типу, робить максимальний вдих, потім на короткий час затримує дихання і після цього здійснює якомога глибший і швидкий видих. При цьому записують спірограму, яку можна визначити об'єм повітря, видихнутий за 1 с (ОФВ). Зазвичай використовують відносне значення цього обсягу, виражене у відсотках ЖЕЛ. Тож якщо ОФВ дорівнює 3 л, а ЖЕЛ - 4 л, то відносний ОФВ становить 75%. У осіб віком до 50 років зі здоровими легенями відносний ОФВ дорівнює 70-80%, з віком він знижується до 65-70%). При обструктивних динамічних опорах подовжується і відносний ОФВ знижується.
Максимальний дебіт повітря. Переконатися в наявності обструктивних порушень вентиляції можна шляхом вимірювання максимальної експіраторної об'ємної швидкості повітря. Для цього, як і при вимірюванні ОФВ, досліджуваний після максимального вдиху здійснює форсований видих. Дебіт повітря визначається з допомогою пневмотахографа. У осіб із здоровими легенями максимальний дебіт повітря, виміряний таким методом, становить близько 10 л/с. При збільшенні аеродинамічного опору повітроносних шляхів він значно знижується. Існує деяке граничне значення дебіту повітря при видиху, перевищити яке неможливо навіть за максимальних зусиль. Це з будовою бронхіол. У їх стінках немає опорних хрящових елементів, таким чином, бронхіоли поводяться як податливі трубки, що спадаються, коли зовнішній (плевральний) тиск перевищує тиск у їхньому просвіті. Якщо під час видиху розвивається значний тиск, аеродинамічний опір в бронхіолах підвищується. Ця залежність стає вираженою в тому випадку, коли зменшується пружна тяга еластичних волокон легеневої тканини (в нормі ця тяга сприяє підтримці просвіту бронхіол). Подібні стани спостерігаються, наприклад, при емфіземі легень. У цьому випадку спроба зробити форсований видих супроводжується спадом бронхіол.
Максимальною вентиляцією легень (МВЛ) називають об'єм повітря, що проходить через легені за певний проміжок часу при диханні з максимально можливою частотою та глибиною. Діагностична цінність цього показника полягає в тому, що він відображає резерви дихальної функції, а зниження цих резервів є ознакою патологічного стану. Для визначення максимальної вентиляції легень здійснюють спірометричний вимір у людини, що робить форсовану гіпервентиляцію з частотою дихальних рухів близько 40-60 за 1 хв. Тривалість дослідження має становити приблизно 10 с. В іншому випадку можуть розвиватися гіпервентиляційні ускладнення (алкалоз). Об'єм дихання, виміряний таким способом, перераховують, щоб отримати значення об'єму за одну хвилину. МВЛ залежить від віку, статі та розмірів тіла і в нормі у молодої людини вона становить 120-170 л/хв. МВЛ знижується як при рестриктивних, і при обструктивних порушеннях вентиляції. Таким чином, якщо у досліджуваного виявлено зменшення МВЛ, то для диференціальної діагностики між цими двома типами порушень необхідно визначити інші показники (ЖЕЛ і ОФВ).
32.3.1. Обструктивні порушення вентиляції легень
Як відомо, обструктивні легеневі розлади дуже поширені. В даний час відомо близько 100 захворювань, що супроводжуються бронхообструктивним синдромом. Останній є основним виразом бронхіальної астми, обструктивної емфіземи легень, хронічного бронхіту, бронхоектатичної хвороби, експіраторного стенозу, стенотичного ларинготрахеїту, муковісцедозу та інших захворювань.
Причинами обструктивних порушень вентиляціїє:
Обтурація дихальних шляхівабо блювотними масами та сторонніми тілами, або здавленням трахеї, головного, великих, середніх і дрібних бронхів збільшеними лімфатичними вузлами, загрудинним зобом, пухлиною середостіння, або потовщенням, або спазмом стінок повітроносних структур.
Інфекції(Туберкульоз легень, сифіліс, грибкові ураження, хронічний бронхіт, пневмонія).
Алергічні ураження дихальних шляхів(Анафілактичний шок, анафілаксія, бронхіальна астма).
Отруєння медикаментами(передозування холінотропними препаратами, вагостимуляторами, бета-адреноблокаторами та ін.).
Обструктивні порушення вентиляції легень – зменшення просвіту (прохідності) або верхніх дихальних шляхів(носових ходів, носоглотки, входу в горло, голосової щілини, трахеї, великих та середніх бронхів), або нижніх дихальних шляхів(Дрібні бронхи, повітроносні бронхіоли (запалення, набряк, обтурація, спазм).
Обструктивні порушення вентиляції легень - це така форма патології системи зовнішнього дихання, при якій збільшено опір струму повітря в дихальних шляхах при закупорці, звуженні, спазмі або здавленні ззовні. Обструктивні порушення повітроносних шляхів можуть бути ендо- та екзобронхіального генезу .
Біофізичною основою обструктивних розладів є збільшення нееластичного дихального опору.Це обумовлено:
аеродинамічний (в'язкісний) опір,що виникають через переміщення молекул газу та тертя об стінки дихальних шляхів;
фрикційним (деформаційним) опором,що з'являються у зв'язку з дією сил тертя під час дихання (при патологічних змінах дихальних шляхів та легеневої паренхіми фрикційний опір зростає у кілька разів);
інерційним опором,залежним від маси тіла та особливостей будови грудної клітки (існує як у спокої, при дихальній паузі, так і при диханні, при вдиху та видиху).
Загальне нееластичний опір залежить від ДО. У здорових осіб воно становить 13-35 см вод. ст./л/хв. При спокійному вдиху сила дихальних м'язів необхідна подолання опору еластичної тяги легких. При форсованому диханні різко зростають сили, спрямовані на подолання нееластичного опору та витрачаються на подолання опору струму повітря в трахеї та бронхах. Величину нееластичного опору визначає стан повітроносних шляхів та швидкість потоку повітря. При обструктивних порушеннях опір струму повітря при вдиху та видиху зростає. Можливе пролабування мембранної частини трахеї, великих та середніх бронхів та часткова або повна обтурація їхнього просвіту. Втрата легкими еластичних властивостей призводить до спадання дрібних бронхів і особливо бронхіол і, відповідно, збільшення бронхіального опору на видиху.
При тахіпное (частому поверхневому диханні) швидкість повітряного потоку при видиху збільшується, відбувається його завихрення, збільшується турбулентний компонент опору, подолання якого потрібно додаткове зусилля дихальних м'язів. Адекватної альвеолярної вентиляції у своїй немає, а об'ємно-часові параметри змінюються.
У разі підвищення опору дихальних шляхів збільшується робота дихальних м'язів, підвищуються енергетичні витрати та киснева заборгованість дихальної мускулатури. Отже, компенсаторно-пристосувальні можливості зовнішнього дихання апарату обмежуються. Це обмеження пов'язане і з феноменом так званої динамічної компресії повітроносних шляхів (експіраторного колапсу)і, таким чином, обумовлено не стільки нездатністю дихальних м'язів збільшувати зусилля, скільки механічними властивостями системи легені – повітроносні шляхи.
Механізм експіраторного колапсу повітроносних шляхів ось у чому. Бронхіоли, що мають просвіт 1-5 мм, як відомо, позбавлені хрящових кілець і тому можуть повністю спадатися, що веде до оклюзії їхнього просвіту. Таке спадання (колапс) відбувається в тому випадку, якщо тиск зовні бронхіол (внутрішньогрудний) виявляється більшим, ніж зсередини. Це частіше може відбуватися при активному, форсованому видиху. З одного боку, скорочення експіраторних м'язів веде до різкого підвищення внутрішньогрудного тиску, а з іншого - зростання швидкості експіраторного потоку повітря в бронхіолах (тут зусилля, створюване експіраторними м'язами сумується з еластичною тягою легень) за законом Бернуллі супроводжується падінням бічного тиску, що надається потоком поверхню бронхіальної стінки. Місце, де обидві сили (зовнішнє та внутрішній тиск на стінку бронхіоли) врівноважуються, називають точкою рівного тиску. У цьому місці просвіт бронхіоли ще зберігається відкритим через жорсткі та пружні властивості її стінки, які зумовлюють опір деформації останньої. Однак дещо «нижче за течією» експіраторного потоку, де переважання внутрішньогрудного тиску над внутрішньобронхіолярним виявляється достатнім, настає спад бронхіоли (рис. 32-2).
Мал. 32-2. Схема динамічної компресії нижніх повітроносних шляхів при форсованому видиху.
Позначення: А -альвеол; ТРД -точка рівного тиску; ТС-точка спадання бронхіоли. 1 - Тиск, створюваний експіраторними м'язами; 2- еластичний потяг легень
Велике значення у патогенезі обструктивних порушень має гіперреактивність бронхів - виражена бронхоконстрикція, що виникає у відповідь роздратування. Речовини, які мають дратівливу дію, проникають в інтерстицій, активують нервові рецептори, в першу чергу n. vagus і викликають бронхоспазм, який усувається фармакологічною блокадою активності м-холінорецепторів. Основою бронхоконстрикції є як специфічна (алергічна), так і неспецифічна (неалергічна) гіперреактивність бронхіального дерева.
У стінках повітроносних шляхів та тканинах легень утворюються бронхо- та вазоактивні речовини. Епітелій бронхіального дерева секретує фактор, що має властивості бронхорелаксації. При бронхоспазму цей чинник більшою мірою впливає на тонус гладкої мускулатури великих бронхів. Секреція його знижена при пошкодженні епітеліальних клітин, наприклад при бронхіальній астмі, що сприяє стійкій обструкції бронхів.
В ендотелії легеневих судин та епітелії бронхів синтезується пептид ендотелін-I, що виявляє виражену не тільки бронхо-, а й вазоконстрикторну дію. Продукція ендотеліну-I збільшується при гіпоксії, серцевій недостатності, бактеріємії, хірургічних втручаннях.
Ейкозаноїди, що утворюються при розпаді арахідонової кислоти, мають як релаксуючу (простагландини Е), так і констрикторну (лейкотрієни, РGF 2α, тромбоксан A 2) дію на гладку мускулатуру. Однак сумарний їхній ефект проявляється в бронхоконстрикції. Крім того, одні ейкозаноїди (тромбоксан А 2) стимулюють агрегацію тромбоцитів, інші (РGI 2) не тільки пригнічують агрегацію тромбоцитів, а й підвищують проникність судинної стінки, викликають її дилатацію, посилюють секрецію слизової оболонки. .
Під впливом метаболітів арахідонової кислоти виникає дисбаланс адренорецепторів з переважанням активності α-адренорецепції над -адренорецепцією. У гладком'язових клітинах бронхів знижується вміст цАМФ, уповільнюється видалення іонів Са2+ із клітинної цитоплазми. Іони Са2+ активують фосфоліпазу А2, що визначає метаболізм арахідонової кислоти. Формується "порочне коло", що підтримує бронхоконстрикцію.
Патофізіологічні наслідки обструкції
повітроносних шляхів
Обструкція повітроносних шляхів, як правило, призводить до:
Збільшення опору повітряному потоку, особливо на видиху, викликає затримку повітря в легенях та зростання функціональної залишкової ємності, переростання та здуття легень. Переростання грудної клітки супроводжується збільшенням роботи дихання.
Зниження ефективності дихальних м'язів. Потрібна велика міра зміни внутрішньогрудного тиску, щоб змінити обсяг легень. Дихання забезпечується з використанням навіть менш ефективних дихальних м'язів.
Збільшення споживання кисню та продукції вуглекислоти. Це веде до гіпоксемії, зниження рН, розвитку дихального та метаболічного ацидозу.
Розвитку неузгодженості між вентиляцією та перфузією. Це призводить до падіння артеріальної оксигенації. Погано перфузовані зони додатково посилюють порушення виведення 2 .
Розвитку дихальної недостатності.
Переважно за обструктивним типомрозвиваються :
бронхіальна астма,
хронічна обструктивна хвороба легень (ХОЗЛ), основу якої становить хронічний бронхіт або емфізема, або їх поєднання,
Бронхоектатична хвороба.
Бронхіальна астма (БА)– хронічне тяжке захворювання легень людини. Представляє найпоширеніше алергічне захворювання. Ним хворіє від 0,3 до 1% населення.
Причинами БАможуть бути: а) внутрішні (генетично детерміновані дефекти у вигляді гіперчутливості слизової оболонки бронхів); б) зовнішні (куріння, пил, токсичні гази, пилок рослин та ін.).
Бронхіальній астмі (БА) передує стан передастми, що характеризується наявністю наступних ознак:
Гострі чи хронічні захворювання легень з обструкцією бронхів. (Астматичний та обструктивний бронхіт, гостра пневмонія з обструкцією, гострі респіратонні захворювання з обструкцією).
Позалегеневі прояви зміненої реактивності.
Еозинофілія крові та/або мокротиння.
Спадкова схильність.
Якщо ці ознаки виявляються, то протягом трьох років виникає клінічно виражена бронхіальна астма у 70% пацієнтів. Чим менше цих ознак, тим менша ймовірність розвитку даного захворювання.
На бронхіальну астму припадає 67-72% бронхообструктивних станів. бронхіальна астма характеризується різко вираженою зміною зовнішнього дихання, (обумовленого бронхіальною обструкцією та порушенням газообміну між зовнішнім середовищем та організмом).
Обов'язковою ознакою бронхіальної астми є напад задухи протягом декількох годин.
Розлад дихання при ХА частіше має експіраторний характер і супроводжується відчуттям стиснення грудної клітки. Грудна клітка знаходиться в положенні максимального вдиху (розширюється).
У диханні беруть участь як м'язи грудної клітини, а й м'язи шиї, плечового пояса, спини, черевної стінки.
БА викликається різними етіологічними факторами, центральне становище серед яких займають алергени, головним чином, інфекційного та пилкового походження, а також холодне повітря, пил, фізичне навантаження, емоції, лібератори (гістамін та ін) тощо.
Патогенез нападу БА визначається наступними змінами.
1. Останнім часом велике значення у формуванні обструктивного синдрому надається ролі гіперреактивності бронхів(Рис. 32-3).
2. Іншим важливим патогенетичним фактором БА є зміни в імунокомпетентній системі, що знайшло відображення в сучасній класифікації бронхіальної астми (інфекційно-алергічна та неінфекційно-алергічна або атопічна).
При імунозалежній формі бронхіальної астми потрапили в сенсибілізований організм алергени взаємодіють з реагінами (IgE), фіксованими на опасистих клітинах, ендотеліоцитах, гладко-м'язових клітинах та ін. ), опасистих клітин, еозинофілів, моноцитів, лімфоцитів та гістіофагів, що продукують різні ФАВ.
У 2% всіх астматиків розвивається аутоімунний варіант бронхіальної астми, що є найважчим варіантом розвитку даного захворювання. У розвитку бронхіальної астми важливе значення мають різні види імунодефіцитів.
|
Сенсибілізація |
Вроджені дефекти мембран та рецепторного апарату клітин-мішеней |
Тривалі інфекції дихальних шляхів |
||||
|
Підвищення дратівливості (реактивності) бронхів |
||||||
|
Вплив алергену |
Загострення інфекції дихальних шляхів |
Дія фізико-хімічних подразників |
Психо-емоційне збудження |
|||
|
Напад бронхіальної астми |
||||||
Рис.32-3.Патогенез нападу бронхіальної астми.
3. Сильну скорочувальну або розслаблюючу дію на тонус гладких м'язів бронхів надає неадренергічна та нехолінергічнасистема за участю субстанції Р, вазоактивного інтестинального пептиду (ВІП). Так, бронхоспазм може бути обумовлений посиленням бронхосуживаючих стимулів (підвищенням холінергічної, -адренергічної активності або субстанції Р) або зниженням -адренергічної активності або ВІП-вивільнення.
4. В основі БА може лежати лікарський механізм, зокрема аспіриновий. Аспіринова астма характеризується: непереносимістю аспірину, бронхоспазмом та полінозом. У механізмі бронхоконстрикторної дії ацетилсаліцилової кислоти лежить його здатність змінювати метаболізм арахідонової кислоти. При активізації ліпооксигеназного шляху її метаболізму підвищується вироблення лейкотрієнів (у тому числі повільно реагує субстанції), що мають бронхоспастичну дію.
5. Дисгормональні порушення, що призводять до розвитку бронхіальної астми.
5.1. бронхіальна астма, обумовлена глюкокортикоїдною недостатністю.Формується частіше за абсолютної глюкокортикоїдної недостатності (якщо кортизолу в крові на 25-30 % менше норми), у цьому випадку необхідна замісна терапія глюкокортикоїдами. Відносна глюкокортикоїдна недостатність проявляється симптомами гіпокортицизму, при цьому рівень кортизолу зазвичай відповідає нормальним значенням. У цьому випадку необхідно перевірити тканинну чутливість до глюкокортикоїдів. За наявності тканинної глюкокортикоїдної резистентності тканин розвивається дуже завзятий у клінічному перебігу варіант бронхіальної астми, при якому доводиться давати гіпердози глюкокортикоїдних препаратів.
5.2. Дизоваріальна БАхарактеризується загостренням, що виникає за 2 - 3 дні на початок менструації. Це зумовлено дефектом вироблення бронходилатуючого прогестерону та надлишком естрогенів. Виявляється підвищенням ректальної температури більш ніж на 10С.
5.3. БА з вираженим адренергічним дисбалансомхарактеризується підвищенням активності α-адренорецепторів. При цьому навіть нормальний рівень адреналіну може спричинити патологічну бронхоспастичну реакцію. Часто така реакція виникає при передозування адреноміметиками(Коли протягом дня проводиться більше 5 їх інгаляцій по 2 вдихи).
5.4 Холінергічний варіант БАпов'язані з конституційними особливостями чи захворюваннями внутрішніх органів, у яких спостерігається виражена ваготонія. Даний варіант спостерігається у 1% хворих на бронхіальну астму, у яких виділяється багато мокротиння (1/2 - 1 склянка на добу). В анамнезі зазвичай відзначається виразкова хвороба, брадикардія, гіпотонія, мокрі (потні) долоні. Купірувати напад БА можна за допомогою атропіну.
6. Нервові механізми виникнення бронхіальної астми.
6.1 Умовно-рефлекторний механізмможе бути провідним у низки хворих (класичний приклад - штучна паперова троянда своїм виглядом провокує напад бронхіальної астми). Можливо і умовно-рефлекторне припинення нападу бронхіальної астми. Зазначено, що непереносимість запахів у хворих на бронхіальну астму на 70 % носить не алергічний, а умовно-рефлекторний характер. Таких хворих вдається лікувати навіюванням.
6.2. Домінантниймеханізм зводиться до того, що дрібні роздратування можуть призводити до сумації збудження та виникнення нападів бронхіальної астми. Виникнення іншої, сильнішої домінанти може на деякий час пригнічувати домінанту бронхіальної астми. Відзначено також, що при підвищенні температури тіла понад 38 0 С, напади бронхіальної астми не виникають.
6.3. Вагусниймеханізм проявляється, як правило, тим, що напади бронхіальної астми виникають у другій половині ночі. Це пов'язано з дефецитом медіаторів неадренергічної системи, зокрема ВІП (що володіє потужною бронходилатуючої дією).
6.4. Механізм, зумовлений неадекватною адаптацієюорганізму до мікросоціального середовища,також може лежати в основі розвитку бронхіальної астми. За таким механізмом бронхіальної астми виникає у 10-20% пацієнтів (частіше у дітей, рідше – у дорослих).
7. Обструктивні зміни бронхів при ХА можна пояснити також впливом прозапальних медіаторів(тканинних гормонів), які посилено звільняються з опасистих клітин у стінках дихальних шляхів. p align="justify"> Особливе місце серед них займає гістамін, що обумовлює спазм гладкої мускулатури, розвиток артеріальної гіперемії, підвищення проникності стінок капілярів, збільшення секреції слизу. В останні роки в патогенезі БА велике значення надається підвищенню продукції простагландину PGF 2α та зниженню продукції PGE 2 .
Значною мірою обструкції повітроносних шляхів сприяють набряк їх слизової оболонки та її інфільтрація.
Основними клінічними проявами бронхіальної астмиє: -інспіраторна та, особливо, експіраторна задишка; - напади ядухи, кашлю, сором за грудиною, свистячих хрипів, особливо, при видиху; -ціаноз, тахікардія, лейкоцитоз, еозинофілія та ін. Ці ознаки посилюються при фізичних навантаженнях, охолодженні, інфікуванні слизової оболонки різних відділів дихальних шляхів.
Принципи лікування БАбазуються на виявленні та обліку етіологічних та патогенетичних факторів, що провокують рецидив захворювання, а також на проведенні заходів та використанні засобів, що запобігають або послаблюють їх патогенні впливи на верхні та нижні дихальні шляхи.
Основними патогенетичними підходами, що знижують реактивність слизових дихальних шляхів, є:
попередження взаємодії алергенів з IgE,
зниження або блокування вивільнення медіаторів алергії,
дилатація м'язів бронхів і, особливо, бронхіол та ін.
Для цього необхідно здійснювати заходи, спрямовані на:
елімінацію або нейтралізацію алергенів,
проведення специфічної імунотерапії (гіпосенсибілізації),
попередження або зниження опосередкованого імунними механізмами бронхоспазму, що викликається медіаторами опасистих клітин,
використання різних протизапальних засобів та бронходилататорів (симпато- та адреноміметиків: ефедрину, адреналіну та ін., що збільшують утворення цАМФ; антихолінергічні засоби: атропін та ін.; кортикостероїди: преднізолон, дексаметозон та ін.; неспецифічні протизапальні засоби, а: індометацин, піроксикам, бронхолітин та ін інгібітори фосфодіестерази: метилксантини - еуфілін, теофілін та ін).
32.3.2. РЕСТРИКТИВНІ ПОРУШЕННЯ ДИХАННЯ
Основу рестриктивних розладів (від латів. restrictio – обмеження) дихання становить зміна в'язкоеластичних властивостей легеневої тканини.
Дорестриктивним порушеннямдиханнявідносять гіповентиляційні розлади, що виникають внаслідок обмеження розправлення легень через пошкодження білків, їх інтерстиція під дією ферментів (еластазу, колагеназу та ін.). До складу інтерстицію входять колаген (60-70%), еластин (25-30%), глікозаміноглікани (1%), фібронектин (0,5%). Фібрилярні білки забезпечують стабільність каркасу легень, його еластичність та розтяжність, створюють оптимальні умови для виконання основної газообмінної функції. Структурні зміни білків інтерстиція проявляються зниженням розтяжності легеневої паренхіми та підвищенням еластичного опору легеневої тканини. Так, у разі розвитку емфіземи порушується рівновага між синтезом і розпадом еластину, оскільки наявний надлишок протеаз не врівноважується інгібіторами протеолітичних ферментів. При цьому найбільше значення має дефіцит -1-антитрипсину.
Опір, який доводиться долати дихальним м'язам під час вдиху, може бути еластичним та нееластичним.
Еластичний потяглегенів спрямовано скорочення обсягу легких. Тобто це величина, зворотна розтяжності. Приблизно 2/3 еластичної тяги легень залежить від поверхневого натягу стінок альвеол. Еластична тяга легень чисельно дорівнює транспульмональному тиску. На вдиху збільшується транспульмональний тиск та обсяг легень. Залежно від фази дихання є коливання внутрішньоплеврального тиску: наприкінці спокійного видиху воно становить 2-5 см вод. ст., наприкінці спокійного вдиху – 4-8 см вод. ст., на висоті максимального вдиху – 20 см вод. ст.
Розтяжність легень(податливість легень, легеневий комплеанс) – величина, що характеризує зміни обсягу легень на одиницю транспульмонального тиску. Розтяжність – величина, обернено пропорційна еластичності. Основним фактором, що визначає межу максимального вдиху, є розтяжність. У міру поглиблення вдиху розтяжність легень прогресивно зменшується, а еластичний опір стає найбільшим. Тому головним фактором, що визначає межу максимального видиху, є еластичний опір легень.
Підвищення транспульмонального тиску на 1 см вод. ст. проявляється підвищенням обсягу легень на 150-350 мл. Робота з подолання еластичного опору пропорційна дихальному обсягу, тобто розтяжність легень на вдиху тим більше, чим більша робота при цьому відбувається. Труднощі розправлення легеневої тканини визначають ступінь гіповентиляційних порушень.
Виділяють дві групи факторів, що призводять до обмежувальних порушень вентиляції легень: 1) позалегеневі та 2) внутрішньолегеневі.
Рестриктивні розлади дихання позалегкового походження можуть бути наслідкомздавлення тулуба, викликаного впливами механічного характеру (здавлення одягом або предметами виробничого обладнання, важкими предметами, землею, піском тощо, особливо, при різних катастрофах), або виникають внаслідок обмеження екскурсій грудної клітки при пневмо-, гідро- та гемотораксі та інших патологічних процесах, що ведуть до компресії легеневої тканини та порушення розправи альвеол при вдиху.
Пневмотораксвиникає через попадання повітря в плевральну порожнину та буває первиннимабо спонтанним,(наприклад, при кістах бронхів, сполучених із плевральною порожниною) та вторинним(пухлини, туберкульоз та ін.), травматичногоі штучного походження, а за механізмом - відкритим, закритим та клапанним.
Гідротораксз'являється при попаданні в плевральну порожнину або ексудату (розвивається ексудативний плеврит), або транссудата (розвивається транссудативний плеврит).
Гемоторакспроявляється наявністю в плевральній порожнині крові та виникає при пораненнях грудної клітки та плеври, пухлинах плеври з пошкодженням судин.
До рестриктивних порушень дихання відносяться також поверхневі, прискорені дихальні рухи, що виникають у зв'язку з надмірним окостенінням реберних хрящів і малою рухливістю зв'язково-суглобового апарату грудної клітки.
Особливе значення у розвитку позалегеневих форм рестриктивних порушень зовнішнього дихання має плевральна порожнина.
У людини в нормальних умовах плевральна рідинаутворюється в апікальній частині парієтальної плеври; дренування рідини відбувається за допомогою лімфатичних стоматів (пор). Місцем їх найбільшої концентрації є медіастинальна і діафрагмальна частини плевральної порожнини. Таким чином, фільтрація і реабcрбція плевральної рідини є функцією парієтальної плеври (рис.32-4).

Мал. 32-4. Механізм утворення плевральної рідини
Знання механізмів освіти плевральної рідини пояснює цілу низку клінічних синдромів. Так, у хворих з легеневою гіпертензією і ознаками правошлуночкової недостатності також як і у хворих з хронічним легеневим серцем в стадії правошлуночкової недостатності, накопичення рідини в плевральної порожнини. Скупчення транссуду в плевральній порожнині виникає при дисфункції лівого шлуночка з розвитком клінічних ознак застійної серцевої недостатності. Виникнення цього клінічного феномену пов'язують з підвищенням тиску в легеневих капілярах, що і призводить до просування трансудата через поверхню віцеральної плеври в її порожнину. Видалення транссуду за допомогою торакоцентезу знижує обсяг циркулюючої крові і тиск в легеневих капілярах, тому в сучасні терапевтичні рекомендації ця процедура включена як обов'язкова при веденні хворих.
Патофізіологічні закономірності виникнення транссудупри застійній серцевій недостатності обумовлені великим об'ємом крові в системі малого круга кровообігу. При цьому виникає ефект обсяг-тиск-трансудат.
В основі цих закономірностейрозвитку екскудативного плевриту лежить потік білків ферментів, що зростає, формових елементів і електролітів крові в плевральну порожнину.
Поверхня плевральних листків мікроворсинок концентрує велику кількість глікопротеїнів і гіалуронової кислоти і оточена фосфоліпідами, тобто. за своєю морфологічною характеристикою нагадує альвеолярний суфактант. Ці особливості пояснюють легкість ковзання поверхонь перієтального і вицерального листків плеври. Мезотеліальні клітини беруть активну участь у запальному процесі. Міграція нейтрофілів в плевральну порожнину здійснюється під дією деяких цитокінів, до яких, зокрема, відноситься інтерлейкін-8. Висока концентрація даного цитокіну спостерігається у хворих з емпіємою плеври. Місцем синтезу цього цитокіну є залучені в запальний процес мезотеліальні клітини та їх воринки. Інтерлейкін-8 виявився чутливим тестом у проведенні хіміотерапії та оцінці її ефективності у хворих з мезотеліомою. Його розглядають як біомаркер в диференційній діагностиці запальних і канцерогенних плевритів. В експериментальних умовах були використані антитіла проти інтерлейкіну-8, що призвело до інгібуючого ефекту на процес міграції нейтрофілів в плевральну порожнину. У фізіологічних умовах інгібуючим ефектом на дію хемоаттрактанта має інтерлейкін-10.
Рестриктивні розлади дихання легеневого походження виникають у результаті : 1) зміни в'язкоеластичних властивостей, у тому числі втрати еластичних волокон, легеневої тканини; 2) пошкодження сурфактанту або зниження його активності.
Порушення в'язкоеластичних властивостей легеневої тканинивідзначається при: - різних видах ушкоджень паренхіми легень; - дифузному фіброзуванні легень різного походження (первинна емфізема легень, пневмосклероз, пневмофіброз, альвеоліти); - осередкових змін у легенях (пухлини, ателектази); - Набряку легень різного генезу (запальний, застійний). Розтяжність легень різко (понад 50 %) зменшується зі збільшенням кровонаповнення легень, інтерстиціальному набряку, зокрема запального характеру. Так, у випадках, що далеко зайшли, емфіземи легень (через зниження розтяжності їх навіть при максимальному вдиху) не вдається досягти межі функціональної розтяжності легень. Через зниження еластичної тяги легень відбувається формування бочкоподібної грудної клітини.
Зменшення розтяжності легеневої тканини є типовим проявом фіброзу легень.
Втрата еластичних властивостей легеневої тканини відбувається при руйнуванні еластичних волокон під впливом тривалої дії багатьох патогенних факторів (токсини мікробів, ксенобіотики, тютюновий дим, порушення харчування, літній та старечий вік), що активують протеолітичні ферменти.
Розтяжність та еластичність легень залежать також від тонусу альвеол та термінальних бронхіол.
Зниження кількості та активності сурфактанту сприяєспаду альвеол. Останньому перешкоджає покриття їх стінок сурфактантом (фосфоліпід-протеїн-полісахарид) та наявність міжальвеолярних перегородок. Сурфактантна система є складовою аерогематичного бар'єру. Як відомо, сурфактант виробляється пневмоцитами 2-го порядку, складається з ліпідів (90%, з них 85% припадає на фосфоліпіди), білків (5-10%), мукополісахаридів (2%) і має період напіврозпаду менше двох діб. Сурфактантний шар забезпечує зниження поверхневого натягу альвеол. При зменшенні легеневих обсягів сурфактант попереджає колабування альвеол. На висоті видиху об'єм легень мінімальний, поверхневий натяг завдяки вистиланню ослаблений. Тому для розкриття альвеол потрібно менший транспульмональний тиск, ніж відсутність сурфактанту.
Переважно за рестриктивним типом розвиваються :
гостра дифузна пневмонія (крупозна пневмонія),
пневмоторакс,
гідроторакс,
гемоторакс,
ателектаз.
Крупозна пневмонія – гостре, як правило, інфекційне ексудативне запалення значного обсягу паренхіми(Респіраторних структур) легені, а також інших його анатомічних утворень. Таким чином, пневмонія (грецьк. pneumon - легеня; син.: запалення легень) - це запалення респіраторних відділів легені, що виникає у вигляді самостійного захворювання або ускладнення будь-якого захворювання.
Захворюваність на пневмоніювисока, на неї хворіють близько 1% населення Землі, з великими коливаннями в різних країнах. З віком, особливо старше 60 років, захворюваність на пневмонію та смертність від неї збільшуються, досягаючи відповідно більше 30 % та 3 %.
Етіологія пневмоній. Серед етіологічних факторів у розвитку пневмонії важливе значення мають різні віруси (аденовіруси, віруси грипу, парагрипу та ін), мікоплазми, рикетсії, бактерії (пневмококи, стрептококи, стафілококи, паличка Фрідлендера (Клебсієла) та дремолієї), гемофілії і гемофілії. . Несприятливими умовами, що прискорюють розвиток, що підсилюють тяжкість перебігу та погіршують результат захворювання, є охолодження ніг, всього тіла, недоїдання, недосипання, інтоксикації, дистрес та інші фактори, що знижують імунітет організму.
Патогенез пневмоній.Встановлено, що при пневмонії основним шляхом проникнення флогогенного фактора у легені є бронхогенний з поширенням їх по ходу дихальних шляхів до респіраторних відділів легень. Гематогенний шлях проникнення інфекційних збудників у легені – виняток. Він має місце при септичних (метастатичних) та внутрішньоутробних пневмоніях.
Патогенні мікроорганізми викликають пневмонію, як правило, тільки тоді, коли вони потрапляють у бронхи з верхніх дихальних шляхів, особливо зі слизом, який оберігає мікроби від бактеріостатичної та бактерицидної дії бронхіального секрету та сприяє їх розмноженню. Вірусна інфекція, сприяючи надмірній секреції слизу в носоглотці, що має до того ж знижені бактерицидні властивості, полегшує проникнення інфекції в нижні відділи дихальних шляхів. Крім того, вірусна інфекція порушує роботу мукоциліарного ескалатора та макрофагів легень, тим самим перешкоджаючи очищенню легень від мікробів. Встановлено, що у 50% дорослих щодня уві сні відбувається мікроаспірація слизу у дихальних шляхах. Мікроби адгезуються до епітеліальних клітин (чинники адгезії - фибронектин і сиаловые кислоти, які у щіткової облямівці епітеліальних клітин) і проникають у тому цитоплазму, у результаті розвивається мікробна колонізація епітелію. Однак, у цей момент фагоцитуючі властивості першої лінії захисту нижніх дихальних шляхів (резидентних макрофагів) проти мікроорганізмної, особливо бактеріальної, флори порушені попередніми вірусними та мікоплазмовими інфекціями. Після руйнування епітеліальних клітин слизової оболонки дихальних шляхів у вогнище запалення залучаються поліморфноядерні лейкоцити, моноцити, активується каскад комплементу, що, своєю чергою, посилює міграцію нейтрофілів у вогнище запалення.
Початкові запальні зміни у легенях при пневмоніях виявляють переважно у респіраторних бронхіолах. Це пояснюється тим, що саме в цьому місці відбувається затримка мікробів, що потрапили в легені, внаслідок наявності тут ампулоподібного розширення бронхіол, відсутності війчастого циліндричного епітелію і менш розвиненої гладкої м'язової тканини. Інфекційний агент, поширюючись межі респіраторних бронхіол, викликає запальні зміни у паренхімі легень, т. е. пневмонію. При кашлі та чханні інфікований випіт із вогнища запалення потрапляє у різні за розміром бронхи, а потім поширюється на інші респіраторні бронхіоли, що обумовлює виникнення нових вогнищ запалення. Таким чином, поширення інфекції у легенях може відбуватися бронхогенно. При обмеженні поширення інфекції внаслідок розвитку запальної реакції у безпосередній близькості від респіраторних бронхіол (як правило навколо них) розвивається осередкова пневмонія. У разі поширення бактерій та набрякової рідини через пори альвеол у межах одного сегмента та закупорки інфікованого слизом сегментарного бронха виникає сегментарна пневмонія(як правило, на тлі ателектазу), а при більш бурхливому поширенні інфікованої набрякової рідини в межах частки легені - пайова (крупозна) пневмонія.
Характерною рисою пневмоній є раннє залучення до патологічного процесу регіонарних лімфатичних вузлів (бронхопульмональних, біфуркаційних, паратрахеальних). У зв'язку з цим одним із найбільш ранніх симптомів пневмонії, який можна виявити при об'єктивному обстеженні (пальпаторна перкусія, рентгеноскопія, рентгенографія та ін.), є розширення коренів легень.
У патогенезі пневмоній певна роль приділяється також дефіциту сурфактанту. Це призводить до ослаблення його бактерицидної дії, порушення еластичності легеневої тканини та раціонального співвідношення вентиляції та кровотоку в легенях. Гіпоксія, аспірація, тютюнопаління, грамнегативні бактерії, що сприяють зниженню рівня сурфактанту в легенях, одночасно призводять до виникнення вторинних гіалінових мембран, які патологоанатоми нерідко виявляють на розтині у хворих на пневмонію. Обмежені вторинні гіалінові мембрани зазвичай не викликають вираженого порушення дихання, будучи супутниками запального процесу в легенях.
Киснева недостатність, що закономірно розвивається при пневмонії, насамперед відбивається на діяльності ЦНС. Часто в розпал пневмонії виникає дисфункція автономної нервової системи з переважанням її симпатичного відділу. У період виходу організму із токсикозу починають домінувати холінергічні реакції.
Розрізняють первинне, самостійне(частіше інфекційне, рідше неінфекційне: застійне, аспіраційне, травматичне, токсичне чи асептичне), і навіть вторинне(виникає при інших, не легеневих, первинних інфекційних захворюваннях) запалення легенів.
Клінічна картина пневмоній, що викликаються різними інфекційними та неінфекційними патогенними факторами, природно, відрізняється один від одного. Наприклад, при пневмококовій пневмонії, що найчастіше зустрічається, захворювання починається гостро з наростаючого ознобу, задишки, кашлю, до яких приєднується біль у грудях (при кашлі і навіть диханні), гнійне мокротиння з кров'ю і т.д. За лабораторними даними відзначається лейкоцитоз з ядерним зрушенням вліво, токсична зернистість нейрофілів, збільшення ШОЕ, анемія. Рентгенологічно визначаються осередкові та зливні затемнення та явища деструкції легень. На тлі ослабленого та/або жорсткого дихання вислуховуються ділянки звучних вологих хрипів.
Принципи лікування пневмонійвключають переважно етіотропне, патогенетичне та саногенетичне лікування. Лікування пневмонії має починатися якомога раніше, бути комплексним та ефективним. Провідне значення має правильний вибір антимікробного засобу, його дози та схеми лікування. Призначається препарат повинен мати виражену бактерицидну дію. Лікування пневмоній повинно проводитись:
під ретельним клініко-бактеріологічним контролем;
на тлі поліпшення (нормалізації) прохідності повітроносних шляхів (для цього призначаються теофедрін, еуфілін та його аналоги);
шляхом призначення засобів: - розріджують мокротиння (мукалтин, термопсис, препарати йоду); - що послаблюють або ліквідують ацидоз повітроносних та газообмінних тканин легень (лужні парові інгаляції 2-3 % розчином соди при температурі 50-60 0 С по 5-10 хвилин перед сном та ін.); - які мають десенсибілізуючу та протизапальну дію; - покращують кровообіг та трофіку легень (фітоадаптогени, лікувальна фізкультура, різні фізіотерапевтичні процедури: на початкових етапах -банки та гірчичники, однак, якщо є небезпека легеневої кровотечі або накопичення рідини в легенях, їх слід виключити; на етапі розсмоктування- Масаж, теплові процедури: індуктотермія, УВЧ, діадинамія) і т.д.
32.3.3. Зміни основних функціональних
показників дихання при обструктивних
та рестриктивних розладах
Для оцінки вентиляційної здатності легень, а також для вирішення питання щодо якого типу (обструктивного або рестриктивного) розвивається дихальна недостатність у клінічній практиці досліджуються різні функціональні показники. Визначення останніх ведеться або за допомогою спірометрії (статичні показники) або пневмотахометрії (динамічні показники).
Основними показниками спірометріїє: 1) дихальний об'єм (ДО), що є інспіраторним об'ємом під час спокійного дихання; 2) резервний об'єм вдиху - максимальний об'єм повітря, який здатний вдихнути випробуваний після спокійного вдиху (РВ вд.); 3) життєва ємність легень (ЖЕЛ), що є максимальним об'ємом повітря, який можна вдихнути або видихнути; 4) залишковий обсяг (ГО) - кількість повітря, що залишається у легенях навіть після максимального видиху; 5) загальна ємність легень (ОЕЛ), що становить суму ЖЕЛ та ГО; 6) функціональна залишкова ємність (ФОЕ) - обсяг повітря в легенях у стані спокою після закінчення звичайного видиху.
До динамічних показників системи диханнявідносяться: 1) частота дихання (ЧД); 2) дихальний ритм (ДР); 3) хвилинний обсяг дихання (МОД), що є твір ДО і ЧД; 4) максимальна вентиляція легень (МВЛ), що становить твір ЖЕЛ та форсованої частоти дихання; 5) обсяг форсованого видиху за 1 секунду (ОФВ 1), що виражається у відсотках до форсованої життєвої ємності легень (ФЖЕЛ); 6) форсований експіраторний потік повітря між 25% та 75% форсованої життєвої ємності легень (ФЕП25%-75%), що дозволяє оцінювати середню об'ємну швидкість повітряного потоку.
У хворих з обструктивними та рестриктивними захворюваннями виявляються характерні зміни (табл.32-1).
Обструктивні вентиляційні порушення виникають внаслідок: 1. звуження просвіту дрібних бронхів, особливо бронхіол за рахунок спазму (бронхіальна астма; астматичний бронхіт); 2. звуження просвіту за рахунок потовщення стінок бронхів (запальний, алергічний, бактеріальний набряк, набряк при гіперемії, серцевої недостатності); 3. наявності на покриві бронхів в'язкого слизу при збільшенні її секреції бокалоподібними клітинами бронхіального епітелію, або слизово-гнійного мокротиння; 4. звуження внаслідок рубцевої деформації бронха; 5. розвитку ендобронхіальної пухлини (злоякісної, доброякісної); 6. здавлення бронхів ззовні; 7. Наявності бронхіолітів.
Рестриктивні вентиляційні порушення мають такі причини:
1. фіброз легень (інтерстиціальний фіброз, склеродермія, бериліоз, пневмоконіози і т. д.);
2. великі плевральні та плевродіафрагмальні зрощення;
3. ексудативний плеврит, гідроторакс;
4. пневмоторакс;
5. великі запалення альвеол;
6. великі пухлини паренхіми легені;
7. Хірургічне видалення частини легені.
Клінічні та функціональні ознаки обструкції:
1. Рання скарга на задишку при раніше допустимому навантаженні або під час “застуди”.
2. Кашель, частіше зі мізерним відділенням мокротиння, що викликає після себе на деякий час відчуття важкого дихання (замість полегшення дихання після звичайного кашлю з відділенням мокротиння).
3. Перкуторний звук не змінений або спочатку набуває тимпанічний відтінок над задньо-бічними відділами легень (підвищення легкості легень).
4. Аускультація: сухі свистячі хрипи. Останні, за Б. Є. Вотчалом, слід активно виявляти при форсованому видиху. Аускультація хрипів при форсованому видиху цінна у плані судження про поширення порушення бронхіальної прохідності легеневими полями. Дихальні шуми змінюються в наступній півсивості: везикулярне дихання - жорстке везикулярне - жорстке невизначене (заглушує хрипи) - ослаблене жорстке дихання.
5. Пізнішими ознаками є подовження фази видиху, участь у диханні допоміжної мускулатури; втягування міжреберних проміжків, опущення нижньої межі легень, обмеження рухливості нижнього краю легень, поява коробкового перкуторного звуку та розширення зони його поширення.
6. Зниження форсованих легеневих проб (індексу Тіффно та максимальної вентиляції).
У терапії обструктивної недостатності чільне місце займають препарати бронходилатуючого ряду.
Клінічні та функціональні ознаки рестрикції.
1. Задишка при фізичному навантаженні.
2. Прискорене неглибоке дихання (коротке - швидкий вдих і швидкий видих, званий феноменом " двері, що захлопуються").
3. Екскурсія грудної клітки обмежена.
4. Перкуторний звук укорочений з тимпанічним відтінком.
5. Нижня межа легень стоїть вище звичайного.
6. Рухливість нижнього краю легень обмежена.
7. Дихання ослаблене везикулярне, хрипи тріскучі чи вологі.
8. Зменшення життєвої ємності легень (ЖЕЛ), загальної ємності легень (ОЕЛ), зниження дихального об'єму (ДО) та ефективної альвеолярної вентиляції.
9. Часто є порушення рівномірності розподілу вентиляційно-перфузійних співвідношень у легенях та дифузні порушення.
Роздільна спірографіяРоздільна спірографія або бронхоспірографія дозволяє визначити функцію кожної легені, а отже, резервні та компенсаторні можливості кожного з них.
За допомогою двопросвітної трубки, що вводиться в трахею і бронхи, і з роздувними манжетами для обтурації просвіту між трубкою і слизовою оболонкою бронха, є можливість отримати повітря з кожної легені і записати за допомогою спірографа криві дихання правої та лівої легені окремо.
Проведення роздільної спірографії показано визначення функціональних показників у хворих, які підлягають хірургічним втручанням на легких.
Безперечно, що більш чітке уявлення про порушення бронхіальної прохідності дає запис кривих швидкості повітряного потоку при форсованому видиху (пік-флуориметрія).
Пневмотахометрія- є методом визначення швидкості руху та потужності струменя повітря при форсованому вдиху та видиху за допомогою пневмотахометра. Випробовуваний після відпочинку, сидячи, робить максимально швидко глибокий видих у трубку (при цьому ніс відключений за допомогою носового затискача). Цей метод, головним чином, використовується для підбору та оцінки ефективності дії бронходилататорів.
Середні величини для чоловіків - 4.0-7.0 л/л для жінок - 3.0-5.0 л/с. Потужність видиху зменшується не тільки при бронхоспазму, але також, хоча і меншою мірою, у хворих зі слабкістю дихальної мускулатури та з різкою ригідністю грудної клітки.
Загальна плетизмографія (ОЗУ)- Це метод прямого вимірювання величини бронхіального опору R при спокійному диханні. Метод заснований на синхронному вимірі швидкості повітряного потоку (пневмотахограми) та коливань тиску в герметичній кабіні, куди поміщається хворий. Тиск у кабіні змінюється синхронно коливань альвеолярного тиску, про який судять за коефіцієнтом пропорційності між об'ємом кабіни та об'ємом газу в легенях. Плетизмографічно краще виявляються невеликі ступені звуження бронхіального дерева.
Оксигемометрія- це бронзове визначення ступеня насичення киснем артеріальної крові. Ці показання оксигемометра можна зареєструвати на папері, що рухається у вигляді кривої - оксигемограми. В основі дії оксигемометр лежить принцип фотометричного визначення спектральних особливостей гемоглобіну. Більшість оксигемометрів та оксигемографів не визначають абсолютної величини насичення артеріальної крові киснем, а дають можливість лише стежити за змінами насичення крові киснем. У практичних цілях оксигемометрія застосовується для функціональної діагностики та оцінки ефективності лікування. З метою діагностики оксигемометрія застосовується з метою оцінки стану функції зовнішнього дихання і кровообігу. Так, ступінь гіпоксемії визначається за допомогою різноманітних функціональних проб. До них відносяться - перемикання дихання хворого з повітря на дихання чистим киснем і, навпаки, проба із затримкою дихання на вдиху та на видиху, проба з фізичним дозованим навантаженням та ін.
До дефектів вентиляції легень та виникнення недостатності дихання можуть призводити різного роду хронічні та гострі патології бронхолегеневої системи (пневмонія, бронхоектатична хвороба, ателектаз, десиміновані процеси в легкому, кавернозні порожнини, абсцеси та ін.), анемія, ураження нервової , пухлини середостіння та легень, судинні захворювання серця та легень тощо.
У цій статті розглянуто рестриктивний тип дихальної недостатності.
Опис патології
Для рестриктивної дихальної недостатності характерно обмеження здатності тканини легені до спадання та розширення, що спостерігається при пневмотораксі, ексудативному плевриті, спайковому процесі в порожнині плеври, пневмосклерозі, обмеженій рухливості каркаса ребер, кіфосколіозі та ін. Недостатність дихання при таких вдиху, яка максимально можлива.
Форми
Рестриктивна обумовлена дефектами альвеолярної вентиляції через обмеженість розтягування легень. Виділяються дві форми вентиляційної недостатності дихання: легенева та позалегенева.
Рестриктивна позалегкова вентиляційна недостатність дихання розвивається через:

Причина
Причини рестриктивної дихальної недостатності має встановлювати лікар. Рестриктивна легенева вентиляційна недостатність дихання розвивається через зниження розтяжності легень, яке спостерігається при застійних та запальних процесах. Легеневі капіляри, переповнені кров'ю, і інтерстиціальна набрякла тканина заважають альвеолам повною мірою розправитися, здавлюють їх. Крім того, в цих умовах зменшується розтяжність інтерстиціальної тканини та капілярів.
Симптоми
Рестриктивна форма дихальної недостатності відрізняється низкою симптомів.
- Зниження показників легеневої ємності загалом, їх залишкового обсягу, ЖЕЛ (даний показник відбиває рівень легеневої рестрикції).
- Дефекти регуляторних механізмів виникають також через порушення функціонування дихального центру, а також його еферентних та аферентних зв'язків.
- Прояв альвеолярної рестриктивної гіповентиляції. Клінічно значущими формами є утруднене та апнейстичне дихання, а також його періодичні форми.
- Обумовлений попередньою причиною та дефектами фізико-хімічного мембранного стану розлад трансмембранного іонового розподілу.
- Коливання нейронної збудливості у дихальному центрі і, як наслідок, – зміни глибини та частоти дихання.
- Розлади зовнішньої дихальної центральної регуляції. Найчастіші причини: новоутворення та травми в довгастому (при запаленні або набряку, крововиливах у мозкову речовину або шлуночки), інтоксикація (наприклад, наркотичними препаратами, етанолом, ендотоксинами, які утворюються при недостатності печінки або уремії), ендотоксинами, деструкції (наприклад, при сифілісі, сирингомієлії, розсіяному склерозі та енцефалітах).

- Дефекти аферентного регулювання діяльності дихального центру, які проявляються надмірною або недостатньою аферентацією.
- Дефіцит збуджуючої аферентації альвеолярної рестриктивної гіповентиляції. Зменшення тонічної неспецифічної активності нейронів, розташованих у ретикулярній формації мозкового стовбура (придбане або успадковане, наприклад, при передозуванні барбітуратів, наркотичних анальгетиків, транквілізаторів та інших психо-і нейроактивних речовин).
- Надмірна збуджуюча аферентація альвеолярної рестриктивної гіповентиляції. Ознаки такі: прискорене тобто тахіпнож, ацидоз, гіперкапнія, гіпоксія. Який ще патогенез рестриктивної дихальної недостатності?
- Надмірна гальмуюча аферентація альвеолярної рестриктивної гіповентиляції. Найчастіші причини: підвищене подразнення слизових систем (при вдиханні людиною дратівливих речовин, наприклад, нашатирного спирту, при гострому трахеїті та/або бронхіті під час вдихання гарячого чи холодного повітря, сильний біль у дихальних шляхах та/або у грудній клітці (наприклад , при плевритах, опіках, травмі).
- Дефекти нервової еферентної дихальної регуляції. Можуть спостерігатися через пошкодження тих чи інших рівнях ефекторних шляхів, які регулюють функціонування дихальних м'язів.
- Дефекти кортико-спінальних шляхів до м'язів дихальної системи (наприклад, при сирингомієлії, ішемії спинного мозку, травмі або пухлинах), що призводить до втрати усвідомленого (довільного) контролю дихання, а також переходу на «стабілізоване», «машиноподібне», «автоматизоване» » дихання.

- Поразки шляхів, що проводять до діафрагми від дихального центру (наприклад, при травмі спинного мозку або ішемії, поліомієліті або розсіяному склерозі), які проявляються втратою дихального автоматизму, а також переходом на дихання довільного типу.
- Дефекти спинальних низхідних шляхів, нервових стовбурів та мотонейронів спинного мозку до дихальної мускулатури (наприклад, при ішемії спинного мозку або травмі, ботулізмі, поліомієліті, блокаді провідності нервів та м'язів при використанні ліків кураре та міастенії, невритах). Симптоми такі: зменшення амплітуди рухів дихання та апное періодичного характеру.
Відмінність рестриктивної від обструктивної дихальної недостатності
Обструктивна дихальна недостатність, на відміну від рестриктивної, спостерігається при утрудненому проходженні повітря по бронхах і трахеї внаслідок бронхоспазму, бронхіту (запалення бронхів), проникнення сторонніх тіл, здавлення трахеї та бронхів пухлиною та бронхою. У цьому порушуються функціональні можливості дихання зовнішнього: повний вдих і особливо видих утрудняються, частота дихання обмежується.
Діагностика
Рестриктивну дихальну недостатність супроводжують обмеженість наповнення повітрям легень через зниження дихальної легеневої поверхні, виключення з дихання частини легені, зменшення еластичних характеристик грудної клітки та легені, а також здібності тканини легені до розтягування (гемодинамічний або запальний легеневий набряк, великі пневмонії, пневмонізи та ін.). Якщо рестриктивні дефекти не поєднуються з порушеннями прохідності бронхів, які описані вище, не зростає опір шляхів, що несуть повітря.

Головне наслідок обмежувальних (рестриктивних) вентиляційних розладів, що виявляються при спірографії класичного виду, - це практично пропорційне зниження більшої частини легеневих ємностей та обсягів: ОФВ1, ДО, ОФВ, ЖЕЛ, РОвид, РОвд та ін.
Комп'ютерна спірографія показує, що крива потік-обсяг є копією правильної кривої у зменшеному вигляді у зв'язку зі зменшенням легеневого об'єму в цілому, який зміщений вправо.
Діагностичні критерії
Найзначніші діагностичні критерії вентиляційних рестриктивних розладів, які дозволяють досить надійно виявити відмінності від обструктивних дефектів:

Слід зазначити, що з діагностичних заходах рестриктивних вентиляційних розладів у чистому вигляді не можна спиратися лише зменшення ЖЕЛ. Найнадійніші діагностико-диференціальні ознаки - це відсутність трансформацій зовнішнього вигляду експіраторної ділянки кривий потік-обсяг та пропорційне зниження РОвид та РОвд.
Як діяти пацієнтові?
Якщо з'являються симптоми рестриктивної дихальної недостатності, слід звернутися до терапевта. Можливо, знадобиться консультація фахівців інших напрямів.
Лікування
Рестриктивні легеневі захворювання потребують тривалої домашньої вентиляції легень. Її завдання при цьому такі:

Найчастіше під час проведення тривалої домашньої легеневої вентиляції пацієнти при рестриктивної дихальної недостатності користуються носовими масками і портативними респіраторами (у деяких випадках застосовується трахеостома), у своїй вентиляція робиться ночами, і навіть кілька годин вдень.
Вентиляційні параметри зазвичай вибираються у стаціонарних умовах, а потім здійснюється регулярне спостереження за хворим та обслуговування фахівцями апаратури вдома. Найчастіше при проведенні тривалої легеневої вентиляції вдома пацієнтам з дихальною недостатністю хронічного характеру потрібно подання кисню з резервуарів з рідким киснем або з кисневого концентратора.
Ось ми й розглянули рестриктивний та обструктивний типи дихальної недостатності.