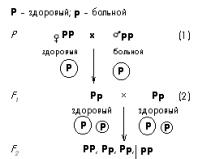
Nem specifikus és specifikus terápiás szerek komplex alkalmazása. Konkrét eszközök. Nézze meg, mit jelent a „specifikus jelentések” más szótárakban
Az aktinolizátumot specifikus gyógyszerként kell alkalmazni a maxillofacialis terület és a nyak aktinomikózisának kezelésére. Magas antigén tulajdonságokkal rendelkezik, és a legjobb eredményt nyújtja. Az immunterápia fejlesztésében és az aktinolizátumos kezelésben tapasztalattal rendelkező szerzők nem adnak javaslatot a szervezet ellenálló képességének figyelembevételére és az immunterápia előírására. Arra összpontosítunk, hogy ezeket az adatokat vegyük figyelembe az immungyógyszerekkel végzett kezelés során.
Az általános és helyi klinikai kép, az aktinolizátummal végzett immunológiai vizsgálatok adatai és egyéb laboratóriumi mutatók (a szervezet specifikus és nem specifikus reaktivitása, a szervezet általános immunológiai reaktivitása, vér- és vizeletvizsgálat stb.), a szervezet funkcionális állapota alapján. értékelik. Ennek függvényében dől el az idő kérdése, az egyéb kezelések sorrendje és az aktinolizátum kijelölése.
Az aktinomikózis komplex kezelésének, a terápiás intézkedések megválasztásának és sorrendjének szigorúan a test reaktivitási állapotától kell függnie. P. N. Veselkin (1963) és A. D. Ado (1978) megjegyzi, hogy enyhe agresszió esetén a normál reakcióképességű szervezet képes ellenállni a fertőzéseknek. Súlyosabb agresszió esetén aktív segítségre van szükség a szervezet fertőzésekkel szembeni reakciójának fokozása érdekében. A súlyos agresszió a szervezet védekezőképességének gyengülésével az adaptív reakciók legmegfelelőbb megőrzését és a szervezet toleranciájának erősítését kényszeríti ki.
Normerg típusú gyulladással jellemezhető aktinomikózis esetén a kezelés aktinolizátum adagolásával kezdődik. Ugyanakkor a nem specifikus immunitás mutatóitól és egyéb adatoktól függően komplex kezelést végeznek általános erősítő és stimuláló szerekkel, valamint bizonyos esetekben biológiailag aktív anyagokkal. Ez utóbbi a hosszú távú aktinomikózis folyamat során fellépő rezisztencia csökkenésétől függ, bizonyos esetekben - a gyulladás hipoergikus típusba való átmenetétől, ami a kezelési rend korrekcióját igényli.
Az aktinomikózisos folyamatban, amely hiperergikus típusban jelentkezik, kifejezett érzékenységgel a sugárzó gombával szemben, a kezelés általános antibakteriális terápiával, enzimterápiával és komplex infúziós terápiával kezdődik, amelynek célja a hemodinamika korrekciója, az anyagcserezavarok megszüntetése, valamint a gyulladás és a méregtelenítés szabályozása. Különös figyelmet kell fordítani a deszenzibilizáló, helyreállító és tonizáló hatású gyógyszerek felírására. A kezelési komplexumban B- és C-vitamint, kokarboxilázt és ATP-t használnak. Tüneti terápiát és az egyidejű betegségek kezelését végzik. Ebben az időszakban a sebészeti beavatkozást (a gennyes gócok feltárását) minimális szöveti trauma mellett kell elvégezni. Egy ilyen kezelés után (2-3 héttől 1-2 hónapig) egy immunológiai vizsgálat releváns adatai alapján egy aktinolizáttal végzett immunterápiát írnak elő.
Az aktinolizátum beadására adott reakció (általános állapot romlása, láz, hidegrázás, a folyamat lokális terjedése) esetén az általános terápiát addig kell folytatni, amíg a szervezet megfelelőbb reakciója meg nem jelenik. Az egyes betegekre vonatkozó javallatok szerint az infúziós oldatokban hormonális gyógyszereket - kortikoszteroidokat - kell tartalmazni. Ezután immunterápiás tanfolyamot végeznek, kombinálva az egyes szervekre és rendszerekre gyakorolt patogenetikai hatáson alapuló kezeléssel. Antigénterheléssel (prodigiosan, pyrogenal stb.) végzett kezelés nem javallt. Ezeket a gyógyszereket csak ezt követően írják fel a második, a második és a harmadik immunterápiás kúra előtt, amikor a sugárzó gomba iránti érzékenységet eltávolítják és a mérgezést csökkentik.
Ha az aktinomikózis klinikai képében helyi hiperergikus reakció alakul ki, a kezelést általános deszenzitizáló és helyi immunszuppresszív terápiával kell kezdeni: hidrokortizon szöveti injekció, immunszuppresszánsok helyi alkalmazása, és csak ezt követően írjon elő aktinolizáttal végzett immunterápiát. Általános erősítő és stimuláló gyógyszerek és antigén stimulánsok felírása nem javallt.
A hipoergikus gyulladásos reakcióval fellépő aktinomikózis folyamatot célszerű általános erősítő és stimuláló intézkedésekkel kezelni. Az antigén stimulánsokat, a hemoterápiát, a vitaminokat tüneti kezeléssel kombinálva kúraként vagy a kúra részeként alkalmazzák, és csak ezt követően írják fel az aktinolizátumot.
Az aktinomikózis anergiás típusú gyulladása általános intézkedéseket igényel, amelyek főként az egyidejű betegségek, a szervek és rendszerek rendellenességeinek kezelésére irányulnak. A javallatok szerint általános tonikokat, stimulánsokat, adaptogéneket használnak. A prodigiosan és metiluracil felírásától tartózkodni kell, de ha Ön levomisolra érzékeny, annak alkalmazása javasolt. Az általános, helyreállító és tüneti terápia, valamint a levomisol kezelés után megkezdődik az aktinolizátum terápia. Egyes betegeknél az immunogenezis korrekciója javul a glükokortikoidok, a hisztoglobin, a csecsemőmirigy-készítmények (T-aktivin) és a diucifon általános terápiába történő bevonása miatt.
Az aktinolizátumos kezelést a Suteev-módszer, a Lenin-módszer szerint vagy az utóbbi, Suteeva által módosított módszerrel végezzük.
Suteev módszere szerint az aktinolizátumot intramuszkulárisan adják be, hetente kétszer 3 ml-t; 20 injekció kúránként.
Az Asnin módszere magában foglalja az aktinolizátum intradermális bejuttatását az alkar belső felületébe hetente kétszer, összesen 25 injekciót a séma szerint: 1. injekció - 0,5 ml, 2. - 0,7 ml. 3. - 0,9 ml, a 4. injekciótól minden további adag 0,1 ml-rel növelve; a 14. injekcióra eléri a 2 ml-t és a 25. injekcióig az is marad. D. I. Lenin módszertanát A. M. Bezredka álláspontjára alapozta, aki az immuntestek intenzívebb termelésére mutatott rá az antigének intradermális beadásával. Jó eredményeket is értünk el.
A Suteeva által módosított intradermális módszerrel végzett aktinolizátum alkalmazása a következő dózisokban történik: 1. injekció - 6,3 ml, 2. - 0,5 ml mindkét alkarba, 3. - 0,5 ml három pont az alkaron, 4. - 0,5 ml az alkaron négy ponton. A 2 ml-es adag változatlan marad a kúra végéig (összesen 25 injekció).
Az APV specifikus gyógyszerként használható. Hetente kétszer intradermálisan injekciózzák az alkarba; 20-25 injekcióból álló kúrához. Az első injekcióhoz az adag 0,1 ml, a 2. injekcióhoz - 0,2 ml (két 0,1 ml-es pontban). Ezután minden injekciónál adjon hozzá 0,1 ml-t, növelve az injekciós pontok számát. A 10. injekció beadásakor a vakcina adagját 1 ml-re emelik, és ez a 20-25. injekcióig így is marad. A vakcina beadása után sűrű, sötétvörös papulák maradnak vissza, ami 4-7 nap múlva megszűnik.
A specifikus terápia első kúra során történő felépülés után, 1 hónapos szünet után, megelőző tanfolyamot végeznek, amely 15-20 aktinolizátum vagy APV injekcióból áll. Más esetekben egy hónapos szünet után egy második tanfolyamot végeznek, majd a kezelést a teljes gyógyulásig folytatják. Nem osztjuk azt a véleményt, hogy tanácsos-e az immunterápia lerövidítése 10-15 injekcióra, ahogyan azt D. I. Lenin (1956), D. I. Asnin és O. B. Minsker (1963), L. A. Makarova (1975) javasolták.
A nehezen kezelhető aktinomikózis hosszú lefolyása serkentő és helyreállító terápiás intézkedéseket igényel. Ezeket a második immunterápiás kúra előtt célszerű elvégezni.
A maxillofacialis terület aktinomikózisában szenvedő betegek kezelésében fontos feladat az optimális feltételek megteremtése a szervezetben a fertőzések elleni küzdelemben. A terápiás intézkedéseknek a szervezet általános ellenállásának növelésére kell irányulniuk, beleértve a nem specifikus védekezési tényezők növelését és korrekcióját.
A kezelés, amely magában foglalja a szervezet általános ellenállásának növelését, magában foglalja a B- és C-vitamin injekciók, az aloe kivonat és a különféle adaptogének széles körű alkalmazását. Ugyanebből a célból hemoterápiát végeznek. Széles körű tapasztalat gyűlt össze a maxillofacialis régió aktinomikózisának kezelésében. A kórházi hemoterápia vérátömlesztés formájában történik, növekvő dózisokban. Hetente egyszer, összesen 4-6 alkalommal, a következő mennyiségben: az első alkalommal - 50 ml, a második - 75 ml, a harmadik - 100 ml, a negyedik - 125 ml, az ötödik - 150 ml, a hatodik - 175 ml. Az autohemoterápiát egy klinikán minden második napon a következő séma szerint végezzük: első alkalommal - 3 ml, második alkalommal - 5 ml, harmadik alkalommal - 7 ml, negyedik - 9 ml, az ötödik - tizedik - 10 ml.
A stimuláló, helyreállító kezelés, a vitaminterápia és a hemoterápia alkalmazásának indikációja egy hosszú ideig (2 hónapig vagy tovább) tartó aktinomikózisos folyamat a gyulladás normergikus és hipoergikus típusában, valamint hiperergikus típusban annak hiányában. a test általános állapotával vagy a funkcionális zavarokkal kapcsolatos ellenjavallatokról.
Különleges helyet foglal el a szervezet nem specifikus tényezőinek szerepének növelésében a fertőzések elleni küzdelemben a biológiai stimulánsok alkalmazása. Az elmúlt években a szakirodalom felfigyelt az antigén stimulánsok jó hatására a maxillofacialis terület akut és krónikus gyulladásos folyamatainak kezelésében. Ezek a gyógyszerek képesek stimulálni a szervezet nem specifikus immunbiológiai reaktivitását. Az aktinomikózis kezelésében sikeresen alkalmaztuk a purin és piramidin sorozat gyógyszereit: pentoxil, metil-uracil, bakteriális poliszacharidok, prodigiosan és pirogenál, levomisol, T-aktivin.
A metiluracilt legfeljebb havi 10 napos ciklusokban kell felírni, naponta háromszor 0,5 mg-ot szájon át; csak 3-4 ciklus. A Pentoxylt naponta háromszor 0,2 g-ban írják fel étkezés után 10-14 napig.A Prodigiozant intramuszkulárisan háromszor adják be 25-50-75 mg dózisban, 3-4 napos időközönként. A prodigiosan injekció beadása után 2-4 órával sok beteg testhőmérséklete rövid ideig 37,5-38 °C-ra emelkedik, néha ízületi fájdalmak, rossz közérzet és fejfájás. Az állapot 12-24 órán belül normalizálódik.A Pyrogenalt a séma szerint, kúra formájában adják be.
A biológiailag aktív gyógyszerek alkalmazásával végzett komplex terápia lehetővé tette az általános állapot javulását, az aktinomikózis folyamatának aktiválását és elhatárolását, valamint az aktinomikózis gócok gyorsabb felszívódását.
A legnagyobb hatást a prodigiosan és a levomisol felírásakor érte el. A prodigiosan kezelés után az aktinomikózis lomha, lassú lefolyása aktiválódott, az aktinomikózis gócok elhatárolódnak és koncentrálódtak, majd a kelés következett. Ezt követően a gyulladásos jelenségek további oldódása és a regenerációs folyamatok serkentése volt megfigyelhető. Megállapították, hogy a prodigiosan pozitív hatással van az aktinolizátummal végzett immunterápiára.
A metiluracil és a pentoxil alkalmazásának javallata egy normerg típusú gyulladással járó aktinomikózisos folyamat, és a betegség időtartama több mint 2 hónap. A Prodigiosan az aktinomikózisos gyulladás hipoergikus típusára javallt. A Pyrogenalt hipoergiára is alkalmazni kell. Különösen jó eredményeket értek el a nyálmirigyek és a csontszövet károsodása esetén.
Az aktinomikózisos gyulladás hiperergikus típusa nem teszi lehetővé biológiailag aktív anyagok és antigén stimulánsok alkalmazását. Csak megfelelő terápia, az általános és helyi tünetek enyhülése és a normergikus gyulladásba való átmenet után javallt. Ellenkező esetben az antigén terhelés az aktinomikózis folyamatának előrehaladásához, metasztázishoz és annak generalizációjához vezethet. A lokális hiperergikus aktinomikózis reakció sem teszi lehetővé, hogy antigén stimulánsokat ajánljunk. Egyes csont- és nyirokcsomókárosodásban szenvedő betegeknél az immunogenezis korrekciója levomisol alkalmazásával érhető el. Ezen túlmenően a bőr tuberkulózisos, szubkután ínyos formák és hyperplasiás lymphadenitis esetén jó eredményeket értünk el immunszuppresszánsok lokális alkalmazásával: prosztaglandinok, spirazidin lanolinon kötszer formájában, antihisztaminok, immunszuppresszánsok, bioszupresszin alkalmazása.
Anergia esetén az antigén stimulánsokkal végzett terápia nem kívánatos, mivel a szervezet adaptív rendszereinek megzavarását, általános funkcionális zavarokat okozhat, és aktiválhatja az aktinomikózis folyamatát is. Számos anergiás állapotú beteget, hipererg típusú aktinomikózisos gyulladást, valamint néhány olyan beteget, akiknek anamnézisében számos allergiás betegség szerepel, sikeresen kezeltük hisztaglobinnal. A gyógyszer antihisztamin hatással rendelkezik, és az aktinolizátum nem befolyásolja a hisztamin rendszert.
Jó napot, kedves olvasók!Folytatjuk vitánkat az immunitás és minden ezzel kapcsolatos téma témájában. A mai cikk lehetővé teszi számunkra, hogy még jobban belemélyedjünk az emberi védőtulajdonságokkal kapcsolatos ismeretekbe. Megbízható védelemmel a biológiai testekkel vagy idegen genetikai információt hordozó anyagokkal szemben. Az immunrendszernek nevezett védekezés. Olyan fogalmak, mint pl specifikus és nem specifikus immunitás , feltárja előttünk az egészségünket őrző leukociták titkait.
Az emberi védekező rendszert a leukociták faji sokfélesége, valamint a termelődéshez és fejlődésükhöz szükséges belső reprodukálók jelentik. A számunkra fontos limfociták, makrofágok, neutrofilek és monociták a csontvelő, a lép, a nyirokcsomók és a csecsemőmirigy szöveteiből származnak.
Az egész univerzum, a makrokozmosz bennünk van. Mindezek az összetevők óvják egészségünket, minden percben átalakulnak, és egyik állapotból a másikba lépnek. Gyorsan és hatékonyan elnyomja az antigéneket, az emberi természettől idegen anyagokat. Azon immunitástípusok között, amelyek az idegen mikrobákra és baktériumokra gyakorolt hatásukat irányítják, meghatározzák nem specifikus és specifikus típusok.

Nem specifikus immunitás
Ezt a típust az antigén elleni küzdelemre tervezték, és humorális és sejtes típusokban nyilvánul meg. Az első a vérplazmában működik, és baktericid komponensek előállításával nyerik, a sejtes pedig önmagáért beszél, ezt a munkát sejtszinten végzik.
A nem specifikus immunitást veleszületettnek, specifikusnak is nevezik, képes meggátolni a testet ért külső támadásokat. Az inváziót idegennek és veszélyesnek érzékeli az ember belső rendszereire nézve.
Ez a fajta védelem úgy működik, hogy befolyásolja a különböző típusú leukociták, köztük a neutrofilek, makrofágok és bazofilek antigénjét. Ez általánosságban így van. Most egy kicsit részletesebben. Mi a nem specifikus immunitás?
Az ilyen típusú immunitás számos vírusfertőzéssel szemben ellenálló. A leendő személy, amíg az anyaméhben van, megbízhatóan el van rejtve az antigéntől, még születés után is, az örökletes immunitás hatása hat hónapig megmarad. De érdemes megjegyezni, hogy ez az időszak nem vonatkozik minden gyermekre. Itt sok múlik az anya egészségi állapotán és a gyermek által örökölt egyéni tulajdonságokon.
Itt a nem specifikus fajok kettéválnak, és két utat követnek:
- Abszolút, kifejezett érzéketlenséggel egyes vírusbaktériumokkal szemben a legkedvezőtlenebb körülmények között.
- Relatív, ami nem biztos, hogy olyan ellenálló, ha kedvezőtlen környezetet teremt a számára. Példa erre a következő eset: egy gyermek súlyosan hipotermiás volt, és meglehetősen hosszú ideig volt ilyen körülmények között, ami a bárányhimlő megbetegedésének valószínűségét jelentette. Nulla feletti hőmérsékleten a beteg megbetegedésének százaléka nulla.
Létezik a vírusokkal szembeni személyes immunitás fogalma is. Ezt az immunrendszer ereje és az endokrin indikátorok normalitása határozza meg.
Megfigyelhető bizonyos faji elfogultság és tudatlanság a fertőzésekkel kapcsolatban, amelyek betegségrezisztenciaként nyilvánulnak meg. Hasonló jelenségek a földrajzi elhelyezkedéshez is kapcsolódnak.
Például: Afrika számos régiójának lakói sokkal ellenállóbbak az olyan betegségekkel szemben, mint a malária. Ők a szó szoros értelmében „talpon vannak”, képesek elviselni a betegséget, míg egy európai magas lázzal fog feküdni, nem tud felemelkedni.
Specifikus immunitás
Ami konkrét az immunitás típusa? Genetikailag nem terjed, kialakulása egész életen át tart. Ennek is megvannak a maga alcsoportjai, amelyekből nagyjából a következőket lehet összeállítani: asztal: 
- Egy adott vagy szerzett természetes aktív típust azt követően észlelnek, hogy egy személy súlyos fertőzésen esett át. De nem csak, ha hosszú ideig szorosan érintkezik kórokozó mikrobákkal, akkor ez a forma is kialakulhat. Elég stabil. Azok, akik gyermekkorukban kanyaróban szenvedtek, nem kaphatják meg újra ezt a betegséget. A stabilitási időszak szerint ez immunitás lehet nem tartós, de évtizedekig kitart, fokozatosan veszítve erejéből. Példa a tífuszra hozható. Egyes egyéni jellemzőkkel, például az influenzával ez a forma még rövidebb távú hatást fejt ki. Ha Önnél volt ez a betegség, akkor nagy a valószínűsége annak, hogy egy bizonyos idő elteltével újra elkapja.
- Sajátos, más néven szerzett természetes passzív megjelenés. A G osztályú immunglobulin átvitelével jut be az anya méhlepényéből a baba szervezetébe. Az anyatej még erősebb támasz.
- Specifikus mesterséges hatóanyag. Mechanizmusok megjelenése a szervezetben személy, oltásokkal kapcsolatos. A védettség bizonyos idővel az oltás után jön létre, és az első pozícióban egy évtől több évig is megmaradhat. Nem lehet örökletesen továbbadni. Különösen igény van rá a pusztító jellegű tömeges fertőzésekre.
- Specifikus mesterséges passzív. Ha az immunrendszer passzív az antitestek termelésére, akkor tevékenységük során már kialakult idegen természetű fehérjék kerülnek a beteg szervezetbe. Gyakran ez a meglehetősen veszélyes eljárás anafilaxiás sokkot okoz. A stabilitás szempontjából ez a faj nem tart sokáig, legfeljebb három hétig, majd csökken.
A specifikus és a nem specifikus immunitási tényezők különböznek egymástól és a személy befolyásolásának különböző módjai. A fenti védekezési módokon kívül szervezetünknek sokkal több módja van arra, hogy ellenálljon a negatív invázióknak, amelyek kórokozó baktériumok, mikrobák és vírusfertőzések formájában jelentkeznek.
Az akadályszerkezetek elsősorban a következőket tartalmazzák:
- bőrrendszer;
- nyálkahártya;
- vérszérum.
Minden a legapróbb részletekig átgondolt, bármilyen külső támadás „visszaverhető” mechanikai, fizikai-kémiai vagy biológiai módszerekkel. Csak meglepődni és csodálni lehet, hogy testünk hogyan képes megvédeni magát.
- A mechanikai behatolásokat a bőr és a nyálkahártyák taszítják. Megvédi a rovarcsípéstől, égési sérülésektől és vágásoktól, törésektől és sérülésektől a külső sérülésektől és a szerkezetek épségének megszakadásától.
- A verejték- és faggyúmirigyek fizikai-kémiai tulajdonságai védőreakció státuszba kerülnek, a nyálkahártya-váladék pedig nem más, mint védőhatás a külső mikrobatámadásokkal szemben.
- Az immunbiológiai tulajdonságok akkor kezdenek működni, ha áttörés történik a bőrrétegen. A humorális és sejtszintű védelem azonnal aktiválódik.
Hogyan ne csodáljuk meg a cselekvések átgondoltságát és egymás belső rendszereinek és szerveinek kölcsönös segítségét. Ezt az egyedülálló világot meg kell védeni, és növelni kell belső potenciálját. Elég, ha valamelyik link meghibásodik, és a rendszer teljes integritása megsérülhet.
Vigyázz az egészségedre és dolgozz az immunitás erősítésén, mert ez a fő gazdagságod. Hosszú évekig szolgálhat hűségesen!
A fiatal haszonállatok gyomor-bélrendszeri betegségeinek kezelése az állatorvostudomány és a gyakorlat egyik nehéz problémája. A hasmenés során folyadékot veszít a széklet, amely a vérplazmához hasonló összetételű. Ez magában foglalja az elektrolitokat nátrium-, kálium- és bikarbonátionokat. Súlyos hasmenés esetén az állatok naponta 20-30-szor több folyadékot választanak ki ürülékükkel, 27-szer több nátriumiont, 17-szer több káliumiont, 37-szer több klóriont, 24-szer több kalciumot és 40-szer több magnéziumot veszítenek. A betegeknél a kiürült vizelet mennyisége csökken, illetve kiürülése leáll, a karbamidtartalom 1200 mg/l-re emelkedik, víz-, elektrolit- és energiahiány lép fel. A székletben a glükóztartalom 4-szeresére, a fehérje 2-szeresére nő. A takarmány emészthetősége csökken, a szervezet nem kapja meg a szükséges tápanyagokat, vitaminokat, makro- és mikroelemeket.
A fiatal állatok gyomor-bélrendszeri fertőzései széles körben elterjedtek, és jelentős károkat okoznak az állattenyésztésben. Összetett etiológiai felépítésük és a patogenetikai kapcsolatok sokfélesége a kóros folyamatba bevonja az összes testrendszert, és csak átfogó terápiás és megelőző beavatkozást igényel. E rendelkezés végrehajtása a terápia összes módszerén alapul: etiotróp - a betegség kórokozója elleni küzdelem; patogenetikai - célja a patogenetikai lánc láncszemeinek megszüntetése, a szervezet önszabályozásának helyreállítása, a védekezés mobilizálása és stimulálása; helyettesítés - a hiányzó anyagok bevitelére és pótlására irányul a szervezetben, amelyek egy kóros folyamat kialakulása miatt elvesztek; neurotróf funkciókat szabályozó és tüneti, a betegség tüneteinek megszüntetését célzó. A komplex kezelés és a megelőző beavatkozás is a terápia összes elvének végrehajtásán alapul (lásd „A fiatal állatok légúti fertőző patológiáinak komplex kezelésének általános elvei”). A terápia aktív, fiziológiás és komplex elvei alapozzák meg a gyomor-bélrendszeri fertőzések állatorvosi intézkedéseinek hatékonyságát.
A bélfertőzésben szenvedő fiatal állatok kezelését etiotróp (a kórokozó és toxinjainak inaktiválása, a betegség kapcsolódó tényezőinek megszüntetése) és patogenetikai (a beteg test kiszáradása elleni küzdelem, toxikózis, az emésztési folyamatok normalizálása) egyidejű alkalmazásával kell kezdeni. a terápia.
A kórokozók elleni küzdelem a terápiás intézkedések során specifikus és nem specifikus eszközökkel történik, amelyeket a betegségek leírásánál részletesen ismertetünk. A hasmenés szindrómával járó bélfertőzések kapcsán azonban meg kell jegyezni, hogy a specifikus hiperimmun szérumok és globulinok kevésbé hatékonyak. Ez annak a ténynek köszönhető, hogy a fertőző ágens túlnyomórészt a gyomor-bél traktus lumenében vagy nyálkahártyáján lokalizálódik, azaz a legtöbb antitest és immunglobulin nehezen hozzáférhető.
A bakteriális gyomor-bélrendszeri betegségek specifikus kezelésének eszközei közül a kóros folyamat bármely fejlődési szakaszában a nagy aktivitású specifikus bakteriofágok a leghatékonyabbak. Használatuk ártalmatlan, nem okoz szövődményeket, nem befolyásolja a normál bélmikroflóra biocenózisát, környezetbarát (nem szennyezi a környezetet, nem von maga után vágási korlátozást). Sőt, ma már csak fágkészítmények használatával lehet megszüntetni a baktériumok hordozását és hatékonyan fertőtleníteni a szervezetet a kórokozótól.
Mono- és polivalens bakteriofágokat fejlesztettek ki és alkalmaztak Escherichiosis, Salmonellosis, Klebsiellosis, Pseudomonas, Proteus és más bakteriális fertőzések ellen. Alkalmazásuk a kórokozó fággal szembeni érzékenységének meghatározása után a leghatékonyabb, amelyet egy egyszerű módszerrel végeznek, amikor a bakteriofágot újonnan vetett gyepen oltják be a kórokozó húsleves kultúrájával. A vizsgált fág negatív növekedési zónáinak jelenléte a baktériumokban 18-20 órás, 35-36 °C-os tenyésztést követően pozitív eredményt jelez, és lehetővé teszi ennek a gyógyszernek a használatát a megfelelő bélbakteriózis esetén. hatás (mérsékelt) vagy lítikus hatás nélkül elősegíti a létfontosságú aktivitás aktiválását és a bakteriális ágens toxintermelését, valamint a kórokozó fágrezisztens törzseinek mutagenezisét és felhalmozódását.
Ha az etiológia nem teljesen tisztázott, komplex gyógyszert javasoltak - polifágot fiatal állatok akut bélbetegségei ellen, beleértve az Escherichia, Proteus, staphylococcus, Klebsiella és pseudomonas bakteriofágokat. Alkalmazása különösen indokolt vírusos betegségek miatti dysbiosis kialakulása esetén a belekben.
Mivel a bakteriofágok savas környezetben elvesztik aktivitásukat, a gyógyszer beadása előtt az állatoknak 3-5%-os, forralt vízben készült nátrium-hidrogén-karbonát-oldatot adnak 1-2 ml/kg mennyiségben. A kezelés kezdetén a bakteriofágot 3 napon keresztül 3-6 alkalommal 3 óránként alkalmazzák; Ha a bakteriofágot szülés utáni fiatal állatoknak adják, akkor a kolosztrum fele mennyiséget kapják.
Az etiotróp kezelés eszközei közül érdemes megemlíteni egy olyan gyógyszert, amely az E. coli - coliprotectan VIEV - által termelt antibiotikum-szerű kolicin.
Az antibiotikumok, szulfonamidok, nitrofuránok és egyéb kemoterápiás szerek alkalmazása hozzájárul a kórokozó gyors inaktiválásához és a szervezet állapotának javulásához. Bélfertőzések esetén a gyomor-bél traktusban domináns hatású antibakteriális szerek szájon át történő alkalmazása hatékony. A gyógyszert a végbélből származó mikroorganizmusok patogén izolátumának és az elhullott állatok kóros anyagának antibiotikumokra és szulfonamid gyógyszerekre való érzékenységének előzetes meghatározása után kell kiválasztani. Erre a célra szabványos lemezes és hígítási módszereket alkalmaznak (lásd „A légúti fertőző betegségek komplex kezelésének általános elvei”).
Egy új gyógyszer, a glükofur-komplex gyógyszer, kifejezett antibakteriális hatással rendelkezik. Az anolit – a természetes víz anódnál történő elektrolízise során nyert savas víz – baktericid és gombaölő hatású. 10 ml/ttkg adagban alkalmazzák kolosztrum (tej) helyett félig éhező diéta során.
Emlékeztetni kell arra, hogy az antibiotikumok alkalmazása nem szünteti meg a baktériumok hordozását, és általános diszbakteriózishoz vezet, mivel a gyógyszer aktív komponense romboló hatással van mind a patogén, mind a szaprofita (úgynevezett opportunista) mikroflóra, valamint a jótékony lakto-, bifidobaktériumokra, propionsav és más baktériumok. A megüresedett biológiai rést (bélüreget) gyorsan megtelepítik élesztőgombák, enterobaktériumok és más szaprofiták, amelyek gyakran gyenge antibiotikum-érzékenységgel és többszörös antibiotikum-rezisztenciával rendelkeznek.
Ezért az antibiotikum használat megkezdése után 2-3 nappal párhuzamosan probiotikus készítmények szájon át történő alkalmazása szükséges. A probiotikumok olyan biológiai készítmények, amelyek szimbionta mikroorganizmusok stabilizált kultúrái vagy fermentációs termékeik, amelyek elősegítik az utóbbi növekedését. Használatuk pozitív hatása annak köszönhető, hogy részt vesznek a gazdaszervezet emésztési és anyagcsere folyamataiban, a fehérje és sok más biológiailag aktív anyag bioszintézisében és felszívódásában, valamint biztosítják a bél kolonizációs rezisztenciáját. A probiotikumok abban különböznek az antibiotikumoktól, hogy nincsenek mellékhatásaik, nem halmozódnak fel a szervekben és szövetekben, és nem okoznak függőséget a patogén mikroflórától.
A probiotikus készítmények alkalmazása a vírusos enterocolitis korai szakaszában is javasolt. A vírusos ágensek megzavarhatják a bél mikrobiocenózisát, mivel a vírusfehérjék az enterocita külső membránjába integrálódva hozzájárulnak az atipikus receptorok vagy receptormezők kialakulásához, amelyekhez a korábban szokatlan tapadással rendelkező baktériumok intenzíven kötődni kezdenek: staphylococcusok, Proteus, élesztőgombák. mint a baktériumok és mások, amelyek diszbiózist indítanak el.
Megfigyelték a probiotikumok regeneráló hatását a bélnyálkahártya különböző struktúráira. Immunmodulátorokkal együtt történő alkalmazásukat követően a duodenumban helyreálltak a nyálka és a baktericid lizozim enzim termeléséért felelős serlegsejtek, a nyálkahártya morfológiája és funkciói, a vérellátás, az enzimatikus és szekréciós aktivitás a jejunumban, valamint a nyálkahártya morfológiája. bolyhok és kripták az ileumban. A probiotikumok segítenek normalizálni az állati vérszérum biokémiai paramétereit, helyreállítani a kalcium-foszfor arányt és csökkentik az alkalikus foszfatáz aktivitását. A legyengült állatokban - a T-limfociták számának növekedése és a neutrofilek fagocita aktivitása.
A fiatal állatok gyomor-bélrendszeri megbetegedései szisztémás és polietiológiai jellegűek. Emiatt a probiotikumok nem működhetnek önálló kezelési eszközökként, hanem a terápiás intézkedések átfogó komplexumának fontos részének, valamint az antibiotikumok természetes alternatívájának tekintendők, lehetővé téve a gasztrointesztinális betegségek előfordulásának csökkentését fiatal állatoknál. valamint az állati eredetű termékek élelmiszer-eredetű toxikus fertőzések kórokozóival való szennyeződésének kockázata. A probiotikus készítmények alkalmazása tejjel, kolosztrummal, vízzel és takarmányokkal lehetséges. Használatuk minden etetés előtt 10-15 perccel javasolt.
Számos probiotikumot regisztráltak és alkalmaztak pozitív hatással fiatal haszonállatok gyomor-bélrendszeri betegségeinek kezelésére és megelőzésére. A főbbek (a bakteriális komponens összetétele zárójelben van feltüntetve):
ABA (Lactobacillus acidophilus);
alinsav (L. acidophilus, Saccaromyces cerevisiae élesztőkivonat);
bactoneotime (L. acidophilus, Str. faecium, Bifidobacterium adolescentis, Bif. globosum);
bioplus C (Bacillus subtilis, Bacillus licheniformis);
biosan (L. delbrueckii, L. buchneri);
biosporin (Bac. subtilis, Bac. licheniformis);
bifacevdobacterin (laktobifadol) (L. acidophilus, Bif. adolescentis);
bifidumbacterin (Bif. adolescentis, Bif. bifidum, Bif. longum);
bifinorm (Bif. adolescentis);
bifitrilak (L. acidophilus, Bif. bifidum, L. bulgaricus, L. fermentum);
vetom-1,1; vetom-2; vetom-4 (Vas. subtilis);
homoprobiotikus baktériumkészítmény (L. acidophilus);
kovász Saratovskaya-3 (Saccaromyces cerevisiae, L. buchneri);
immunobak (L. acidophilus, Str. faecium, Bif. adolescentis, Bif. globosum);
intestevite (Bacillus ssp., Bif. globosum, Str. faecium);
kombinált probiotikus készítmény (E. coli M-17 p74, Bac. firmus - CK);
lakk (L. acidophilus, P. shermanii, Str. faecium, Str. diacetylactis);
tejsavölő (L. acidophilus, L. fermentum, Str. faecium);
laktoamilovorin (L. amylovorus);
PP (probiotikus termék) (Str. bovis, L. gallinarum);
probiotikus készítmény tőled. subtilis, Bif. bifidum, E. coli;
prodigest (kérődzők bendőkivonata);
realak (L. acidophilus, L. fermentum, Bif. globosum, a Saccaromyces cerevisiae élesztő autolizátuma);
Romakol (E. coli M-17);
Savit (Saccaromyces cerevisiae, Str. faecium);
SBA (Bif. adolescentis, Bif. bifidum, L. acidophilus, Str. faecium);
sgol (L. acidophilus);
sporobacterin (Bac. subtilis 534);
sporovit (Bas. subtilis, Vas. licheniformis);
streptobifid (Bif. globosum, Str. faecium);
streptoecolact (Str. lactis);
szubalin (Bac. subtilis);
fagozán (L. acidophilus, Str. faecium);
fitobakterin (Ruminococcus abus);
cellobacterin (Ruminococcus abus).
A probiotikus készítmények is elterjedtek: biod-5; bifitrilak; laktobifadol; dakticin; bifi-dum-SHJ; aciptol; colibacterin; ICD; bifidin; UDS; enterobakterin-2; streptobifid-forte; laktoferon; okarína; laktobakterin CTX-1; biosporin V, ALIFT-P; STF-32; propiocid; Acid Lac Way (USA); prodigest (Szlovénia); bioplus S (Németország); Colby-Milch (Németország); Omnifiora (Franciaország) stb.
A hasmenéssel járó gyomor-bélrendszeri betegségek etiotróp terápiájával párhuzamosan pihenési feltételeket kell teremteni, javítani kell az állathigiéniát, csökkenti az emésztőrendszer terhelését, amit félig éhező diétával érnek el. Ebben az esetben az egyik etetés kimarad (tej vagy kolosztrum ivása), a másodikban - elektrolit oldatot adnak (esetleg antiszeptikus oldatokkal, például 1% -os dioxidin oldattal 1-2 cm 3 / kg arányban). ), a harmadikban - 25%-os tej és 75%-os elektrolitoldat, a következő ivásnál - egyenlő térfogatú tej és elektrolitoldat, majd - tej túlsúlynál (75%) és a következő ivásnál áttérnek teljes etetés.
A kazeinobezoár betegség megelőzése, valamint az etetési rend és technológia megsértésének megszüntetése érdekében a borjakat a 3-4. etetéstől kezdődően és 3-4 napig etetik 1: 1 arányban meleg nátrium-kloriddal hígított kolosztrummal. megoldás. A kolosztrumnak ez a nátrium- és klórionokkal való dúsítása megakadályozza a sűrű, gumiszerű kazeinrögök kialakulását.
Ugyanezen célokra hatékony kombinálószereket használni - olyan gyógyszereket, amelyek megakadályozzák a kazeinrögök képződését az oltóanyagban, és hozzájárulnak azok megsemmisítéséhez. A startin, a camicel, a peocel, a combiter KA-32/60, valamint a kalcium-peroxid (cocox) aktív hatása a borjúcsirkék mirigygyomrából származó aktív készítmény, a laktolizátum és a spellakt diétás termékek, amelyek emellett normalizálják ásványianyag-anyagcsere és csökkenti a kiszáradást, megállapították, és töltse fel a szervezetet könnyen emészthető fehérjékkel és szénhidrátokkal.
Az elektrolit oldatok bevezetése egyidejűleg biztosítja a kiszáradás elleni küzdelmet, amely elválaszthatatlanul kíséri a drasztikus hatású patológiákat. Vízhajtókkal együtt történő alkalmazásuk biztosítja a méreganyagok kijutását is a beteg szervezetből.
A kiszáradás és a toxikózis súlyos tünetei esetén ezen oldatok intravénás, intraperitoneális vagy szubkután infúziója javasolt. A hivatalos elektrolit oldatok közül a leggyakoribb a dyspepsia, a rehydraltan (V. V. Mityushin szerint), a hlosol, a lers (K szerint). Ya. Dolnikov), Ringer-, Ringer-Locke-oldatok, dizol, vetglukozalan, kolinát, re-hidropektán, glükofuracid, vetseptol.
Hatékony a recept szerint elkészített glükóz-só oldat használata: 1 liter vízhez: 4 g nátrium-klorid, 1 g kálium-klorid, 20 g glükóz. Forrásban lévő vízfürdőben 30 percig végzett sterilizálás után 2,5 g szódát, 1 g novokaint és egy antibakteriális gyógyszert (500 000 egység sztreptomicint vagy neomicint) adunk az oldathoz. Borjúnként 100-200 ml-t írjon fel 1-2 naponta egyszer.
Glükóz-citrát oldatot készítünk a recept szerint: 1 liter vízhez: 8,5 g nátrium-klorid, 4,5 g nátrium-citrát és 20 g glükóz. Adagok - 400 ml-ig fiatal szarvasmarhák vagy lovak számára, legfeljebb 150 ml - bárányok, gidák.
Használható 50 g nátrium-karbonát, 420 g nátrium-hidrogén-karbonát, 20 g kálium-klorid és 100 g nátrium-klorid keveréke 1 liter vízhez, valamint izotóniás nátrium-klorid-oldat (sóoldat), 2- 3% nátrium-acetát, vagy 6,5 g só és 4,5 g szóda keveréke 1 liter vízben.
Az antitoxikus hatást elektrolit és glükóz oldatok hexaminnal (0,5 cm 3 40%-os oldat 1 kg állati tömegre vonatkoztatva), furoszemiddel, erdei fenyőtűk főzeteivel, csikóslábfélékkel, réti lóhere fejével, polpollal, kamilla hozzáadásával biztosítják. ., petrezselyem gyűjteményekben és más diuretikumokban, valamint aszkorbinsav parenterális adagolása 1000 mg-os dózisban; komplex készítmények nátrium-nukleináttal; vitamin-aminosav-mikroelem komponens - gamavit, aminonovit (0,2-0,7 cm 3 /kg naponta 1 alkalommal); szgol orális adagolása -0,5-1 g/kg szarvasmarhának, 4 g/kg sertésnek; enteroszorbensek.
Az enteroszorbensek megkötik a toxikus bomlástermékeket, aluloxidált termékeket, felhalmozódott gázokat, baktériumokat a bélüregben, csökkentve a gyomor-bél traktus nyálkahártyájának terhelését, valamint a toxigén folyamatokat. Ezek általában higroszkópos porok vagy tabletták, amelyek átlagos orális dózisa 0,5-1,5 g/kg állattömeg: aktív szén, zooszorb, lignin, hidroxál, szorbex, polifepán, poliszorb, zoo-carb, pektoszorbit, florceol B , EST-1, lipamid, pektoszorbit, hesplen, hepatocel, hepatovit, szaponin, mikroszorb-P, cydineg, enterozim, mexidol, biogél 5, poliszorb VP, anolit, katolit, biogél 5, tsesseidin, florzeol B.
A bélnyálkahártya túlzott irritációja és a hasmenés, mint patogenetikai kapcsolat megszüntetése burkoló és összehúzó szerek alkalmazásával érhető el. Bevonóként naponta 2-3 alkalommal 10-12 ml/kg állattömeg 1-5%-os rizsfőzet pasztát, keményítőfőzetet, 1:30 arányú lenmagfőzetet igyunk; 5-8 ml/kg 1:10 arányú elecampane, ökörfarkkóró virágok, pöttyös pinty, izlandi moha, mályvavirágok és levelek főzetéből.
Az összehúzó szerek csoportjába tartoznak a gyógynövények főzetei és infúziói: 1:10 arányú főzetek tölgyfa kéregből, kígyózó rizómából, cincér rizómából, égető gyökérből és rizómából, zsályalevélből; infúziók 1:10 kamillavirágból, infúziók 1:20 szürke éger gyümölcsből, lósóskafű, orbáncfű, borsmenta; Nyírfa chaga gomba kivonat (befungin) 1%-os oldata, stb. 5-10 ml/ttkg adagban használják. A kollekciókban összehúzó és gyulladáscsökkentő, vizelethajtó és általános serkentő hatású összetevőket kombinálhat.
Példák a hasmenés elleni díjra:
1) 1 liter vízhez: kamillavirág - 10 g, orbáncfű gyógynövény - 20, réti lóhere virága - 10, pitypang gyökere - 20 g;
2) 1 liter vízhez: tölgy kéreg - dél, zsurlófű - 20, éger kúp (zúzott) - 10, eperlevél - 10, lósóska - dél.
A lefőzött keveréket 4-8 ml/kg arányban 3-4 alkalommal naponta 20-30 perccel etetés előtt itassuk meg.
Termelési körülmények között a legegyszerűbb összehúzó szer a szénafőzet (1 kg vödör vízre), 500 ml borjúnként naponta 3-4 alkalommal.
Az enterocolitisben a fiatal állatok nemcsak sok vizet és elektrolitot veszítenek. Az étvágytalanság és az élelmiszerek alacsony emészthetősége a vitaminok és az emésztőenzimek észrevehető hiányához vezet, és a bélbetegség patogenetikai folyamata magában foglalja a hipovitaminózis reakcióit, az emésztőmirigyek és a máj szekréciós hiányát. Ebben a tekintetben a fiatal állatok fertőző gyomor-bélrendszeri betegségeinek komplex kezelésében enzimpótlást és vitaminterápiát kell alkalmazni.
Enzimanyagként a pepszint (1%-os oldat 0,5%-os sósavoldattal) szájon át 15 perccel a kolosztrum fogyasztása előtt alkalmazzák 5-Yug/kg állati tömegben, természetes gyomornedv 30-50 cm 3, mesterséges gyomornedv - 80 -100 cm 3 borjúfejenként. A pankreatint szájon át, tripszint és abomint tartalmazó kapszulákban, 2-5 mg/kg állati testtömeg-kg dózisban írják fel, és egyéni előírás szerint az enteropharm, hemolizátumot 15 perccel a takarmányozás előtt alkalmazzák, különösen az élet első napjaiban, mivel valamint a gastrovetin, a pancreavetin.
A vitaminkészítmények közül elsősorban az A, D, E csoportot használják, monogasztrikusnál a B b B 2, B 6, PP vitaminokat is. Emlékeztetni kell arra, hogy a Bt- és B6-vitaminok egyidejű beadása esetén a szervezetben foszforilálva antagonista viszonyba lépnek, ami csökkenti a biológiai formákká való átalakulásuk lehetőségét. A C-, PP-, K- és B12-vitamin fokozza a vér alvadási képességét, ami fokozott vérviszkozitás (dehidratációs szindróma) mellett veszélyes szívelégtelenség és thromboemboliás folyamatok kialakulására. Ez utóbbi valószínűsége nő a penicillinnel és származékaival végzett egyidejű antibiotikum-terápia esetén. A vitaminkészítmények gyulladt bélben való csekély felszívódása miatt parenterális alkalmazása javasolt.
Alkalmaz:
intramuszkuláris A-vitamin koncentrátum vagy retinol-acetát olajos oldata (ezer NE naponta fejenként): korai tejes borjak 15-40, késői tejes borjak és csikók 3 hónapos kortól 40-70, bárányok 2,5-10, malacok 2,5-4 ;
intramuszkulárisan Caroline malacok, tejelő borjak termesztésére 5-10 cm 3 fejenként 3 alkalommal 5 napos időközzel;
0,2%-os olajos béta-karotin oldat 0,2 cm 3 /testtömeg-kg borjak és 1,3 cm 3 /kg takarmány adagok malacok számára takarmánykeverékek részeként;
intramuszkuláris D 2-vitamin koncentrátum - 20 000-30 000 fejenként;
intramuszkuláris E-szelén - 0,5 cm 3 /10 kg;
intramuszkulárisan vagy szubkután naponta egyszer trivit (A, D 3, E) és tetravit (A, D 3, E és F): nagy állatok fiatal állatai számára - 5-7 cm 3; malacok, bárányok, gidák - 1,5; nyulak - 0,3 cm 3;
ursovit (A, D 3, E, C) szubkután olajos oldata: csikók és borjak - 2,5 cm 3; malacok, bárányok, gidák számára - 1-2 cm 3;
intramuszkulárisan 1 alkalommal 2-3 naponta aminovit (A, D 3, E, C, Bi, B 2, B 6, PP, K 3, N stb.) 5 kg-ig terjedő állatoknak - 1,0-1,5 cm 3 ; 20 kg-ig - 3, 40 kg-ig - 6, 9-10 cm 3 felett;
intramuszkulárisan vagy szubkután eleovit (A, D 3, E, K 3, Bt, B?, B 5, B 6, B c, B ]2, N) (1 állatonként): csikók, borjak - 2-3 cm 3 ; bárányok - 1, malacok - 1-1,5 cm 3;
szubkután vagy intramuszkulárisan multivitamin (A, D 3, E, B b 2, B 5, Bb, B 12 stb.) 2 cm 3 /50 kg súlyú adagban nagytestű állatoknak, 1 cm 3 /10 kg súly kis állatoknak stb.
Mint már említettük, a bélfertőzéseket gyakran szaprofita és gyengén virulens baktériumok, pantropikus koronavírusok és rotavírusok, adenovírusok és egyéb kórokozók okozzák a szervezet immunhiányos állapotának hátterében, amelyet ipari stressz, táplálkozási hiányosság vagy egyensúlyhiány, valamint a technológia megsértése okoz. posztnatális állatok kolosztrum etetésére. Ezt a körülményt különböző szerzők tanulmányai jelzik, akik megjegyzik, hogy a borjakban a hasmenés tünetegyüttesével járó megbetegedések az immunológiailag aktív fehérjék alacsony szintje – a vérszérum immunglobulinjai, a T- és B-vitaminok alacsony száma – hátterében fordulnak elő. limfociták és a neutrofilek fagocita aktivitása. Ez indokolja az immunmodulátorok alkalmazásának népszerűségét fiatal állatok bélfertőzéseinek kezelésére. Spektrumuk és potenciáljuk igen széles: ligfol, timogén, timalin, thym-regivit, timogar és timozin at, T-aktivin, B-aktivin, quacyclin, izokvaterin, hisztoeroglobin, gangliin, zeofract, argequin, sodakhist vestin és annak módosulatai, , immunofan, polyentered, STEMB, xymedon, milon, vitulin C, ribav, rodest, ASD 2. frakció, dostim, mastim, polioxidónium, foszprenil, propolisz, enterofar allogén vérszérummal és ferroglucinnal, ozonált nátrium-klorid, komplex immunoprobiotikum készítmények interferonnal - baktoferon, laktoferon, immunobak, bactoneotime, valamint neoferon, leukinferon és még sokan mások. Egyes vírusfertőzésekben, amelyekben a makrofágok a vírus replikációjának helyei lehetnek (vírusos hasmenés, adenovírus fertőzés), az immunmodulátorokat - monocita stimulánsokat - óvatosan kell alkalmazni.
Súlyos toxikózis és fokozott vérviszkozitás esetén szívműködést támogató gyógyszerek felírása szükséges: intramuszkulárisan szulfokamfokain, cordiamin vagy szubkután kámfor 20%-os olajos oldata 0,05 cm 3 /kg dózisban; intramuszkuláris kokarboxiláz 1 mg/kg/nap sebességgel.
A szervezet biotonuszának fenntartásához citráttartalmú anyavér intramuszkuláris alkalmazása 0,5 cm 3 /kg dózisban minden második napon hatékony; hidrolizin L-103 vagy amilopeptid-2 - 1,5-2 cm 3 /kg naponta kétszer; poliglobulinok vagy gamma-globulinok a betegség első napján, majd 4-5 nap múlva ismét, tioglobulin - 0,7 cm 3 /kg 24 óránként a gyógyulásig. Nem kevésbé fontos a hepatoprotektorok felírása: dipromónium - 10 mg/kg; lipamid - 0,25-1 mg / kg; sirepara - 0,1 cm 3 /kg; valamint tsidinega, hepatocel, hepatosan, metovit, toksovit, essentiale, pumpkinol.
A szervezet biotonusának fenntartásához ligo-virint, magzati szövetkészítményt „suifet”, szelenopirint, lenton TM-et, erakondot, reamberint, limontart, hemovit-plus-t, conferont, vitalacidot, ribav, diarin, gamavit, gastrovetint, trikaptolt is alkalmaznak. , 2,5%-os múmiaoldat, oxihumát, Dorogov-stimulátor, koponyán keresztüli elektromos stimuláció (TCES), ximedon, tehén placentából származó biostimulátor, milon, 5%-os vizes-alkoholos propolisz emulzió (VSEP), valamint homeopátiás szerek: Rulsatilla, Nux -Vomica, Argentum nitricum.
Megállapították az ózonpunkció kifejezett hatékonyságát a természetes rezisztencia humorális és celluláris tényezőire és az újszülöttek életképességére, az ózon immunmoduláló és fertőzésellenes hatását parenterális adagolás esetén, valamint a reflexológia (farmako- és lézerpunkció) stimuláló hatását. .
Az ózonterápia alkalmazási köre az ózonnak a szövetekben történő oxigénszállítást és -felszabadulást befolyásoló tulajdonságai miatt meglehetősen széles. Jelenleg vannak olyan kísérleti és klinikai anyagok, amelyek az ózon immunmoduláló, gyulladáscsökkentő, baktericid és egyéb tulajdonságait jelzik. Az immunmoduláló hatás a citokinek limfociták és monociták - interferon, interleukinok - szintézisének aktiválásával jár, amelyek aktiválják mind a sejtes, mind a humorális immunitást. Az ózon antibakteriális hatása a szabad gyökök fokozott hatásával és a leukociták megnövekedett fagocita aktivitásával, a vírusellenes hatás pedig a membrán polipeptidláncainak károsodásával, ami megakadályozza a vírusok sejtekhez való kötődését. Ezenkívül az RNS egyik szála két részre hasad, ami megzavarja a vírus replikációjának folyamatát. A vírus behatolása elleni védelmet az interferon szintézise is biztosítja.
A kolosztrum ózonozása növeli az immunglobulinok adszorpciós kapacitását az újszülöttek beleiben. Az ózonozott nátrium-klorid oldatok parenterális beadása a borjaknak serkenti az immunrendszer különböző részeinek funkcionális aktivitását, és biztosítja az állatok nagy biztonságát.
A nem hagyományos terápiás módszerek közül az utóbbi években alkalmazták a reflexológiát, amely a reflex – az idegi aktivitás leguniverzálisabb mechanizmusa – elvén alapul. A reflexológia kiegészítheti vagy helyettesítheti a gyógyszeres terápiákat. Ebben az esetben a biológiailag aktív pontokba 0,5% -os novokain oldatot fecskendeznek, vagy lézert alkalmaznak rájuk. A farmako- és lézerpunkció elősegíti az állatok természetes rezisztenciájának humorális és celluláris faktorainak növelését. Megállapítást nyert, hogy az ilyen módszereknek kitett tehenekből nyert borjakban a gyomor-bélrendszeri betegségek ritkábban fordultak elő, a biztonság 100% volt. A kontaktszkennelés módszerével a kérődzőket lézersugárral kezelik az éhes üreg területén, a hasfal ventrális részén bal és jobb oldalon a vékonybél bőrén lévő projekciós területen, valamint a kétoldali ágyéki és keresztcsont paravertebralis dorzális vonalának biológiailag aktív pontjain.
Emésztőrendszeri fertőzések esetén oxigénterápia és helyi fűtés is javallt. A neurotróf funkciókat szabályozó terápiaként javasolták a Mosin szerinti mellhártya feletti blokádot vagy a Gerov szerinti visceralis blokádot.
A lenton gyógyszert használják. Tartalmaz ampicillint, analgint, acetilszalicilsavat, nátrium-kloridot, cukrot, mézet, csikósláblevél- és teakivonatot, desztillált vizet. Ennek a gyógyszernek a példáján látható a terápia szisztematikus megközelítésének tendenciája. Komplex hatását a gyomor szekréciós és motoros evakuációs funkcióinak normalizálása jellemzi; a patogén mikroflóra elnyomása; a gasztrointesztinális nyálkahártya védőreakciójának erősítése az agresszív anyagokkal szemben; gyulladáscsökkentő és mérsékelt immunstimuláló hatás. A lenton használatával gyors és magas terápiás hatás érhető el: az akut bélfertőzésekből való felépülés a betegség súlyosságától függően 3-6 napon belül megtörténik.
Az új generációs módosított természetes adaptogén ligfol (olipifát) természetes (fa) lignin, nátrium-pirofoszfát-dekahidrát, nátrium-klorid és pirogénmentes víz hidrolíziséből nyert humuszanyagokat tartalmaz. A Ligfol megakadályozza a stressz-szindróma negatív hatásait, a maladaptív reakciók előfordulását, felgyorsítja a proliferációs folyamatokat a bőrön, a nyálkahártyákon, az izmokon és a parenchymás szerveken. Hatékony hepatoprotektor, erős antioxidáns, immunmodulátor, különösen az immunitás celluláris komponensének patológiás fókuszában, a vérképzés stimulátora, a szervezet általános nem specifikus stimulátora és daganatellenes aktivitással rendelkezik.
A ligfol intramuszkuláris alkalmazása vemhes teheneknél 5 cm 3 adagban 7-10 nappal az ellés előtt és az ellés napján lehetővé tette a születési és ellés utáni megbetegedések számának csökkentését, valamint hozzájárult az életképesebb utódok születéséhez. valamint az újszülött borjak gyomor-bélrendszeri megbetegedésének gyakoriságának csökkenése. A létfontosságú tevékenység serkentésére, a stressz korrekciójára és a jobb alkalmazkodásra a ligfolt 1-1,5 cm 3 dózisban adják be a borjaknak az egyik korcsoportból a másikba való áthelyezés előtti napon. A ligfol egyszeri, 5 cm 3 dózisban történő alkalmazása a kocáknál a vemhesség 97. napján segít növelni az „üzleti” malacok hozamát (10 kocánként akár 4,5-5) és csökkenti a mortalitást.
UDC 619:616-092:636.52/58 E.G. Turitsyna, N.V. Donkova
KÜLÖNLEGES ÉS NEM SPECIFIKUS MEGELŐZŐ ESZKÖZÖK INTEGRÁLT ALKALMAZÁSÁNAK PROBLÉMÁI IPARI BAROMFI Tenyésztésben
Tanulmányozták a Krasznojarszk Területen található baromfitelepeken meglévő immunizálási programokat, kezelési és megelőző intézkedések rendszereit; retrospektív elemzést végeztünk a csirkepusztulás szerkezetéről; homeosztatikus és immunológiailag alátámasztott szervek és szövetek citomorfológiai vizsgálata történt. Vizsgálták a baromfitermékekben található gyógyászati szennyeződések maradék mennyiségét.
Kulcsszavak: baromfitenyésztés, vakcinázás, terápiás és profilaktikus kezelés, mortalitási szerkezet, citomorfológia, gyógyászati szennyeződések.
Ye.G. Turitsyna, N.V. Donkova
A KÜLÖNLEGES ÉS NEM SPECIFIKUS MEGELŐZÉSI ESZKÖZÖK ALKALMAZÁSÁNAK KÉRDÉSEI AZ IPARI BAROMFITenyésztésben
A Krasznojarszk régióban működő baromfitelepeken tanulmányozzák a meglévő immunizálási programokat, valamint kezelési és profilaktikus cselekvési programokat; elvégzik a csirkeveszteség szerkezetének retrospektív elemzését; megadjuk a testek és szövetek citomorfológiai becslését a homeosztatikus és immunológiai ellátáshoz. Kutatják a baromfitenyésztési termelésben előforduló gyógyászati szennyező anyagok maradék mennyiségét.
Kulcsszavak: baromfitenyésztés, vakcinázás, kezelés és profilaktikus feldolgozás, veszteségszerkezet, citomorfológia, gyógyászati szennyeződések.
Az ipari baromfitenyésztésben a madárpopuláció magas termelékenységét és biztonságát az állat-egészségügyi intézkedések komplexuma biztosítja, amelyek között a fertőző betegségek specifikus és nem specifikus megelőzése fontos helyet foglal el. A speciális megelőzés a baromfi univerzális vakcinázásából áll, amely aktiválja az immunrendszer képességeit és biztosítja a patogén mikroorganizmusok hatásaival szembeni ellenállást. A nem specifikus profilaktikus szerek növelik a baromfi természetes ellenálló képességét, és számos antimikrobiális tulajdonsággal rendelkeznek.
A fertőző betegségek specifikus megelőzésére irányuló átfogó programok biztosítják az antigén összetétel ismételt és változatos stimulálását annak érdekében, hogy a vakcinázott állatállományban specifikus antitestek képződjenek, amelyek szükség esetén megvédhetik a madarat a fertőzéstől. A számos immunizálás hátterében gyakran előfordulnak különböző etiológiájú és súlyosságú oltás utáni szövődmények, amelyek a klinikai állapot romlásával, sőt a beoltott populáció egy részének halálával járnak. Emellett az ipari vállalkozások körülményei között az egyedfejlődés rövid időszaka alatt a baromfi különféle nem specifikus, elsősorban antibakteriális profilaktikus szerek hatásának van kitéve, ami gyakran okoz kimutatást az élelmiszer-alapanyagokban és a baromfi élelmiszertermékekben.
A munka célja azoknak a problémáknak a tanulmányozása és elemzése volt, amelyek a specifikus és nem specifikus prevenciós eszközök komplex alkalmazása hátterében a modern ipari baromfitartás körülményei között jelentkeznek.
A tanulmány céljai között szerepelt a Krasznojarszk Területen található baromfitelepeken meglévő immunizálási programok, valamint kezelési és megelőző intézkedések sémák tanulmányozása; a csirkepusztulás szerkezetének retrospektív elemzése; homeosztatikus és immunológiai szervek és szövetek citomorfológiai vizsgálata
a baromfitermékekben található gyógyászati szennyeződések maradék mennyiségének gikus támogatása és tanulmányozása.
A kutatás anyagai és módszerei. A vizsgálatokat a Krasznojarszk Terület baromfitelepein, az Alkalmazott Biotechnológiai és Állatorvosi Intézet Állatanatómiai és Szövettani Osztályán, valamint a Krasznojarszki Állami Agráregyetem mezőgazdasági nyersanyagok és élelmiszerek minőségellenőrzésére szolgáló vizsgálati központjában végezték. 2000 és 2010 között. E cél elérése érdekében a baromfitelepeken alkalmazott vakcinázási és kezelési és megelőző intézkedéseket elemezték, összefoglalták a baromfipusztulásról szóló állat-egészségügyi jelentés statisztikai anyagait, valamint a Krasznojarszk Terület Mezőgazdasági és Élelmiszerpolitikai Minisztériumától származó információkat és analitikai adatokat.
Az immunológiai és homeosztatikus támogató szervek és szövetek citomorfológiai állapotának felmérése magában foglalta a belső szervek (csecsemőmirigy, Fabricius bursa, lép, máj, vese, agy) abszolút és relatív tömegének növekedését, valamint szövettani állapotuk vizsgálatát. szerkezet; a morfobiokémiai vérparaméterek vizsgálata (vörösvértestek száma, leukociták, leukogram, ESR, biomembránok lipid-peroxidációs termékei stb.). A hematológiai és szövettani vizsgálatokat általánosan elfogadott módszerek szerint végeztük.
A baromfitermékekben található gyógyászati szennyeződések visszamaradó mennyiségének vizsgálatát a MUK 4.2026-95 szerinti élelmiszeripari termékek antibiotikum-meghatározásának expressz módszerével végeztük.
A kapott adatokat variációs statisztika módszerével dolgoztam fel Student-féle 1-teszt segítségével.
Kutatási eredmények és megbeszélés. A Krasznojarszki Területen kilenc ipari baromfitenyésztő vállalkozás működik különböző tulajdoni formákkal, amelyek tojótyúkok, brojlercsirkék és brojlerpulykák tenyésztésére szakosodtak. A Krasznojarszk Terület Mezőgazdasági és Élelmiszerpolitikai Minisztériumának információi és elemző anyagai szerint az ipari baromfitelepeken a különböző típusú baromfiállományok száma 2009-ben több mint 6 millió darab volt. Ez az állatállomány egy teljes biológiai szervezetnek tekinthető, amely koncepcionális megközelítést igényel az egészségével kapcsolatos problémák megoldásában, valamint átfogó állat-egészségügyi és egészségügyi intézkedések végrehajtásában.
Kutatásaink során megállapítottuk, hogy a fertőző betegségek specifikus megelőzésére a régió baromfitelepein változó intenzitású oltási programokat alkalmaznak. Az antigén-stimuláció készlete a baromfitenyésztő vállalkozás termelési specializációjától, a fiatal állatok nevelésének időtartamától, valamint más olyan gazdaságokkal való kereskedelmi és gazdasági kapcsolatoktól függ, ahonnan egy adott fertőzés behurcolható. Így a tojástermelésre szakosodott baromfitelepeken 110-120 napos tenyészidő alatt 7-15 alkalommal immunizálják a fiatal állatokat, a gazdaság járványos jóllététől függően. A baromfihús előállítására szakosodott vállalkozásoknál a brojlercsirkéket életük első 20 napjában 7-8 alkalommal vakcinázzák, 42 napos időtartammal. A brojlerpulyka állatállományát 130-135 tenyésztési nap alatt 9-10 alkalommal vakcinázzák. Ráadásul a teljes antigénterhelés 90%-a a madárra esik élete első két hónapjában.
Feltételezhető, hogy a térségbe behurcolt új, kevéssé vizsgált fertőző betegségek nyilvántartásba vételével a megelőzésükre készített vakcinák arzenálja folyamatosan bővül,
és ezért az immunizálási rendszerek egyre telítettebbek lesznek.
Minden átfogó vakcinázási program a keltetőkben kezdődik egy, gyakran két, egy napnál fiatalabb madarak vakcinázásával. Az egymást követő immunizálások közötti intervallum körülbelül 7-8 nap, egyes időszakokban 2-3 napra csökken. Ha a vakcinázás utáni antitestek alacsony titerét érik el, anélkül, hogy az állatállomány 80-100%-os immunitását elérnék, a baromfitelepeken dolgozó állatorvosok növelik az immunizálás gyakoriságát, minimalizálják az antigénstimulációk közötti intervallumokat, és még intenzívebbé teszik a specifikus prevenciós programot.
A vakcinák kiválasztásakor előnyben részesítik az élő vírus vakcinákat, amelyekre jellemző a viszonylag alacsony költség, valamint az erős és hosszan tartó immunitás létrehozásának képessége, amely intenzitása közel áll a fertőzés utáni immunitáshoz. Ez nem veszi figyelembe számos élő vakcina reaktogenitását, amely a vakcinavírusok tropizmusának köszönhető a limfociták membránszerkezetében. Ismeretes, hogy a fertőző bursalis betegség, a Marek-kór és a Newcastle-kór elleni vírusvakcinák erősen reaktogenikusak.
Egyes vakcinavírusok limfocitákra gyakorolt közvetlen citopátiás hatása mellett a baromfi immunizálása helyi és általános jellegű vakcinázás utáni reakciók kialakulásához vezet, amelyek megnyilvánulási foka gyakran az immunizálás módjától függ. Azt tapasztaltuk, hogy a vakcinák intramuszkuláris és szubkután beadása helyi reakciókat okozhat, például rövid ideig tartó fájdalmat és duzzanatot a vakcina beadásának helyén, amelyek két-három napon belül eltűnnek. Az intranazális, intraokuláris és aeroszolos vakcina beadási módszerekkel rhinitis és kötőhártya-gyulladás alakul ki, amelyek a legkifejezettebbek az aeroszolos immunizálási módszerrel. Az oltás utáni reakciók kevésbé kifejezettek, ha ivási módszerrel oltják be.
A vakcinázott állatállomány morfofunkcionális állapotának felmérése során azt találtuk, hogy az immunizálások ESR-szint növekedést és leukocitózis kialakulását okozzák, elsősorban a limfociták miatt. Így a naposcsibék Marek-kór és fertőző hörghurut elleni oltása a limfociták abszolút és relatív mennyiségének közel háromszoros növekedését okozza az élet első hetében (P<0,001). Высокий уровень лимфоцитов в крови сохраняется в течение двух последующих месяцев, пока птица подвергается интенсивным антигенным стимуляциям. В отдельных случаях относительное содержание лимфоцитов в крови достигает 80-85%, при норме 52-60%, а гранулоцитов - 12-15% при норме 24-30%. При этом в популяции лимфоцитов антигенстимулированных цыплят значительное место занимают большие гранулярные лимфоциты (рис. 1). По мнению Ройта А. с соавторами, большие гранулярные лимфоциты функционально являются цитотоксическими лимфоцитами, играющими ведущую роль в защите организма от вирусных инфекций .
Rizs. 1. Nagy szemcsés limfocita immunizált csirke vérében.
Pappenheim festés. Uv. 1000
Az immunkompetens szervek morfofunkcionális vizsgálatai azt mutatják, hogy az első immunizálás serkenti növekedésüket és fejlődésüket. A naposcsibék Marek-kór elleni immunizálását követő első napon a csecsemőmirigy abszolút tömege 5-6%-kal, a relatív tömege 6-15%-kal nő a kiindulási állapothoz képest. Ha egy napos madarat egyidejűleg több antigénnel stimulálnak, a különbség a kontroll nem immunizált madárhoz képest eléri a 20%-ot.
A csecsemőmirigy abszolút tömegének növekedése az antigénstimuláció során elsősorban a lebenyek kérgi anyagának felső rétegének limfocitáinak proliferációjának köszönhető, amit a mitotikus index 2-2,5-szeres növekedése is bizonyít a nem vakcinázott csirkékhez képest. (P<0,001). Корковая зона расширяется, нарастает плотность лимфоцитов в условном поле зрения коры и медуллы, усиливается пиронинофилия субкапсулярной зоны. Пролиферативные процессы сопровождаются полнокровием тимуса, отечностью и разрыхлением междольковой соединительной ткани, активизацией эндотелия мелких сосудов.
A csecsemőmirigy rövid távú hiperpláziája, amely bármely élő vírus vakcina beadására válaszul alakul ki, a véletlen involúció I. stádiumára jellemző. Az immunizálások közötti hosszú időközökkel (12-14 nap vagy több) a hiperpláziát a csecsemőmirigy abszolút és relatív tömegének csökkenése, a szerv apoptózis miatti limfociták általi pusztítása és a limfociták migrációja váltja fel, ami a II. stádiumra jellemző. és III. véletlen involúció, amelyek kialakulása maguknak a vakcinavírusoknak immunszuppresszív hatásával hozható összefüggésbe.
Az oltások és az újraoltások közötti intervallumok 2-5 napra csökkentése, mivel korlátozott ideig többszöri ütemezett immunizálásra van szükség, limfofollikuláris hiperplázia kialakulásához vezet a csecsemőmirigyben, amelyet limfoid tüszők megjelenése jellemez a medullában. 2. ábra) és a lebenyek kortikális zónájában (3. ábra), amelyek a normál mirigyben nem találhatók meg.
Rizs. 2. Limfociták tüszőszerű felhalmozódása (nyilakkal jelölve) a csecsemőmirigyben.
Életkor 95 nap. Hematoxilin-eozin. Uv. 100
Rizs. 3. A csecsemőmirigy limfofollikuláris hiperpláziája. 120 napos kor.
Hematoxilin-alciánkék. Uv. 100
A csecsemőmirigy limfofolikuláris hiperpláziája egyes szerzők szerint a szervezet autoimmun és allergiás reakcióinak eredménye, és a mirigy funkcionális aktivitásának csökkenése kíséri a T-limfociták érett formáinak csökkenése és csökkenése miatt. a csecsemőmirigy biológiailag aktív anyagainak kiválasztásában.
A Fabricius bursa az első immunizálásra a nyiroktüszők hiperpláziájával és az interfollikuláris és szubepitheliális kötőszövetben plazmacitikus reakció kialakulásával reagál. 1-1,5 hónapos korig azonban öt-hétszeri oltás után csökken a szerv abszolút és relatív tömege, mirigyes struktúrák, ciszták alakulnak ki a tüszők helyén, ami különösen
fertőző bursalis betegség elleni immunizálás után jellemző. A 2-3 hónapos madarakban az antigén stimulációk száma csökken, és a bursa abszolút tömege ismét növekedni kezd.
A védőoltások serkentik a lép fehér pépének kialakulását, amelyet a nyiroktüszők számának és méretének növekedése, valamint a periarteriális limfoid felhalmozódás jellemez. A vörös pulpában plazmacitikus reakció alakul ki, amelynek intenzitása az immunizálás teljes időtartama alatt magas szinten marad.
A 100-110 napos madár csecsemőmirigyében és lépében a 100-110 napos madár csecsemőmirigyében és lépében megjelenik a kis erek falának és a környező szöveteknek a plazma impregnálása, beleértve a 14-16 antigén stimulációt is magában foglaló komplex oltási programok végrehajtását a vérben keringő, a szervekben rögzíthető immunkomplexek hatása, funkcionális jellemzőik megváltoztatása (4. ábra).
Rizs. 4. A csecsemőmirigy medulláris zónájában (balra) és a lépben (jobbra) a kis erek falának és a környező szövetek plazma permeációja. 120 napos kor. Hematoxilin-alciánkék.
Uv. 100 (balra) és 400 (jobbra)
Figyelembe véve a baromfiállományt és az oltások gyakoriságát, elmondható, hogy a régióban évente több tízmillió vírusfertőzés elleni oltást végeznek. A baromfi hatalmas biológiai tömege van folyamatosan kitéve vakcina antigéneknek, amelyek közül néhány potenciális veszélyt jelent az immunpatológiás állapotok kialakulására, ami a vakcinázás utáni immunogenezis más betegségekkel szembeni gátlásában, a beoltott madarak jelentős mortalitásában és a fertőzésekkel szembeni fokozott érzékenységben nyilvánul meg. opportunista mikroflóra. Ezenkívül az antigének ellenőrizetlen ismételt beadásával antigénekből és antitestekből álló keringő immunkomplexek rögzülnek a szövetekben, az erek falában, ami anafilaxiás reakciókat okozhat.
A madár szervezetének adaptív szerkezetátalakítása, amely a vírusvakcinák általi antigénstimuláció hatására megy végbe, fokozott rezisztenciát eredményez a vírusfertőzésekkel szemben, de csökkenti a bakteriális betegségek elleni védelem szintjét.
Az opportunista mikroflóra által okozott és számos immunizálás hátterében fellépő bakteriális fertőzések megelőzésére a baromfitelepeken komplex kezelési és megelőző intézkedéseket alkalmaznak. A baromfitenyésztésben használt gyógyszerek arzenálja szokatlanul széles és változatos. Tartalmazza a baromfi termelékenységének növeléséhez, a takarmány minőségének megőrzéséhez, a fertőző és nem fertőző betegségek megelőzéséhez és kezeléséhez szükséges gyógyszereket. A kezelési és megelőző kezelési sémák elemzése kimutatta az antimikrobiális gyógyszerek (antibiotikumok, szulfonamidok, nitrofuránok, kokcidiosztatikumok stb.) elterjedtségét, amelyeket a baromfi kezelésére az élet első napjától kezdve és a teljes tenyészidőszakban alkalmaznak. A leggyakrabban használt gyógyszerek az aliciklusos szerkezetek - tetraciklinek, amelyek széles terápiás hatással és minimális metabolizmussal rendelkeznek.
Az antimikrobiális szerek széles körű alkalmazása elnyomja az opportunista mikroflórát, és lehetővé teszi az intenzív immunizálások által kiváltott bakteriális fertőzések kitörésének megfékezését. Az állat-egészségügyi jelentési dokumentumok elemzése a régióban a fertőző betegségek számának jelentős csökkenését mutatta ki.
betegségek a baromfi mortalitás szerkezetében a 2003 és 2009 közötti időszakban. Az intenzív antibiotikum-használat ellenére azonban továbbra is a colibacillosis a fiatal madarak elhullásának fő oka mindenhol. Részesedése a mortalitási szerkezetben az összes regisztrált fertőző betegség 63-96%-át teszi ki, és a colibacillosis miatt elpusztultak 98-99%-a csirke az élet első két hónapjában. Ennek a betegségnek általában rejtett lefolyása van, azonban a madarak kedvezőtlen tételeiben a vakcinázás kiváltó oka lehet a fertőzés megnyilvánulásának.
A hosszan tartó antibiotikumok szerves károsodást okozhatnak a gyomor-bél traktusban, és kifejezett nefrotoxikus és hepatotoxikus hatást mutathatnak. A régióban található baromfitelepeken a fiatal baromfi mortalitás szerkezetének elemzése kimutatta, hogy az emésztőszervek patológiája 28%, a máj -12%, a vese pedig -11%-a az összes nem fertőző betegségnek (5. ábra).
■ a légzőrendszer patológiája ■ az emésztőrendszer patológiája
■ embrionális fejletlenség ■ alultápláltság
□ hepatitis □ nephritis
□ omphalitis □ egyéb
Rizs. 5. Fiatal madarak nem fertőző betegségek miatti elhullásának szerkezete a Krasznojarszk Területen
2008-ra
A brojlercsirkék homeosztatikus szerveinek morfológiai vizsgálatai kimutatták, hogy a baromfi fejlődésének korai szakaszát a máj, a vesék és kisebb mértékben az agy magas növekedési üteme jellemzi. A fejlődés első két-három hetében a szervek különösen intenzív növekedése figyelhető meg, ami mindig a sejtek magas mitotikus aktivitásával jár. A csirke fejlődésének ebben az időszakában következik be a maximális gyógyszerexpozíció, amely hepato- és nephropathiák megjelenéséhez vezethet, és ennek következtében a máj és a vesék méregtelenítő és kiválasztó képességének csökkenéséhez.
A tetraciklinnek a fiatal csirkék szervezetére gyakorolt kísérleti gyógyhatása körülményei között azt találtuk, hogy a brojlercsirkék szervezetében a hepato- és nefrociták citoplazmájának szétesési folyamatai fejlődnek ki, a foszfolipidek szabad gyökös oxidációjának termékei képződnek. növekszik a biomembránok mennyisége, ami a xenobiotikus anyagcsere-folyamatok aktivitásának gátlásához és citotoxikus hatások kialakulásához vezet.
A hosszú ideig oxitetraciklint kapó csirkék májában és veséjében a disztrófiás és gyulladásos reakciók kialakulása a biomembránok lipid-peroxidációjának aktiválásával, a membránhoz kötött enzimek: alanin és aszpartát aminotranszferázok aktivitásának növekedésével, dysprotenémia kialakulásával jár együtt. , hiperbilirubinémia, hiperkoleszterinémia, hipoglikémia, az ESR növekedése és a vér leukocita profiljának megváltozása.
Adataink szerint hosszú távú antibiotikum-használat mellett nemcsak a gyomor-bél traktus és a baromfi homeosztatikus szerveinek károsodásának kockázata nő, hanem a baromfitermékek szennyeződésének valós veszélye is fennáll, különösen a brojlercsirke termelés során. hús, maradék antibiotikumokkal. Egyes adatok szerint az állatgyógyászati készítmények, különösen az antibiotikumok maradék mennyisége a baromfitermékek 15-26%-ában található, ami összhangban van más szerzőkkel. A vizsgált antibakteriális szerek közül leggyakrabban a tetraciklint mutatják ki, amely minden élelmiszer-típusban megtalálható, de leggyakrabban a húsban és a baromfitojásban, valamint ezek feldolgozott termékeiben.
Véleményünk szerint az antibakteriális szerek élelmiszerekbe való bejutásának egyik fő oka a különböző gyógyászati xenobiotikumok lavina citotoxikus hatása miatt a máj és a vese méregtelenítő és kiválasztó funkciójának csökkenése lehet. Ezért lehetséges, hogy
Az antibiotikumok emberi szervezetbe juttatása a megengedett napi bevitel (ADI) feletti táplálékkal, ami a bél mikroökológiájának megzavarásához vezethet, allergiás reakciókat, máj- és vesekárosodást okozhat, valamint rezisztens mikroorganizmus-törzsek megjelenését idézheti elő.
Ez a cikk csak néhány problémát vizsgál meg, amelyek a specifikus és nem specifikus betegségmegelőzési szerek ipari baromfitenyésztésben történő integrált használatával kapcsolatosak. A vizsgálatok eredményei azonban lehetővé teszik, hogy a következő következtetéseket vonjuk le:
2. A baromfi specifikus prevenciós programok végrehajtása során végzett antigénstimulálása citomorfológiai változások komplexét idézi elő az immunológiai támogatást biztosító szervekben és szövetekben, ami egyrészt a szervezet fokozott vírusellenes védekezéséhez vezet, másrészt kéz, csökkenti a bakteriális fertőzésekkel szembeni ellenállást.
3. A nem specifikus profilaxis intenzív alkalmazása a bakteriális fertőzések kitörésének potenciális veszélye miatt a homeosztatikus szervek mikroszerkezeti károsodásához, méregtelenítő és kiválasztó tulajdonságaik csökkenéséhez, valamint a baromfitermékek gyógyászati szennyezőanyagokkal való szennyezettségének csökkenéséhez vezet.
Irodalom
1. Birman B.Ya., Nasonov I.V. A madarak fertőző bursalis betegségének vakcinamegelőzési programja a jelenlegi szakaszban // Proceedings of the 1st International. állatorvos. kongr. a baromfitenyésztésről. - M., 2005. - P.115-117.
2. Gomboev D.D. Állatok iatrogén betegségei (antibiotikumok hosszú távú alkalmazása) // Járványtan, diagnosztika, megelőzés és az állatbetegségek leküzdésére irányuló intézkedések: gyűjtés. tudományos tr. - Novoszibirszk, 1997. - P.341-342.
3. Javadov E.D. Vírus által kiváltott immunszuppresszió és megelőzésének módszerei az ipari baromfitenyésztésben: absztrakt. dis. ...Dr. állatorvos. Sci. - M., 2004. - 49 p.
4. Inaktivált vakcinák „Avikron” - a madárbetegségek hatékony megelőzése az ipari baromfitenyésztésben / E.D. Javadov [és mások] // Állatorvoslás. - 2009. - 6. sz. - 13-15.o.
5. Donkova N.V. Tanyasi madarak citofunkcionális endoökológiája orvosi xenobiotikumok hatására: monográfia. / Krasznojarszk állapot mezőgazdasági univ. - Krasznojarszk, 2004. - 268 p.
6. A csecsemőmirigy patológiája gyermekeknél / T.E. Ivanovskaya [és mások]. - Szentpétervár: SOTIS, 1996. - 270 p.
7. Kashkin K.P., Karaev Z.O. A szervezet immunreaktivitása és az antibiotikum terápia. - L.: Medi-
Tsina, 1984. - 200 p.
8. MUK 4.2.026-95. Expressz módszer az antibiotikumok állati termékekben történő meghatározására. - Belép. 03.29.95. - M.: Orosz Goskomsanepidnadzor, 1995. - 18 p.
9. Nekrutov A.V. Az inaktivált vakcina hatékonysága a Gumboro-betegség megelőzésére csirkékben // Állatorvoslás. - 2007. - 1. sz. - 25-28.o.
10. Pronin A.V. Immunmoduláció és vakcina profilaxis: tapasztalatok a fosprenil gyógyszerrel // Ros. állatorvos. magazin - 2005. - 1. sz. - 42-44.
11. Royt A., Brostoff J., Meil D. Az immunválaszt végző sejtek // Immunology. - M.: Mir, 2000. - P.18-20.
12. A csecsemőmirigy betegségei / V.P. Harcsenko [és mások]. - M.: Triada, 1998. - 232 p.
13. Donoghue D.J., Hairston H. Oxitetraciklin átvitele csirke tojássárgájába vagy albumenbe // Poultry Sc. - 1999. -
Vol. 78. - 3. sz. - P. 343-345.
14. Furusawa N. Tojótyúkok tojásainak és tojásképző szöveteinek spiramicin-, oxitetraciklin-, szulfamometoxin-tartalma // J. veter. Med. Ser. A. - 1999. - 1. évf. 46 - 10. sz. - P.599-603.
15. Yassin S.F. A csecsemőmirigy sebészete // eMedicine Specialties. Mellkassebészet, 2009. - 20. évf. 4. - URL: http://emedicine.medscape.com/article/427053-overview (Hozzáférés: 2009. 12. 08.).
Drog terápia.
A fertőző betegségek modern terápiája magában foglalja a különböző típusú kezelések komplex alkalmazását. Olyan gyógyszerek alkalmazását, amelyek hatása a betegség okának megszüntetésére irányul, ún etiotróp terápia . Az etiotróp gyógyszerek hatásának alkalmazási pontja fertőző betegeknél a betegségük kórokozói, a cél pedig a létfontosságú tevékenység visszaszorítása vagy ezeknek a kórokozó mikrobáknak a teljes elpusztítása.
Az etiotróp terápia alapja az antibiotikumok és a kemoterápiás gyógyszerek. Az antibiotikumok felfedezése és a klinikai gyógyászatban való széles körű elterjedése hozzájárult a fertőző betegségekből eredő mortalitás tízszeres csökkenéséhez és a szövődmények előfordulásának csökkenéséhez. Később azonban világossá vált, hogy az antibiotikumok a normális emberi mikroflórát is befolyásolhatják, és olyan ma már oly gyakori állapotot okoznak, mint a dysbiosis. Ebben a tekintetben óvatosság és szorgalom szükséges az antibiotikumok felírásakor. Az antibiotikumokat semmilyen esetben sem szabad a legkisebb hőmérséklet-emelkedésnél alkalmazni, mivel az ilyen terápia következményei sokkal súlyosabbak lehetnek, mint maga a betegség, amelyre felírták. Az antibiotikumok többféleképpen adhatók be a szervezetbe: bőrön (topikusan), orálisan, inhalálva, rektálisan (kúpok formájában), intramuszkulárisan, intravénásan és savós üregekbe.
Kemoterápiás gyógyszerek - kémiai szintézissel nyert anyagok, amelyek káros hatással vannak a fertőző betegségek kórokozóira.
A patogenezis fő láncszemeire ható, ezáltal a szervek és rendszerek károsodott működését kiküszöbölő, a makroorganizmus védőmechanizmusait erősítő gyógyszerek alkalmazását nevezzük. patogenetikai terápia .
A feladat tüneti terápia célja a beteg szenvedésének enyhítése a betegség egyéni fájdalmas megnyilvánulásainak kiküszöbölésével, de a fertőző betegek kezelésében nem annyira alapvető fontosságú, mint az előző kettő. A tüneti terápia módszerei és eszközei különböző fájdalomcsillapítók, altatók, allergia-, lázcsillapító és számos egyéb gyógyszer alkalmazása.
A hatás jellegétől függően minden gyógyszer két csoportra osztható: specifikus és nem specifikus hatások.
Konkrét akció alatt a drogokon olyan cselekvést értünk, amely mindig szigorúan meghatározott biológiai hatást vált ki. A terápiás arzenálban a specifikus szerek között a biológiai eredetű gyógyszerek dominálnak. Közös jellemzőjük a fertőző betegségek megelőzésére, kezelésére és diagnosztizálására való alkalmazásuk lehetősége. A specifikus hatású készítmények közé tartoznak például a szérumok, immunglobulinok és bakteriofágok. Ezen gyógyszerek mindegyike csak egy szigorúan meghatározott betegség esetén fejt ki terápiás hatást. Pl. diftéria elleni szérum - diftéria, vérhas bakteriofág Shigella ellen hat, stb.
v Bakteriofágok(a görög phagos - zabáló, azaz felfaló baktériumok szóból) szerkezetükben közel állnak a vírusokhoz, és a baktériumok élő, aktívan szaporodó formáira hatnak, pusztulásukat (lízisüket) okozva. A bakteriofágok hatásának sajátossága, hogy csak bizonyos típusú mikrobiális sejtekkel tudnak kölcsönhatásba lépni, és nem képesek kölcsönhatásba lépni a test sejtjeivel, ami miatt a bakteriofágok teljesen biztonságosak az ember számára. Terápiás és profilaktikus célokra a bakteriofágokat tabletták formájában (saválló bevonattal) és folyékony formában (palackokban) állítják elő.
A klinikai gyakorlatban a fágterápiát főként akut bélbetegségek esetén alkalmazzák.
v Szeroterápia. A terápiás és profilaktikus immunkészítményeket széles körben használják szérumok vagy azokból kinyert specifikus frakciók (immunglobulinok) formájában bizonyos fertőző betegségek sürgősségi megelőzése és kezelése céljából.
Az ebbe a csoportba tartozó készítményeket mesterségesen immunizált állatok (általában lovak) véréből, valamint olyan személyek véréből nyerik, akik a megfelelő fertőző betegségekben szenvedtek, vagy akiket a megfelelő vakcinákkal immunizáltak. Az immunizáláshoz használt gyógyszerektől függően antibakteriális, vírusellenes és antitoxikus szérumokat különböztetnek meg. Az ilyen szérumkészítmények kész antitesteket tartalmaznak, amelyek semlegesíthetik a patogén mikrobák vagy toxinjaik hatását.
Így a szérumok bevezetése lehetővé teszi a passzív immunitás nagyon rövid időn belüli létrehozását, ami különösen fontos a rövid lappangási idővel járó fertőző betegségek sürgősségi megelőzésében vagy egy már kialakult betegség (például botulizmus, diftéria).
A hiperimmun szérumok beadásával létrejövő passzív immunitás rövid életű és 1-2 hétre korlátozódik, ezt követően a specifikus antitestek kiürülnek a szervezetből. Terápiás célokra a szérumot intramuszkulárisan vagy intravénásan adják be, és csak kórházi környezetben, mivel használatuk a beteg állapotának folyamatos ellenőrzését igényli.
Nem specifikusan ható szerek szélesebb körű reakciókat váltanak ki a szervezetben, ahol a hasznos, terápiás hatásúak mellett mellékhatások, haszontalanok, sőt károsak is léteznek.